
�����ʵ�����NaHCO3��KHCO3�Ļ����9.20g��100mL���ᷴӦ��
��1���Է����������״�������ɵ�CO2���ʱ������Ҫ�����ݣ���a��b�ȱ�ʾ��Ҫע����λ����___________��
��2�����״�������ɵ�CO2�������
|
�������ݵ�ȡֵ��Χ |
����CO2���������״���� |
|
�����ʱ |
|
|
�������ʱ |
|
��3����NaHCO3��KHCO3���ǵ����ʵ�����ϣ���9.20g������������ȫ��Ӧʱ�ڱ�״��������CO2���������_______L��С��______L.

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
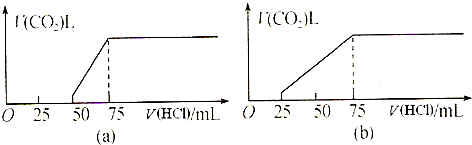
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
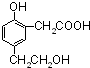 ���õ����ʵ����ĸ��л���ֱ���Na��NaOH��NaHCO3��Ӧʱ��������Na��NaOH��NaHCO3�����ʵ���֮��Ϊ��������
���õ����ʵ����ĸ��л���ֱ���Na��NaOH��NaHCO3��Ӧʱ��������Na��NaOH��NaHCO3�����ʵ���֮��Ϊ���������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ��ѧʽ | HF | H2CO3 | HClO |
| ����ƽ�ⳣ�� ��K�� |
7.2��10-4 | K1=4.4��10-7 K2=4.7��10-11 |
3.0��10-8 |
 ������˵����ȷ����
������˵����ȷ���� SO2Cl2��l����H=-97.3kJ?mol-1
SO2Cl2��l����H=-97.3kJ?mol-1�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������������ ���ͣ�013
��֪��Ȼ������Ҫ�ɷ� ��һ�ֻ��������ЧӦ�����壬�����ʹ�����
��һ�ֻ��������ЧӦ�����壬�����ʹ����� ��
�� ����������ЧӦ��ǰ�ߴ������й���Ȼ���ļ�����������ȷ����
����������ЧӦ��ǰ�ߴ������й���Ȼ���ļ�����������ȷ����
����Ȼ����ú����������ǽ�������Դ
�ڵ������� ��
�� ����������ЧӦҲ��ǰ�ߴ�
����������ЧӦҲ��ǰ�ߴ�
��ȼ����Ȼ��Ҳ������ij���֮һ
[����]
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�013
��֪��Ȼ������Ҫ�ɷ� ��һ�ֻ��������ЧӦ�����壬�����ʹ�����
��һ�ֻ��������ЧӦ�����壬�����ʹ����� ��
��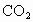 ����������ЧӦ��ǰ�ߴ������й���Ȼ���ļ�����������ȷ����
����������ЧӦ��ǰ�ߴ������й���Ȼ���ļ�����������ȷ����
����Ȼ����ú����������ǽ�������Դ
�ڵ������� ��
��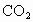 ����������ЧӦҲ��ǰ�ߴ�
����������ЧӦҲ��ǰ�ߴ�
��ȼ����Ȼ��Ҳ������ij���֮һ
[����]
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com