
| ��ѧʽ | HF | H2CO3 | HClO |
| ����ƽ�ⳣ�� ��K�� |
7.2��10-4 | K1=4.4��10-7 K2=4.7��10-11 |
3.0��10-8 |
 ������˵����ȷ����
������˵����ȷ���� SO2Cl2��l����H=-97.3kJ?mol-1
SO2Cl2��l����H=-97.3kJ?mol-1| 1 |
| c(SO2)��c(Cl2) |
| 1 |
| c(SO2)��c(Cl2) |


 �óɼ�1��1��ĩ���100��ϵ�д�
�óɼ�1��1��ĩ���100��ϵ�д� ��״Ԫ���źþ�ϵ�д�
��״Ԫ���źþ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� | ��ⷽ��ʽ | ����ƽ�ⳣ�� |
| CH3COOH | CH3COOH?CH3COO-+H+ | K=1.76��10-5 |
| H2CO3 | H2CO3?HCO3-+H+ HCO3-?CO32-+H+ |
K1=4.31��10-7 K2=5.61��10-11 |
| H2S | H2S?HS-+H+ HS-?S2-+H+ |
K1=9.1��10-8 K2=1.1��10-15 |
| H3PO4 | H3PO4?H2PO4-+H+ H2PO4-?HPO42-+H+ HPO42-?PO43-+H+ |
K1=7.52��10-3 K2=6.23��10-8 K3=2.20��10-13 |
| c��2 |
| 1-�� |
| c��2 |
| 1-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010��㶫ʡִ����ѧ�߶���ѧ�����п��Ի�ѧ�� ���ͣ������
�������ᣬ��һ���¶��´ﵽ����ƽ��ʱ��������Ũ�ȴ���һ�ֶ����Ĺ�ϵ���±���25��ʱ���ֳ�������ĵ���ƽ�ⳣ��
| �� | ���뷽��ʽ | ����ƽ�ⳣ��K |
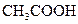 | 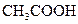  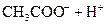 |  |
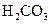 |  | 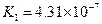 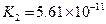 |
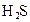 | 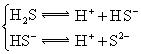 | 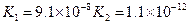 |
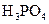 | 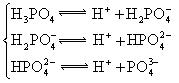 | 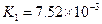 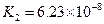 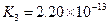 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�����ʡ�����и����ڶ���ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ������
��.����ƽ�ⳣ������K��ʾ)�Ĵ�С�����жϵ���ʵ����ǿ����25��ʱ���й����ʵĵ���ƽ�ⳣ�����±���ʾ��
|
��ѧʽ |
HF |
H2CO3 |
HClO |
|
����ƽ�ⳣ�� ��K�� |
7.2��10-4 |
K1=4.4��10-7 K2=4.7��10-11 |
3.0��10-8 |
��1�����ʵ���Ũ�Ⱦ�Ϊ0.1mol/L������������Һ����Na2CO3��Һ ��NaHCO3��Һ ��NaF��Һ ��NaClO��Һ�����������ж�pH�ɴ�С��˳����______________��
��2��25��ʱ����20mL0.1mol��L��1������м���VmL0.1mol��L��1NaOH��Һ����û����Һ��pH�仯������ͼ��ʾ������˵����ȷ����_______��

A��pH��3��HF��Һ��pH��11��NaF��Һ�У���ˮ�������c(H+)���
B���ٵ�ʱpH��6����ʱ��Һ�У�c(F��)��c(Na+)��9.9��10-7mol/L
C���ڵ�ʱ����Һ�е�c(F��)��c(Na+)
D���۵�ʱV��20mL����ʱ��Һ��c(F��)<c(Na+)��0.1mol��L��1
��3����֪25��ʱ����HF(aq)+OH��(aq)��F��(aq)+H2O(l) ��H��-akJ��mol��1��
��H+(aq)+OH��(aq)��H2O(l) ��H��-bkJ��mol��1��
�����ĵ��뷽��ʽ����ЧӦ�ɱ�ʾΪ________________________��
��4������������һֱ��Ϊ���ĺ�������ڡ�1971��������ѧ���÷���ͨ��ϸ��ĩʱ���HFO����ṹʽΪH��O��F��HFO������ʵ�����H2O��Ӧ�õ�HF�ͻ�����A����ÿ����1molHFת��_______mol���ӡ�
��.�Ȼ�������SO2Cl2����Ҫ�����Ȼ���������һ����ɫҺ�壬�۵�C54.1�棬�е�69.1�档�Ȼ��������ø���Ķ�������������ڻ���̿���������·�Ӧ��ȡ��
SO2(g)��Cl2(g) SO2Cl2(l) ��H���C97.3kJ��mol��1
SO2Cl2(l) ��H���C97.3kJ��mol��1
��1����д�����³�ѹ�»�ѧƽ�ⳣ��K�ı���ʽ��K=_________________��
��2����������Ӧ����Ҫʹ��ѧƽ�ⳣ��K����ѧ��Ӧ����v��Ҳ���ɲ�ȡ�Ĵ�ʩ��_____��ѡ���ţ���
a�������¶� b������SO2Cl2
c�����ӷ�Ӧ��Ũ�� d����������������
��3��������������˵��������Ӧ�Ѵ�ƽ�����____________��ѡ���ţ���
a����(Cl 2)����(SO2) b������������ѹǿ����ʱ����仯
c��c(Cl 2) : c(SO2)��1:1 d��������������ɫ����ʱ�����仯
��4��300��ʱ�����Ϊ1L���ܱ������г���16.20g SO2Cl2���ﵽƽ��ʱ�����к�SO2 7.616g�����������е�ƽ����ϵ�У��ټ���16.20g SO2Cl2�����ٴδ�ƽ��ʱ�������к�SO2��������Χ��________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010��㶫ʡ�߶���ѧ�����п��Ի�ѧ�� ���ͣ������
�������ᣬ��һ���¶��´ﵽ����ƽ��ʱ��������Ũ�ȴ���һ�ֶ����Ĺ�ϵ���±���25��ʱ���ֳ�������ĵ���ƽ�ⳣ��
|
�� |
���뷽��ʽ |
����ƽ�ⳣ��K |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
�ش����и��ʣ�
��1��Kֻ���¶��йأ����¶�����ʱ��Kֵ________�����������С���������䡱����
��2�����¶���ͬʱ���������Kֵ��ͬ����ôKֵ�Ĵ�С�����Ե����ǿ���кι�ϵ?__________________��
��3������CH3COOH��H2CO3��HCO3-��H2S��HS-��H3PO4��H2PO4-��HPO42-���������ᣬ����������ǿ����_________����������________��
��4����Ԫ�����Ƿֲ�����ģ�ÿһ��������Ӧ�ĵ���ƽ�ⳣ��������ͬһ�ֶ�Ԫ�����K1��K2��K3֮������������ϵĹ��ɣ�����H3PO4�˹�����________________�������˹��ɵ�ԭ����_________________________��
 ��5������ƽ�ⳣ������ʵ��ķ����ⶨ�����ģ����Ѿ����ij�¶��� NH3∙H2O��Һ�д������·�Ӧ��NH3∙H2O NH4++OH-
��֪0.10 mol��L-1
NH3∙H2O��Һ�У��ﵽƽ��ʱ��Cƽ����OH-��=4.2 �� 10-3mol��L-1��Cƽ����NH3∙H2O����C��ʼ��NH3∙H2O����ˮ�ĵ���ɺ��Բ���;
��5������ƽ�ⳣ������ʵ��ķ����ⶨ�����ģ����Ѿ����ij�¶��� NH3∙H2O��Һ�д������·�Ӧ��NH3∙H2O NH4++OH-
��֪0.10 mol��L-1
NH3∙H2O��Һ�У��ﵽƽ��ʱ��Cƽ����OH-��=4.2 �� 10-3mol��L-1��Cƽ����NH3∙H2O����C��ʼ��NH3∙H2O����ˮ�ĵ���ɺ��Բ���;
����pH��ֽ������Һ��pHֵ���������Cƽ����OH-�����ⶨ��ҺpHֵ�IJ�����______________��
�ڲ���Cƽ����NH3∙H2O���ķ��������_____________����������ƣ�
������¶��¸÷�Ӧ��ƽ�ⳣ��K.(д��������̣�����������2λ��Ч����)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com