
【题目】课题式研究性学习是培养学生创造性思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。
试回答下列问题:

(1)电源A极的名称是 。
(2)甲装置中电解反应的总化学方程式: 。
(3)如果收集乙装置中产生的气体,两种气体的体积比是 。
(4)欲用丙装置给铜镀银,G应该是 (填“铜”或“银”),电镀液的主要成分是 (填化学式)。
(5)装置丁中的现象是 。
【答案】(11分)(1)正极(2分)
(2)2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4 (3分)
2Cu+O2↑+2H2SO4 (3分)
(3)1∶1(2分)
(4)银(1分) AgNO3(1分)
(5)Y极附近红褐色变深(2分)
【解析】
试题分析:将电源接通后,向乙中滴入酚酞试液,在F极附件先显红色,说明F电极为阴极,则E为阳极,所以C、G、X都是阳极,D、H、Y都是阴极,
(1)连接阴极的电极负极、连接阳极的电极是正极,A连接阳极,则为正极,故答案为:正极;
(2)甲中阳极上氢氧根离子放电、阴极上铜离子放电生成铜,所以电池反应式为2CuSO4+2H2O![]() 2Cu+O2↑+H2SO4;
2Cu+O2↑+H2SO4;
(3)乙中阳极上氯离子放电生成氯气、阴极上氢离子放电生成氢气,生成相同物质的量的氢气、氯气时转移电子相等,电解过程中转移电子总数相等,所以生成氢气、氯气物质的量相等,相同条件下气体的物质的量之比等于体积之比,所以氯气和氢气体积之比为1:1;
(4)欲用丙装置给铜镀银,Ag作阳极、Cu作阴极,则G为银,电解质为AgNO3;
(5)氢氧化铁胶粒带正电荷,通电时向阴极移动,Y为阴极,所以看到的现象是Y极附近红褐色变深。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】乙醇燃料电池中采用磺酸类质子溶剂,在200 ℃左右时供电,电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意如图。下列说法中,错误的是
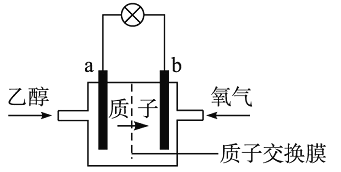
A.电池工作时,质子向电池的正极迁移
B.电池工作时,电流由b极沿导线流向a极
C.a极上发生的电极反应是C2H5OH+3H2O-8e-=2CO2+12H+
D.b极上发生的电极反应是4H++O2+4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】参考下列图表和有关要求回答问题。
(1)图Ⅰ是1 mol NO2(g)和1 molCO(g)反应生成CO2和NO过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是________,ΔH的变化是________(填“增大”“减小”或“不变”)。请写出NO2和CO反应的热化学方程式____________________;
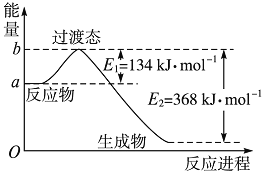
图Ⅰ
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1
则甲醇完全燃烧的热化学方程式为________________________;
(3)下表是部分化学键的键能数据:
化学键 | P—P | P—O | O=O | P=O |
键能/(kJ·mol-1) | a | b | c | x |
已知白磷的标准燃烧热ΔH为-d kJ·mol-1,白磷及其完全燃烧的产物结构如图Ⅱ所示,则上表中x=__________kJ·mol-1(用含有a、b、c、d的代数式表示)。
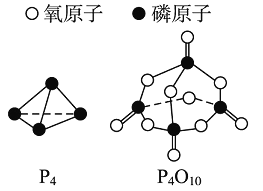
图Ⅱ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写及评价,均合理的是
选项 | 离子方程式 | 评价 |
A | 将2 mol Cl2通入到含1 mol FeI2的溶液中: 2Fe2++2I-+2Cl2===2Fe3++4Cl-+I2 | 正确;Cl2过量,可将Fe2+、I-均氧化 |
B | Ba(HCO3)2溶液与足量的NaOH溶液反应: Ba2++HCO | 正确;酸式盐与碱反应生成正盐和水 |
C | 过量SO2通入到NaClO溶液中: SO2+H2O+ClO-===HClO+HSO | 正确;说明酸性: H2SO3强于HClO |
D | 1 mol/L的NaAlO2溶液和2.5 mol/L的HCl溶液等体积互相均匀混合: 2AlO | 正确;AlO |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为制取硝酸铜,某同学设计了如下四种方法:①铜与浓硝酸反应制取硝酸铜;②铜与稀硝酸反应制取硝酸铜;③铜先与空气反应制取氧化铜,再与硝酸反应制取硝酸铜;④铜与硝酸银溶液反应制取硝酸铜。
(1)方法②中被氧化的铜与被还原的硝酸的物质的量之比是 。
(2)“绿色化学”是当今社会提出的一个新概念。在“绿色化学”工艺中,杜绝污染源,提高原子利用率是绿色化学的重要衡量指标。请从“绿色化学”和经济效益角度考虑,大量制取硝酸铜宜采用上述第 (填序号)种方法,原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质所发生的化学反应中,由于反应物的用量不同而得到不同产物的是
①铁与稀硝酸 ②硫酸铜溶液与氨水 ③碳酸钠溶液与稀盐酸 ④铁与氯气
A. ①②③ B. ①②③④ C. ②③ D. ③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com