
【题目】下列各组物质所发生的化学反应中,由于反应物的用量不同而得到不同产物的是
①铁与稀硝酸 ②硫酸铜溶液与氨水 ③碳酸钠溶液与稀盐酸 ④铁与氯气
A. ①②③ B. ①②③④ C. ②③ D. ③④
科目:高中化学 来源: 题型:
【题目】课题式研究性学习是培养学生创造性思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。
试回答下列问题:

(1)电源A极的名称是 。
(2)甲装置中电解反应的总化学方程式: 。
(3)如果收集乙装置中产生的气体,两种气体的体积比是 。
(4)欲用丙装置给铜镀银,G应该是 (填“铜”或“银”),电镀液的主要成分是 (填化学式)。
(5)装置丁中的现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前我国的火力发电机组绝大多数为燃煤机组,而以燃煤为主的电力生产所造成的环境污染是制约电力工业发展的一个重要因素,其中氮氧化物(NOx)是继粉尘和二氧化硫之后燃煤电站环保治理的重点。
(1)燃煤烟气脱硫的方法很多,如石灰石—石膏法、氨水法等。其中石灰石-石膏法脱硫的原理第一步是SO2+Ca(OH)2![]() CaSO3+H2O,然后再将产物氧化制成石膏,写出该反应的化学方程式: 。
CaSO3+H2O,然后再将产物氧化制成石膏,写出该反应的化学方程式: 。
(2)燃煤烟气脱硝可采用氨(NH3)作为还原介质,在催化剂及氧气存在的条件下,氮氧化物(NOx)与还原剂发生反应,生成无害的氮气和水,写出二氧化氮与氨反应的化学方程式: 。
(3)我国的环境空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:
浓度限值(mg·m-3) | ||
一级标准 | 二级标准 | 三级标准 |
0.15 | 0.50 | 0.70 |
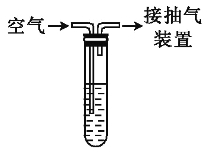
现有某化学兴趣小组按图所示的实验装置对某地空气中二氧化硫含量进行测定:向试管中加入1.00 mL 1.00×10-3 mol·L-1碘水,加入适量水,再加入2~3滴淀粉溶液使溶液显蓝色,通过抽气装置缓慢抽气,使空气由导气管进入试管与碘水充分反应,当溶液由蓝色变为无色时,恰好完全反应(反应的化学方程式:SO2+I2+2H2O![]() H2SO4+2HI),实验过程中进入试管内的空气的总体积为0.1 m3。请计算此空气中二氧化硫的浓度为多少mg·m-3,并判断二氧化硫的浓度级别为几级。
H2SO4+2HI),实验过程中进入试管内的空气的总体积为0.1 m3。请计算此空气中二氧化硫的浓度为多少mg·m-3,并判断二氧化硫的浓度级别为几级。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产硫酸过程中,SO2在接触室中被催化氧化为SO3,已知该反应为放热反应。现将2 mol SO2 、1 mol O2充入一密闭容器充分反应后,放出热量98.3 kJ,此时测得SO2的转化率为50%。下列热化学方程式正确的是
A.2SO3(g)![]() 2SO2(g)+O2(g);△H =+196.6 kJ/mol
2SO2(g)+O2(g);△H =+196.6 kJ/mol
B.2SO2(g)+O2(g)![]() SO3(g);△H =-98.3 kJ/mol
SO3(g);△H =-98.3 kJ/mol
C.SO2(g)+1/2O2(g)![]() SO3(g);△H=+98.3 kJ/mol
SO3(g);△H=+98.3 kJ/mol
D.SO2(g)+1/2O2(g)![]() SO3(g);△H=-196.6 kJ/mol
SO3(g);△H=-196.6 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为一种盐,C、D、F、N、O为无色气体,E常温常压下为无色无味的液体,N、H、L为高中常见的单质,I为常见无氧强酸,M的焰色反应为紫色,反应①常用于气体F的检验。
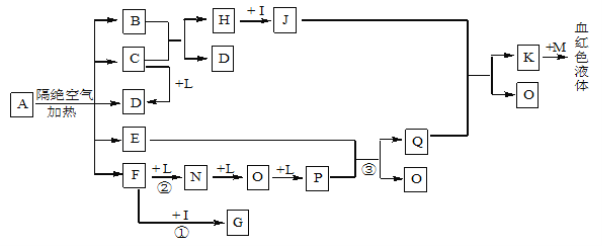
(1)写出D的电子式为_______________;
(2)写出反应①的化学方程式: ;写出反应②的化学方程式: ;反应③中氧化剂和还原剂的物质的量之比为_________________;
(3)将等体积、等浓度的G和F的溶液混合,溶液显碱性,则溶液中离子浓度从大到小的顺序为 ______________________;
(4)检验J中阳离子的实验方法为 ;
(5)已知B中氧元素的质量分数为22.2﹪,且A分解产生的各物质的物质的量之比为n(B):n(C): n(D):n(E):n(F)=1:2:2:1:2,则A的化学式为_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器中,加入X和Y各4mol,一定条件下发生化学反应:
2X(g)+ 2Y(g)![]() Z(g) + 2 W(g) △H <0, 反应进行到5s时达到化学平衡,测得X的转化率为25%,则下列说法正确的是
Z(g) + 2 W(g) △H <0, 反应进行到5s时达到化学平衡,测得X的转化率为25%,则下列说法正确的是
A.5s时,正、逆反应速率都达到最大
B.前5s内平均反应速率υ(Y)= 0.1 mol/( L·s)
C.达平衡时,各物质的浓度都保持不变,反应停止
D.升高温度,测得容器中密度不变时,表示该反应已经达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中盛有H2和Cl2混合气体体积为n L,用电火花引燃后,恢复到原来状态,气体体积不变。把气体通入足量的NaOH溶液,气体没有剩余,则原混合气体中H2与Cl2的物质的量比为( ):
A.≥1 B.≤1 C.=1 D.<1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】选择萃取剂将碘水中的碘萃取出来,这中萃取剂应具备的性质是
A. 不溶于水,且必须易与碘发生化学反应
B. 不溶于水,且比水更容易使碘溶解
C. 不溶于水,且必须比水密度大
D. 不溶于水,且必须比水密度小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是海水综合利用的一个方面。

请回答下列问题:
(1)①步主要反应的的离子方程式:_____________________________。
(2)分离出氢氧化镁的操作为__________,第③步需要加入_________。
(3)将粗食盐中含有的Mg2+、Ca2+和SO42—等杂质除去,加入的试剂有(按加入顺序填入)___________(只要求填一组合理的答案即可) 。
(4)⑤产物氢气在__________极生成,若电解食盐水时消耗NaCl的质量为234g,则在理论上最多可得氯气的体积为 升(标准状况)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com