
����Ŀ��Ŀǰ�ҹ��Ļ����������������Ϊȼú����,����ȼúΪ���ĵ�����������ɵĻ�����Ⱦ����Լ������ҵ��չ��һ����Ҫ����,���е�������(NOx)�Ǽ̷۳��Ͷ�������֮��ȼú��վ�����������ص㡣
(1)ȼú��������ķ����ܶ�,��ʯ��ʯ��ʯ�෨����ˮ���ȡ�����ʯ��ʯ-ʯ�෨�����ԭ����һ����SO2+Ca(OH)2![]() CaSO3+H2O,Ȼ���ٽ����������Ƴ�ʯ��,д���÷�Ӧ�Ļ�ѧ����ʽ: ��
CaSO3+H2O,Ȼ���ٽ����������Ƴ�ʯ��,д���÷�Ӧ�Ļ�ѧ����ʽ: ��
(2)ȼú���������ɲ��ð�(NH3)��Ϊ��ԭ����,�ڴ������������ڵ�������,��������(NOx)�뻹ԭ��������Ӧ,�������ĵ�����ˮ,д�����������백��Ӧ�Ļ�ѧ����ʽ: ��
(3)�ҹ��Ļ��������������жԿ����ж�����������Ũ��(��λ����Ŀ����������������������)��ֵ���±���ʾ:
Ũ����ֵ(mg��m-3) | ||
һ���� | ������ | ������ |
0.15 | 0.50 | 0.70 |
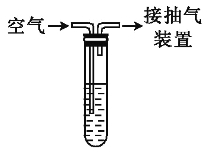
����ij��ѧ��ȤС�鰴ͼ��ʾ��ʵ��װ�ö�ij�ؿ����ж������������вⶨ:���Թ��м���1.00 mL 1.00��10-3 mol��L-1��ˮ,��������ˮ,�ټ���2~3�ε�����Һʹ��Һ����ɫ,ͨ������װ�û�������,ʹ�����ɵ����ܽ����Թ����ˮ��ַ�Ӧ,����Һ����ɫ��Ϊ��ɫʱ,ǡ����ȫ��Ӧ(��Ӧ�Ļ�ѧ����ʽ:SO2+I2+2H2O![]() H2SO4+2HI),ʵ������н����Թ��ڵĿ����������Ϊ0.1 m3�������˿����ж��������Ũ��Ϊ����mg��m-3,���ж϶��������Ũ�ȼ���Ϊ������
H2SO4+2HI),ʵ������н����Թ��ڵĿ����������Ϊ0.1 m3�������˿����ж��������Ũ��Ϊ����mg��m-3,���ж϶��������Ũ�ȼ���Ϊ������
���𰸡�(1)2CaSO3+O2![]() 2CaSO4(������д��2CaSO4��H2O��CaSO4��2H2OҲ��)
2CaSO4(������д��2CaSO4��H2O��CaSO4��2H2OҲ��)
(2)6NO2+8NH3![]() 7N2+12H2O
7N2+12H2O
��3������
��������(1)ʯ��ʯ-ʯ�෨������ʯ��ʯ�����ṩCaO,��һ���õ�Ca(OH)2,����SO2����CaSO3,CaSO3 ��������һ��������CaSO4,�õ�ʯ��;(3)�ɷ�Ӧ:SO2+I2+2H2O![]() H2SO4+2HI,�õ�n(SO2)=n(I2)=1.00��10-3L ��1.00��10-3 mol��L-1=10-6 mol,m(SO2)=10-6mol��64 g��mol-1��103 mg��g-1=0.064 mg,������SO2Ũ��==0.64 mg��m-3,����0.50 mg��m-3<0.64 mg��m-3<0.70 mg��m-3,�˿����ж��������Ũ��Ϊ������
H2SO4+2HI,�õ�n(SO2)=n(I2)=1.00��10-3L ��1.00��10-3 mol��L-1=10-6 mol,m(SO2)=10-6mol��64 g��mol-1��103 mg��g-1=0.064 mg,������SO2Ũ��==0.64 mg��m-3,����0.50 mg��m-3<0.64 mg��m-3<0.70 mg��m-3,�˿����ж��������Ũ��Ϊ������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ο�����ͼ�����й�Ҫ��ش����⡣
(1)ͼ����1 mol NO2(g)��1 molCO(g)��Ӧ����CO2��NO�����������仯ʾ��ͼ�����ڷ�Ӧ��ϵ�м����������Ӧ��������E1�ı仯��________����H�ı仯��________(�������С�����䡱)����д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ____________________��
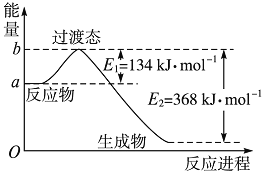
ͼ��
(2)�״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ���ǣ�
��CH3OH(g)��H2O(g)=CO2(g)��3H2(g) ��H����49.0 kJ��mol��1
��CH3OH(g)��![]() O2(g)=CO2(g)��2H2(g) ��H����192.9 kJ��mol��1
O2(g)=CO2(g)��2H2(g) ��H����192.9 kJ��mol��1
��֪��H2O(g)=H2O(l) ��H����44 kJ��mol��1
��״���ȫȼ�յ��Ȼ�ѧ����ʽΪ________________________��
(3)�±��Dz��ֻ�ѧ���ļ������ݣ�
��ѧ�� | P��P | P��O | O=O | P=O |
����/(kJ��mol��1) | a | b | c | x |
��֪���ı�ȼ���Ȧ�HΪ��d kJ��mol��1����������ȫȼ�յIJ���ṹ��ͼ����ʾ�����ϱ���x��__________kJ��mol��1(�ú���a��b��c��d�Ĵ���ʽ��ʾ)��
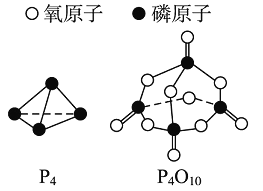
ͼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ����д�����ۣ�����������
ѡ�� | ���ӷ���ʽ | ���� |
A | ��2 mol Cl2ͨ�뵽��1 mol FeI2����Һ�У� 2Fe2����2I����2Cl2===2Fe3����4Cl����I2 | ��ȷ��Cl2�������ɽ�Fe2����I�������� |
B | Ba(HCO3)2��Һ��������NaOH��Һ��Ӧ�� Ba2����HCO | ��ȷ����ʽ����Ӧ�������κ�ˮ |
C | ����SO2ͨ�뵽NaClO��Һ�У� SO2��H2O��ClO��===HClO��HSO | ��ȷ��˵�����ԣ� H2SO3ǿ��HClO |
D | 1 mol/L��NaAlO2��Һ��2.5 mol/L��HCl��Һ�����������Ȼ�ϣ� 2AlO | ��ȷ��AlO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��ȡ����ͭ,ijͬѧ������������ַ���:��ͭ��Ũ���ᷴӦ��ȡ����ͭ;��ͭ��ϡ���ᷴӦ��ȡ����ͭ;��ͭ���������Ӧ��ȡ����ͭ,�������ᷴӦ��ȡ����ͭ;��ͭ����������Һ��Ӧ��ȡ����ͭ��
(1)�������б�������ͭ�뱻��ԭ����������ʵ���֮���� ��
(2)����ɫ��ѧ���ǵ�����������һ���¸���ڡ���ɫ��ѧ��������,�ž���ȾԴ,���ԭ������������ɫ��ѧ����Ҫ����ָ�ꡣ��ӡ���ɫ��ѧ���;���Ч��Ƕȿ���,������ȡ����ͭ�˲��������� (�����)�ַ���,ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ijѧ���Ļ�ѧʵ�鱨���������¼�¼����ʵ�����ݺ����ģ� ��
A. ��100 mL��Ͳ��ȡ5.26 mLϡ������Һ
B. ��������ƽ��ȡ11.7 g CuO��ĩ
C. �ù㷺pH��ֽ�����Һ��pHΪ3.5
D. �¶ȼ�����ʾ�����¶���Ϊ25.68oC
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ǰ���������ʡ�������˳�����е���
A. �ռҺ̬������� B. ��ʯ�ҡ����ס���ʯ��
C. �ɱ��������Ȼ��� D. ����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���Һ������Զ�TiO2���Ⱦ��R���ⷴӦ��Ӱ����ͼ��ʾ�������ж���ȷ����
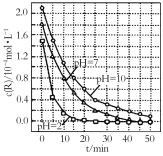
A��R����ʼŨ��ԽС����������Խ��
B����0��50 min֮�䣬pH��2��pH��7ʱR�Ľ���ٷ������
C����Һ����Խǿ��R�Ľ�������ԽС
D����20��25 min֮�䣬pH��10ʱR��ƽ����������Ϊ0.04 mol��L��1��min��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������������Ļ�ѧ��Ӧ�У����ڷ�Ӧ���������ͬ���õ���ͬ�������
������ϡ���� ������ͭ��Һ�백ˮ ��̼������Һ��ϡ���� ����������
A. �٢ڢ� B. �٢ڢۢ� C. �ڢ� D. �ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������ȤС���H2O2�ķֽ�������������ʵ��̽����
��1���±��Ǹ�С���о�Ӱ�����������H2O2���ֽ����ʵ�����ʱ�ɼ���һ�����ݣ�
��10 mL H2O2��ȡ150 mL O2�����ʱ��
Ũ�� ʱ�������� ��Ӧ���� | 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
������������������ | ���� ����Ӧ | ���� ����Ӧ | ���� ����Ӧ | ���� ����Ӧ |
���������������� | 360 | 480 | 540 | 720 |
������MnO2���������� | 10 | 25 | 60 | 120 |
��С������Ʒ���ʱ��������Ũ�ȡ�a��___________b��___________�����ضԹ�������ֽ����ʵ�Ӱ�졣
��������Ӱ��H2O2�ֽ����ʵ�����a��b����ѡһ����˵�������ضԸ÷�Ӧ���ʵ�Ӱ�죺_____________��
��2����������ͬ��������С��ͬ��MnO2�ֱ���뵽5 mL 5%��˫��ˮ�У����ô����ǵ�ľ�����ԡ��ⶨ������£�
���� ��MnO2�� | ������� | �۲��� | ��Ӧ��������ʱ�� |
��ĩ״ | ��ϲ��� | ���ҷ�Ӧ�������ǵ�ľ����ȼ | 3.5���� |
��״ | ��Ӧ���������Ǻ�����ľ��δ��ȼ | 30���� |
��д��H2O2������Ӧ�Ļ�ѧ����ʽ��______________________��
��ʵ����˵���������õĴ�С��________________�йء�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com