
【题目】一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示。下列判断正确的是
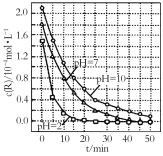
A.R的起始浓度越小,降解速率越大
B.在0~50 min之间,pH=2和pH=7时R的降解百分率相等
C.溶液酸性越强,R的降解速率越小
D.在20~25 min之间,pH=10时R的平均降解速率为0.04 mol·L-1·min-1
科目:高中化学 来源: 题型:
【题目】将下图所示实验装置的 K 闭合,下列判断正确的是
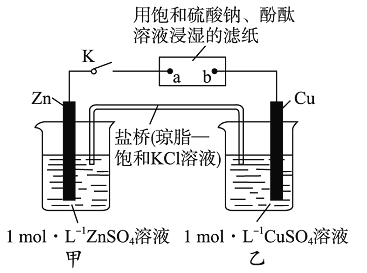
A.Cu电极上发生还原反应 B.电子沿 Zn→a→b→Cu路径流动
C.片刻后甲池中c(SO![]() )增大 D.片刻后可观察到滤纸b点变红色
)增大 D.片刻后可观察到滤纸b点变红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方案不能达到实验目的的是
A. 用碘水鉴别淀粉溶液和食盐水
B. 用澄清石灰水鉴别Na2CO3和NaHCO3溶液
C. 用丁达尔效应鉴别FeCl3溶液和Fe(OH)3胶体
D. 除去Cl2中HCl,将混合气体依次通过饱和食盐水和浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前我国的火力发电机组绝大多数为燃煤机组,而以燃煤为主的电力生产所造成的环境污染是制约电力工业发展的一个重要因素,其中氮氧化物(NOx)是继粉尘和二氧化硫之后燃煤电站环保治理的重点。
(1)燃煤烟气脱硫的方法很多,如石灰石—石膏法、氨水法等。其中石灰石-石膏法脱硫的原理第一步是SO2+Ca(OH)2![]() CaSO3+H2O,然后再将产物氧化制成石膏,写出该反应的化学方程式: 。
CaSO3+H2O,然后再将产物氧化制成石膏,写出该反应的化学方程式: 。
(2)燃煤烟气脱硝可采用氨(NH3)作为还原介质,在催化剂及氧气存在的条件下,氮氧化物(NOx)与还原剂发生反应,生成无害的氮气和水,写出二氧化氮与氨反应的化学方程式: 。
(3)我国的环境空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:
浓度限值(mg·m-3) | ||
一级标准 | 二级标准 | 三级标准 |
0.15 | 0.50 | 0.70 |
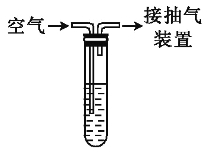
现有某化学兴趣小组按图所示的实验装置对某地空气中二氧化硫含量进行测定:向试管中加入1.00 mL 1.00×10-3 mol·L-1碘水,加入适量水,再加入2~3滴淀粉溶液使溶液显蓝色,通过抽气装置缓慢抽气,使空气由导气管进入试管与碘水充分反应,当溶液由蓝色变为无色时,恰好完全反应(反应的化学方程式:SO2+I2+2H2O![]() H2SO4+2HI),实验过程中进入试管内的空气的总体积为0.1 m3。请计算此空气中二氧化硫的浓度为多少mg·m-3,并判断二氧化硫的浓度级别为几级。
H2SO4+2HI),实验过程中进入试管内的空气的总体积为0.1 m3。请计算此空气中二氧化硫的浓度为多少mg·m-3,并判断二氧化硫的浓度级别为几级。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】选修3——物质结构与性质
已知X、Y、Z、R、Q为周期表中原子序数依次增大的前36号元素,相关信息如下:
X元素是宇宙中最丰富的元素 |
Y元素基态原子的核外p电子数比s电子数少1 |
Z元素被誉为“太空金属”,也有“生物金属”之称,其基态原子次外层有2个未成对电子 |
R元素在元素周期表的第十一列 |
Q元素在周期表里与R元素在同一个分区 |
请回答下列问题:
(1)YX3中心原子的杂化轨道类型是 ,离子化合物YX5的电子式是 。
(2)CO与Y2属于等电子体,1 个CO分子中含有的π键数目是 个。
(3)工业上利用ZO2和碳酸钡在熔融状态下制取化合物A(A可看做一种含氧酸盐),A晶体的晶胞为正方体(如图1)。
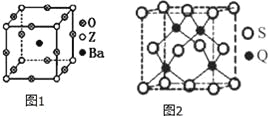
①制备A的化学反应方程式是 ;
②在A晶体中,Z的配位数为 ;
(4)R2+离子的外围电子层电子排布式为 。R2O的熔点比R2S的 (填“高”或“低”)。
(5)Q元素和硫(S)元素能够形成化合物B,B晶体的晶胞为正方体(如图2),若晶胞棱长为5.4×10-8cm,则晶胞密度为 gcm﹣3(列式并计算)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产硫酸过程中,SO2在接触室中被催化氧化为SO3,已知该反应为放热反应。现将2 mol SO2 、1 mol O2充入一密闭容器充分反应后,放出热量98.3 kJ,此时测得SO2的转化率为50%。下列热化学方程式正确的是
A.2SO3(g)![]() 2SO2(g)+O2(g);△H =+196.6 kJ/mol
2SO2(g)+O2(g);△H =+196.6 kJ/mol
B.2SO2(g)+O2(g)![]() SO3(g);△H =-98.3 kJ/mol
SO3(g);△H =-98.3 kJ/mol
C.SO2(g)+1/2O2(g)![]() SO3(g);△H=+98.3 kJ/mol
SO3(g);△H=+98.3 kJ/mol
D.SO2(g)+1/2O2(g)![]() SO3(g);△H=-196.6 kJ/mol
SO3(g);△H=-196.6 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为一种盐,C、D、F、N、O为无色气体,E常温常压下为无色无味的液体,N、H、L为高中常见的单质,I为常见无氧强酸,M的焰色反应为紫色,反应①常用于气体F的检验。
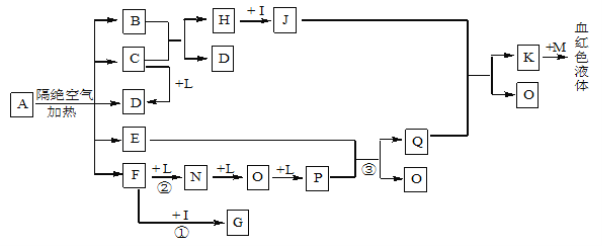
(1)写出D的电子式为_______________;
(2)写出反应①的化学方程式: ;写出反应②的化学方程式: ;反应③中氧化剂和还原剂的物质的量之比为_________________;
(3)将等体积、等浓度的G和F的溶液混合,溶液显碱性,则溶液中离子浓度从大到小的顺序为 ______________________;
(4)检验J中阳离子的实验方法为 ;
(5)已知B中氧元素的质量分数为22.2﹪,且A分解产生的各物质的物质的量之比为n(B):n(C): n(D):n(E):n(F)=1:2:2:1:2,则A的化学式为_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中盛有H2和Cl2混合气体体积为n L,用电火花引燃后,恢复到原来状态,气体体积不变。把气体通入足量的NaOH溶液,气体没有剩余,则原混合气体中H2与Cl2的物质的量比为( ):
A.≥1 B.≤1 C.=1 D.<1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一瓶Na2SO3溶液,由于可能已部分氧化,某学生进行如下实验:取少量溶液,滴入Ba(NO3)2溶液产生白色沉淀,再加入过量稀硝酸,充分振荡后仍有白色沉淀,结论正确的是
A. Na2SO3溶液已部分氧化
B. 加入Ba(NO3)2溶液后生成的沉淀中一定含有BaSO4
C. 加硝酸后的不溶沉淀一定为BaSO4
D. 此实验能确定Na2SO3溶液是否部分氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com