
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:

(1)该浓盐酸中HCl的物质的量浓度为__________mol·L-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_____。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液的密度 D.溶液中Cl-的数目
(3)下列容量瓶的使用方法中,不正确的是____________
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(4)某学生欲用上述浓盐酸和蒸馏水配制480mL物质的量浓度为0.200 mol·L-1的稀盐酸。
①该学生需要用量筒量取________mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作会使所配制的稀盐酸的物质的量浓度偏大的有_____
A.转移溶液后未洗涤烧杯和玻璃棒就直接定容。
B.用量筒量取浓盐酸时俯视观察凹液面。
C.在容量瓶中定容时俯视刻度线。
D.定容后把容量瓶倒置摇匀,发现液面低于刻度线,又加水至刻度线。
【答案】11.9BCBCD8.4C
【解析】本题分析:本题主要考查物质的量浓度以及配制一定物质的量浓度的溶液,涉及到物质的量浓度与质量分数之间的换算、容量瓶的使用、溶液的配制等。
(1)![]() ;
;
(2)A项:![]() 可知,溶液中HCl的物质的量随溶液的体积变化而变化,错误;B项:从一定物质的量浓度的盐酸溶液中取用任意体积的该盐酸溶液,其溶液的浓度不变,正确;C项:盐酸溶液是均一稳定的分散系,任何体积的密度不变,正确;D项:
可知,溶液中HCl的物质的量随溶液的体积变化而变化,错误;B项:从一定物质的量浓度的盐酸溶液中取用任意体积的该盐酸溶液,其溶液的浓度不变,正确;C项:盐酸溶液是均一稳定的分散系,任何体积的密度不变,正确;D项:![]() ,体积不同时,溶液中离子的数目也不同,错误。
,体积不同时,溶液中离子的数目也不同,错误。
(3)A项:容量瓶在使用之前需要检查是否漏水,正确;B项:容量瓶用水洗净后,不需要再用待配溶液洗涤,错误;C项:容量瓶用于精确配制一定物质的量浓度的溶液,不能用于溶解固体。若试样为固体,应在烧杯溶解后再转移到容量瓶中,错误;D项:试样为液体时,用量筒取样后倒入烧杯中稀释,冷却后再用玻璃棒引流转入容量瓶中,错误;E项:摇匀操作为:盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀,正确;
(4)①配制480mL溶液应该选取500mL容量瓶,故![]() ;②根据
;②根据![]() ,A项:转移溶液后未洗涤烧杯和玻璃棒,导致
,A项:转移溶液后未洗涤烧杯和玻璃棒,导致![]() 减小,
减小,![]() 偏小,错误;B项:用量筒量取8.4mL浓盐酸时俯视观察凹液面,
偏小,错误;B项:用量筒量取8.4mL浓盐酸时俯视观察凹液面,![]() 偏小,
偏小,![]() ,
,![]() 偏小,错误;C项:定容时俯视刻度线,
偏小,错误;C项:定容时俯视刻度线,![]() 偏小,
偏小,![]() 偏大,正确;D项:定容后把容量瓶倒置摇匀,发现液面低于刻度线,又加水至刻度线,
偏大,正确;D项:定容后把容量瓶倒置摇匀,发现液面低于刻度线,又加水至刻度线,![]() 偏大,
偏大,![]() 偏小,错误。
偏小,错误。


科目:高中化学 来源: 题型:
【题目】周期表中前20号几种元素,其相关信息如下(铍的原子半径为0.089nm);F原子中无中子,G在地壳中含量居第二位,H元素焰色反应呈紫色。根据题意请回答下列问题:
元素代号 | A | B | C | D | E |
原子半径/nm | 0.075 | 0.143 | 0.102 | 0.099 | 0.074 |
主要化合价 | +5,—3 | +3 | +6,—2 | —1 | —2 |
(1)B的原子结构示意图为___________。
(2)F2C和F2E两种化合物中,沸点较高的是____(填化学式)。
(3)用电子式表示化合物H2E的形成过程_______________________________。
(4)某同学设计了以G同族的短周期元素的最低价氢化物为燃料的电池,电解质为KOH。 则该电池的负极的电极反应式为__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:NaH+H2O=H2+NaOH,对该反应的判断正确的是( )
A.1mol NaH参加反应失去1mol电子
B.每生成1mol H2转移2mol电子
C.NaH既是氧化剂,又是还原剂
D.NaOH是氧化产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合乙烯和乙醇的结构与性质,推测丙烯醇(CH2=CH—CH2OH)不能发生的化学反应( )
A.加成反应
B.氧化反应
C.与Na反应
D.与Na2CO3溶液反应放出CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释下列事实
A. 苯不能因发生化学反应而使溴水褪色 B. 苯能与H2发生加成反应
C. 溴苯没有同分异构体 D. 间二溴苯只有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:① A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平 ② ![]() 。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
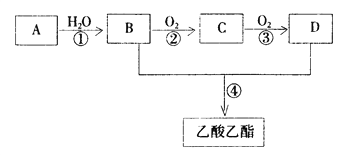
回答下列问题:
(1)B、D分子中的官能团名称分别是 __________、___________。
(2)写出下列反应的反应类型:①__________,②__________,④________。
(3)写出下列反应的化学方程式:
②____________________________;④_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KIO3是一种无色易溶于水的晶体,医药上可作防治地方甲状腺肿的药剂,目前碘酸钾被广泛应用于食盐加碘。一种由含碘废水制取碘酸钾的工艺如下:

(1) 检验“含碘废水”中含有的单质I2,常用的试剂是________。
(2) 进行“过滤1”时,需同时对CuI沉淀进行洗涤。在洗涤过滤滤液中可通过滴加________盐溶液来检验其是否已洗涤干净。
(3) “滤渣2”的成分为____________(填化学式)。
(4) “制KI”时,发生反应的化学方程式为____________。
(5) 江苏食用加碘盐新标准是每千克食盐中碘元素含量为25毫克(波动范围为18~33 mg/kg)。测定食盐试样中碘元素含量的步骤如下:称取4.000 g市售食盐加入锥形瓶中,依次加入适量的水、稍过量KI及稀硫酸;充分反应后,再加入12.00 mL 6.000×10-4 mol·L-1 Na2S2O3溶液,与生成的碘恰好完全反应。有关反应原理为:
KIO3+5KI+3H2SO4===3K2SO4+3I2+3H2O; I2+2S2O![]() ===2I-+S4O
===2I-+S4O![]() 。
。
①计算该食盐试样中碘元素的含量(单位mg/kg,写出计算过程)。
_______
②该食盐试样是否符合江苏食用加碘盐新标准并说明判断依据。
_______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com