
甲醇可以与水蒸气反应生成氢气,反应方程式如下:
CH3OH(g)+H2O(g)  CO2(g)+3H2(g) ΔH>0
CO2(g)+3H2(g) ΔH>0
(1)一定条件下,向体积为2 L的恒容密闭容器中充入1 mol CH3OH(g)和3 mol H2O(g),20 s后,测得混合气体的压强是反应前的1.2倍,则用甲醇表示该反应的速率为________。
(2)判断(1)中可逆反应达到平衡状态的依据是(填序号)________。
①v正(CH3OH)=v正(CO2)
②混合气体的密度不变
③混合气体的平均相对分子质量不变
④CH3OH、H2O、CO2、H2的浓度都不再发生变化
(3)下图中P是可自由平行滑动的活塞,关闭K,在相同温度时,向A容器中充入1 mol CH3OH(g)和2 mol H2O(g),向B容器中充入1.2 mol CH3OH(g)和2.4 mol H2O(g),两容器分别发生上述反应。已知起始时容器A和B的体积均为a L。试回答:
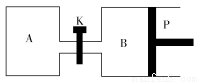
①反应达到平衡时容器B的体积为1.5aL,容器B中CH3OH转化率为________,A、B两容器中H2O(g)的体积百分含量的大小关系为:B(填“>”“<”或“=”)________A。
②若打开K,一段时间后重新达到平衡,容器B的体积为________L(连通管中气体体积忽略不计,且不考虑温度的影响)。
(1)0.01 mol/(L·s)
(2)③④ (3)75% < 1.75a
【解析】本题主要考查化学反应速率、化学平衡的判断及有关等效平衡的计算,属于中等难度的题。
(1)反应前气体的总物质的量为4mol,反应后气体的总物质的量为4 mol×1.2=4.8 mol。
CH3OH(g)+H2O(g)  CO2(g)+3H2(g) △n
CO2(g)+3H2(g) △n
1 mol 1 mol 1 mol 3 mol 2 mol
0.4 mol (4.8-4)mol
则v(CH3OH)=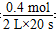 =0.01 mol/(L·s)。
=0.01 mol/(L·s)。
(2)①中两种物质的速率表示的是同一方向的反应速率,不能作为反应达到平衡的依据。②由于混合气体的质量和体积都不变,故其密度始终不变,不能说明反应是否达平衡。③中混合气体的平均相对分子质量不变,说明混合气体的总物质的量不变,即反应正向进行和逆向进行的趋势相同,故可作为反应达到平衡的依据。④中各气体的物质的量浓度不变,说明反应已达到平衡。故应选③④。
(3)反应达平衡时,B中气体的总物质的量为: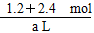 ×1.5 a L=5.4 mol,气体的总物质的量比反应前增加5.4 mol-1.2 mol-2.4 mol=1. 8 mol。
×1.5 a L=5.4 mol,气体的总物质的量比反应前增加5.4 mol-1.2 mol-2.4 mol=1. 8 mol。
CH3OH(g)+H2O(g)  CO2(g)+3H2(g) △n
CO2(g)+3H2(g) △n
1 mol 1 mol 1 mol 3 mol 2 mol
0.9 mol1.8 mol
故B中CH3OH的转化率为: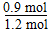 ×100%=75%。
×100%=75%。
若A、B两容器中的压强相等,两容器中的气体达平衡时,为等温等压下的等效平衡,两容器中H2O(g)的百分含量相等。现在A容器的体积不变,而反应后气体的总物质的量增加,即压强增大,平衡应逆向(气体体积减小的方向)移动,H2O(g)的百分含量增加,故B中H2O(g)的百分含量小于A中H2O(g)的百分含量。(2)若打开K,则A中气体的压强与B中相同,两容器中的气体达平衡时,为等温等压下的等效平衡,这时原A中气体的体积将变为: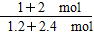 ×1.5 a L=1.25 a L,气体体积增加0.25 a L,故这时容器B的体积变为:1.5 a L+0.25 a L=1.75 a L。
×1.5 a L=1.25 a L,气体体积增加0.25 a L,故这时容器B的体积变为:1.5 a L+0.25 a L=1.75 a L。


科目:高中化学 来源:2015届北京市怀柔区高二上学期期末质量检测化学试卷(解析版) 题型:推断题
从丁烷出发可合成一种香料A,其合成路线如下:
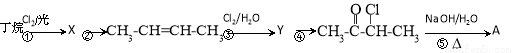
已知CH2=CH2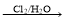 ClCH2—CH2—OH
ClCH2—CH2—OH
(1)丁烷的最简式为 反应②的条件为 。
(2)X的结构简式为 ;Y的结构简式为 。
(3)上述反应①②③④中,未涉及的反应类型是 。(填序号)
a.氧化反应;b.还原反应;c.聚合反应;d.取代反应;e.消去反应
(4)反应⑤的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题9有机化合物的获取与应用练习卷(解析版) 题型:选择题
下列各组中的反应属于同一反应类型的是( )
A.由溴丙烷水解制丙醇;由丙烯与水反应制丙醇
B.由苯硝化制硝基苯;由苯与氢气反应制环己烷
C.由乙酸和乙醇制乙酸乙酯;由甲酸乙酯水解制甲酸和乙醇
D.由氯代环己烷消去制环己烯;由丙烯与溴反应制1 ,2?二溴丙烷
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题8溶液中的离子反应练习卷(解析版) 题型:选择题
下图是向100 mL的盐酸中逐渐加入NaOH溶液时,溶液的pH变化图像,根据如图所得结论正确的是( )
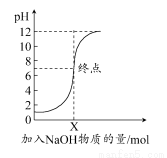
A.原来盐酸的物质的量浓度为0.1 mol·L-1
B.NaOH溶液的浓度为0.1 mol·L-1
C.原来盐酸的物质的量浓度为1 mol·L-1
D.NaOH溶液的浓度为0.01 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题8溶液中的离子反应练习卷(解析版) 题型:选择题
下列电离方程式的书写正确的是( )
A.NH4++H2O NH3·H2O+H+
NH3·H2O+H+
B.S2-+2H2O H2S+2OH-
H2S+2OH-
C.CH3COOH+H2O CH3COO-+H3O+
CH3COO-+H3O+
D.CH3COOH+OH- CH3COO-+H2O
CH3COO-+H2O
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题7化学反应速率与化学平衡练习卷(解析版) 题型:选择题
将一定量的氨基甲酸铵固体置于某容积恒定的真空容器中,发生反应:H2NCOONH4(s)  2NH3(g)+CO2(g),在不同温度下,该反应平衡状态时的部分数据见下表。下列说法正确的是( )
2NH3(g)+CO2(g),在不同温度下,该反应平衡状态时的部分数据见下表。下列说法正确的是( )
温度 | 平衡浓度/(mol·L-1) | |
c(NH3) | c(CO2) | |
T1 | 0.1 |
|
T2 |
| 0.1 |
A.若T2>T1,则该反应的ΔH<0
B.向容器中充入N2,H2NCOONH4质量增加
C.NH3体积分数不变时,说明该反应达到平衡
D.T1、T2时,H2NCOONH4转化的Δn(T2)=2Δn(T1)
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题7化学反应速率与化学平衡练习卷(解析版) 题型:选择题
往一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)  2HI(g) ΔH<0,当达到平衡后,t0时若保持混合气体总物质的量不变而改变某一反应条件,使容器内压强增大(如图所示),下列说法正确的是( )
2HI(g) ΔH<0,当达到平衡后,t0时若保持混合气体总物质的量不变而改变某一反应条件,使容器内压强增大(如图所示),下列说法正确的是( )
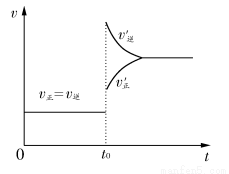
A.容器内气体颜色变深,平均相对分子质量不变
B.平衡不移动,混合气体密度不变
C.H2转化率增大,HI平衡浓度减小
D.t0时改变的条件是减小体积或升高体系温度
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题6化学反应与能量变化练习卷(解析版) 题型:选择题
某些化学键键能数据如下:
化学键 | H—H | Cl—Cl | H—Cl |
键能/ kJ·mol-1 | 436 | 243 | 431 |
则下列热化学方程式不正确的是( )
A. 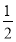 H2(g)+
H2(g)+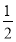 Cl2(g)=HCl(g) ΔH=-91.5 kJ·mol-1
Cl2(g)=HCl(g) ΔH=-91.5 kJ·mol-1
B.H2(g)+Cl2(g)=2HCl(g)ΔH=-183 kJ·mol-1
C. 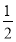 H2(g)+
H2(g)+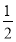 Cl2(g)=HCl(g)ΔH=+91.5 kJ·mol-1
Cl2(g)=HCl(g)ΔH=+91.5 kJ·mol-1
D.2HCl(g)=H2(g)+Cl2(g)ΔH=+183 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题3从矿物到基础材料练习卷(解析版) 题型:选择题
下列各组物质中,不是按下图所示(“→”表示一步完成)关系相互转化的是( )
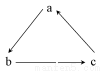
选项abc
AFeFeCl3FeCl2
BCl2NaClONaCl
CSiSiO2H2SiO3
DHNO3NONO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com