
【题目】FeBr2是一种黄绿色固体,某学习小组制备并探究它的还原性
Ⅰ.实验室制备FeBr2
实验室用下图所示装置制取溴化亚铁.其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管.e是两只耐高温的瓷皿,其中盛有细铁粉.
实验开始时先将铁粉加热至600℃~700℃,然后将干燥、纯净的CO2气流通入D中,E管中反应开始,不断将d中液溴滴入100℃~120℃的D中,经过几小时的连续反应,在铁管的一端沉积有黄绿色鳞片状溴化亚铁
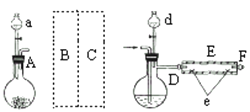
请回答:
(1)如何检查用塞子(插有导管和仪器)塞紧的D的气密性________.
(2)若在A中盛固体CaCO3,a中盛6mol/L盐酸,为使导入D中的CO2为干燥纯净的气体,则图中B、C处的装置和其中的试剂应是:B为________,C为________.为防止污染空气,实验时应在F处连接盛________的尾气吸收装置
(3)反应过程中要不断通入CO2,其主要作用是①________,②________.
Ⅱ.探究FeBr2的还原性,
(1)实验需要90 mL 0.1 mol·L-1FeBr2溶液,配制FeBr2溶液除烧杯、量筒、胶头滴管、玻璃棒外还需的玻璃仪器是________。
(2)取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br-被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+被Cl2氧化成Fe3+。
设计实验证明假设2是正确的_______________________________
(3)实验证明:还原性Fe2+>Br-请用一个离子方程式来证明:______________________________;
(4)若在40mL上述FeBr2溶液中通入3×10-3molCl2,则反应的离子方程式为:_____。
【答案】 关闭d的活塞,夹紧C~D之间的胶管,将下出口导管插入水中,然后将D用手捂热,若下导管出口有气泡冒出,松开手后水回升到导管中,则证明D装置不漏气 NaHCO3溶液的洗气瓶 浓H2SO4的洗气瓶 NaOH溶液 用CO2把反应器中空气赶尽 将Br2蒸气带入反应管中 100 mL容量瓶 向黄色溶液中加入少量KSCN溶液,若溶液变血红色,则证明假设2正确 2Fe2++Br2=2Fe3++2Br- 4Fe2++2Br-+3Cl2 = 4Fe3++ Br2+2Cl-
【解析】试题分析:Ⅰ.(1)由于装置D中含有进气口和分液漏斗,所以检验装置D的操作是:关闭d的活塞,夹紧C~D之间的胶管,将下出口导管插入水中,然后将D用手捂热,若下导管出口有气泡冒出,松开手后水回升到导管中,则证明D装置不漏气。
(2)浓盐酸易挥发,生成的CO2气体中含有水蒸气和氯化氢,因此要得到干燥纯净的水蒸气可以依次通过盛有饱和碳酸氢钠溶液和浓硫酸的洗气瓶;溴蒸汽有毒,为了防止污染空气,实验时应在F处连接盛氢氧化钠溶液的尾气吸收装置。
(3)由于装置含有空气,空气中的氧气能氧化金属铁,另外为了使溴蒸汽能与铁充分接触反应,依次CO2的主要作用是用CO2把反应器中空气赶尽,同时将Br2蒸气带入反应管中。
Ⅱ.(1)配制FeBr2溶液时需要天平、钥匙、烧杯、玻璃棒、100mL的容量瓶,胶头滴管,则除烧杯、量筒、胶头滴管外还需的玻璃仪器是100mL的容量瓶;
(2)由于铁离子能与KSCN溶液反应使溶液显红色,因此证明假设2成立的是向黄色溶液中加入少量KSCN溶液,若溶液变血红色,则证明假设2正确;
(3)由还原性Fe2+>Br-,则氯化亚铁溶液中加入1~2滴溴水发生氧化还原反应生成Fe3+,反应为的离子方程式Fe2++Br2=2Fe3++2Br-;
(3)溴化亚铁的物质的量是0.004mol,氯气是0.003ml,由于还原性Fe2+>Br-,二者以4:3反应,由电子守恒可知,亚铁离子全部被氧化,溴离子有0.002mol被氧化,因此反应的离子反应方程式为4Fe2++2Br-+3Cl2=4Fe3++Br2+2Cl-。


科目:高中化学 来源: 题型:
【题目】由2-氯丙烷制取少量的1,2-丙二醇时,需要经过下列哪几步反应( )
A.消除、加成、取代B.加成、消除、取代
C.取代、消除、加成D.消除、加成、消除
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() U是重要的核工业原料,它的浓缩一直被国际社会关注,有关
U是重要的核工业原料,它的浓缩一直被国际社会关注,有关 ![]() U说法正确的是( )
U说法正确的是( )
A.![]() U原子核中含有92个中子
U原子核中含有92个中子
B.![]() U原子核外有143个电子
U原子核外有143个电子
C.![]() 和
和 ![]() U互为同位素
U互为同位素
D.![]() U和
U和 ![]() U为同一核素
U为同一核素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温州某学生用0.1000mol/LNaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:

A.检查滴定管是否漏水
B.用蒸馏水洗干净滴定管
C.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管“0”刻度以上2~3cm处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下
D.用待测定的溶液润洗酸式滴定管
E.用酸式滴定管取稀盐酸20.00mL,注入锥形瓶中,加入酚酞
F.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
G.另取锥形瓶,再重复操作一次
完成以下填空:
(1)操作F中应该选择图中 ______ 滴定管(填标号)。
(2)滴定时边滴边摇动锥形瓶,眼睛应观察 ______。
A.滴定管内液面的变化B.锥形瓶内溶液颜色的变化
滴定终点溶液颜色的变化是 ______ .若指示剂改为甲基橙则颜色的变化是 ______。
(3)滴定结果如表所示:
滴定次数 | 待测液体积/mL | 标准溶液的体积/mL | ||
滴定前刻度 | 滴定后刻度 | |||
1 | 20 | 1.02 | 21.03 | |
2 | 20 | 2.00 | 25.00 | |
3 | 20 | 0.60 | 20.59 | |
滴定中误差较大的是第 ______ 次实验,造成这种误差的可能原因是 ______。
A.碱式滴定管在装液前未用标准NaOH溶液润洗2~3次
B.滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C.滴定开始前碱式滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
D.达到滴定终点时,仰视溶液凹液面最低点读数
E.滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
(4)该盐酸的浓度为______mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质,能互称为同系物的一组是( )
A. O2和O3 B. H2C=CH2和CH3CH2CH=CH2
C. CH3CH2CH=CH2和CH3CH=CHCH3 D. 丁烷和异丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用海水制盐工业中的母液来生产金属镁的一种工艺流程如下:
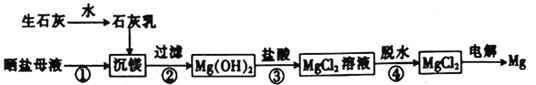
下列说法错误的是
A. 上述工艺流程中未涉及置换反应
B. 设计步骤①、②、③的主要目的是富集MgCl2
C. 脱水时在HC1气氛中进行可防止MgCl2发生水解
D. 电解得到的炽热镁粉可在二氧化碳气氛中冷却
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在探究酶的活性实验中,某同学将pH值分别为1、7、10的等量唾液淀粉酶滴入编号为甲、乙、丙的等量淀粉溶液的三支试管中,立即将3支试管置于85℃水浴中,10min后分别加入碘液,能出现蓝色的试管是( )
A. 甲试管 B. 乙试管
C. 乙和丙试管 D. 甲、乙、丙三支试管
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com