
(1)铬的外围电子排布式是 ,与铬同周期,最外层有3个未成对电子数的主族元素名称是 ,该元素对应的最低价氢化物分子的中心原子采取了 杂化方式,分子的空间构型是 。
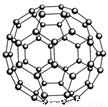
(2)富勒烯(C60)的结构如图,1molC60分子中σ键的数目为______ 。继C60后,科学家又合成了Si60、N60。请解释如下现象:熔点:Si60>N60>C60,而破坏分子所需要的能量: N60>C60>Si60,其原因是: 。
(3)氟化氢水溶液中存在氢键有 种。
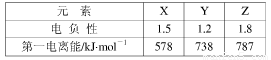
(4)2011年诺贝尔化学奖授予了因发现准晶体材料的以色列科学家。某准晶体是锰与另一个短周期元素X形成的凝固态。已知:金属的电负性一般小于1.8。元素X与同周期相邻元素Y、Z的性质如下表:则X元素符号是 ,锰与X在准晶体中的结合力为 。
(1)3d54s1 砷 sp3 三角锥 (各1分,共4分)
(2)90NA (2分) 组成、结构相似的分子晶体,相对分子质量越大,分子间作用力(或范德华力)越强,熔化所需的能量越多,故熔点:Si60>N60>C60(1分);而破坏分子所需断开化学键,元素电负性越强其所形成的化学键越稳定,或成键电子数越多,成键原子半径越小,断键所需能量越多,故破坏分析需要的能量顺序为N60>C60>Si60(1分)(合理答案均可,各1分,共2分)
(3) 4 (2分)
(4)Al (2分) 金属键 (1分)
【解析】
试题分析:(1)根据能量最低原理、洪特规则等规律,基态Cr原子外围电子排布式为3d54s1;价电子排布式为4s24p3的As符合要求,即砷;PH3中P采取sp3杂化方式,孤对电子与成键电子对形成正四面体形,则PH3分子为三角锥形;(2)读图可知,每个碳原子周围形成3个C—C键,每个C—C键被相邻2个碳原子共用,则1个碳原子可形成1.5个σ键,60个碳原子可形成90个σ键,1molC60分子含有90NA个σ键;组成、结构相似的分子晶体,相对分子质量越大,分子间作用力(或范德华力)越强,熔化所需的能量越多,故熔点:Si60>N60>C60;破坏分子所需断开化学键,元素电负性越强其所形成的化学键越稳定,或成键电子数越多,成键原子半径越小,断键所需能量越多,故破坏分析需要的能量顺序为N60>C60>Si60;(3)氟化氢水溶液中存在的氢键有F—H……F、F—H……O、O—H……F、O—H……O四种类型;(4)由表中信息可知X是铝,锰与铝以金属键结合。
考点:考查外围电子排布式、元素推断、杂化类型、分子构型、σ键、物质的熔点、化学键、氢键、金属键等相关知识。


科目:高中化学 来源: 题型:
| 1-x |
| x |
| 1-x |
| x |
查看答案和解析>>
科目:高中化学 来源: 题型:
 氧气是化工生产的重要原料,很多金属和非金属都能和氧气直接作用.
氧气是化工生产的重要原料,很多金属和非金属都能和氧气直接作用.| 氧化物 | MgO | CaO | SrO | BaO |
| 晶格能/kJ?mol-1 | 3791 | 3410 | 3223 | 3054 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com