
【题目】右图是温度和压强对反应:X+Y ![]() 2Z 影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
2Z 影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
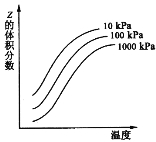
A.上述可逆反应的正反应为放热反应
B.X、Y、Z均为气态
C.X和Y只有一种为气态,Z为气态
D.上述反应的逆反应的△H>0
 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
【题目】MnO2用途很广,它是一种广泛应用的氧化剂。例如将它加入熔态的玻璃中,可以除去带色的杂质(硫化物或亚铁盐),称为普通玻璃的“漂白剂”。在锰-锌干电池中用作去极剂,以氧化在电极上产生的氢。
(1)Zn- MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。其电解质溶液呈________性(填“酸”、“碱”或“中”),原因是_________________、________________(用离子方程式表示);该电池工作时,电子流向__________极(填“正”或 “负”)。
(2)工业上,常以菱锰矿(主要成分MnCO3,常含有少量铁、钙、锌等元素)为原料,用电解法可以制备MnO2。其制备过程如下:

写出酸浸的主要化学方程式:______________________。
②下图可以看出,从MnSO4和ZnSO4混合溶液中结晶MnSO4·H2O晶体,需要控制的温度范围为______________(填字母)。
A.0~40℃ B.40~60℃ C.60℃以上
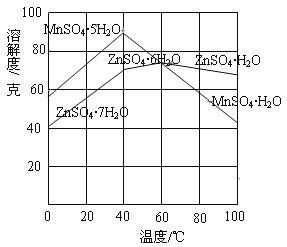
③请写出用惰性电极电解MnSO4溶液制备MnO2的阳极反应:___________________。
④该工艺产生的废水中含有较多的Mn2+,通常用H2S或者Na2S溶液处理。25 ℃,在0.10 mol·L-1 H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图(忽略溶液体积的变化、H2S的挥发)。
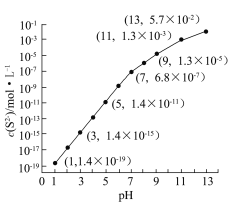
i.pH=13时,溶液中的c(H2S)+c(HS-)=__________mol·L-1;
ii.某溶液含x mol·L-1 Mn2+、0.10 mol·L-1 H2S,当调节溶液pH=5时,Mn2+开始沉淀,则x= 。[已知:Ksp(MnS)=2.8×10-13]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.植物油氢化过程中发生了加成反应
B.淀粉和纤维素互为同分异构体
C.环己烷与苯可用酸性KMnO4溶液鉴别
D.水可以用来分离溴苯和苯的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A.石灰石溶于稀盐酸:CaCO3+2H+=Ca2++CO2↑+H2O
B.硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓
C.氧化镁与稀硫酸:MgO+2H+=Mg2++H2O
D.常温下,将铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 目前加碘食盐中主要添加的是KIO3
B. 日常生活中和医院常用无水乙醇杀菌消毒
C. 绿色食品是指不含任何化学物质的食品
D. 在空气质量日报中CO2含量属于空气污染指数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应N2+O2![]() 2NO在恒容密闭容器中进行,达到平衡后,充入N2,下列说法正确的是
2NO在恒容密闭容器中进行,达到平衡后,充入N2,下列说法正确的是
A. 平衡向逆反应方向移动,N2和O2的转化率都减小
B. 平衡向正反应方向移动,N2和O2的转化率都增大
C. 压强增大平衡不移动,N2的转化率不变
D. 平衡向正反应方向移动,N2的转化率减小,O2的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,向体积为2L的密闭容器中加入2 mol N2和10 mol H2发生如下反应:N2+3H2![]() 2NH3,2 min时测得剩余的N2为1mol,则化学反应速率的表示不正确的是
2NH3,2 min时测得剩余的N2为1mol,则化学反应速率的表示不正确的是
A.v(N2)=0.25 mol·L-1·min-1 B.v (H2)=0.0125 mol·L-1·s-1
C.v(NH3)=1.0 mol·L-1·min-1 D.v (H2)=0.75 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁、是由H+、Na+、Al3+、Ba2+、OH—、Cl—、HCO3—离子中的两种组成,可以发生如图转化,下列说法不正确的是
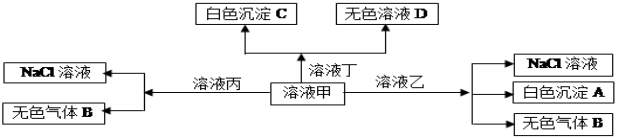
A.在丁中滴加甲开始反应的离子方程式:HCO3—+ Ba2++OH—= BaCO3↓+ H2O。
B.溶液丙中还可以大量共存的离子有:Fe2+、NO3—、SO42—
C.白色沉淀A可能溶解在溶液D中
D.甲为NaHCO3,乙为AlCl3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com