
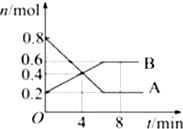
 某温度时,在0.5L密闭容器中,某一反应的A、B气体物质的量随时间变化的曲线如图所示,由图中数据分析求得:
某温度时,在0.5L密闭容器中,某一反应的A、B气体物质的量随时间变化的曲线如图所示,由图中数据分析求得: B.
B.分析 由图可知,从反应开始,A的物质的量减少,B的物质的量增加,则A为反应物、B为生成物,开始至4min时,A减少0.8mol-0.4mol=0.4mol,B增加0.4mol-0.2mol=0.2mol,结合反应速率之比等于化学计量数之比、v=$\frac{△c}{△t}$计算,且第8min时A、B的物质的量不再变化,达到平衡状态,以此来解答.
解答 解:(1)由图可知,从反应开始,A的物质的量减少,B的物质的量增加,则A为反应物、B为生成物,开始至4min时,A减少0.8mol-0.4mol=0.4mol,B增加0.4mol-0.2mol=0.2mol,由反应速率之比等于化学计量数之比可知,A、B的化学计量数比为2:1,且后来达到平衡状态,则反应为2A B,
B,
故答案为:2A B;
B;
(2)反应开始至4min时,B的平均反应速率为$\frac{\frac{0.4mol-0.2mol}{0.5L}}{4min}$=0.lmol/(L?min),
故答案为:0.lmol/(L?min);
(3)第4min时,A的物质的量仍在减少,为正反应阶段,正、逆反应速率的大小关系为:v(正)>v(逆),故答案为:>;
(4)第8min时,A、B的物质的量不再变化,达到平衡状态,则v(正)=v(逆),故答案为:=.
点评 本题考查物质的量随时间变化曲线,为高频考点,把握图象中物质的量的变化、平衡状态的判断、速率比较等为解答的关键,侧重分析与应用能力的考查,注意速率的比较,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 都属于铵盐 | B. | 都属于离子化合物 | ||
| C. | 互为同素异形体 | D. | 互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgNO3 | B. | CuSO4 | C. | K2SO3 | D. | Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙炔通入酸性高锰酸钾溶液中,溶液褪色 | |
| B. | 苯滴入溴水中,振荡后溴水层接近无色 | |
| C. | 油脂的皂化反应 | |
| D. | 将含裂化获得的汽油滴入溴水中,溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
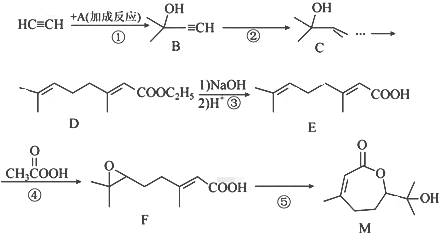
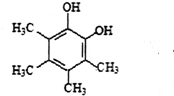
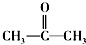 ,两分子HC≡CH与一分子A反应的产物的结构简式为
,两分子HC≡CH与一分子A反应的产物的结构简式为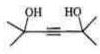 .
. .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | HClO4、H3PO4、H2SO4的酸性依次减弱 | |
| B. | HCl、HBr、HI的稳定性依次减弱 | |
| C. | N、O、F原子半径逐渐增大 | |
| D. | 钠、镁、铝的还原性依次减弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com