
有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
阳离子 | K+、Na+、Al3+、Cu2+ |
阴离子 | OH-、HCO3-、NO3-、SO42- |
为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀完全溶解;
③进行焰色反应,B、C为紫色(透过蓝色钴玻璃),A、E为黄色;
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀,B中无明显现象。
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)写出B、C的化学式:B ; C 。
(2)写出过量E滴人到C溶液中的离子反应方程式 。
(3)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为 。
(4)在A溶液中加澄清石灰水,其离子方程式为 。
(5)上述五种化合物中有一种是常用作净水剂,其净水原理是: (请结合方程式及必要的文字进行叙述)。
(1) KNO3 (2分) ; KAl(SO4)2(带结晶水也同样给分)(2分)
(2)Al3++4OH-=AlO2-+2H2O(2分)
(3)Na2CO3 (2分)
(4) HCO3-+Ca2++OH-=CaCO3↓+H2O(或2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O)(2分)
(5)Al3++3H2O=Al(OH)3(胶体)+3H+ (2分) Al(OH)3(胶体)具有很强的吸附能
力,它能凝聚水中的悬浮物并使之沉降,从而达到净水的目的。(2分)
【解析】
试题分析:①将它们溶于水后,D为蓝色溶液,说明D中含有离子Cu2+;②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解,由以上离子可以看出,应为Al3+与OH-的反应,则E中含有OH-,C中含有Al3+;③进行焰色反应, B、C为紫色(透过蓝色钴玻璃),说明B、C中含有K+;④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,则A含有HCO3-,焰色反应不呈紫色,A应为NaHCO3,C、D中产生白色沉淀该沉淀为BaSO4,说明C、D中含有SO42-;所以C为KAl(SO4)2,D为CuSO4,E焰色反应不呈紫色,只能为NaOH,⑤将B、D两溶液混合,D为CuSO4,未见沉淀或气体生成,说明二者没有发生任何反应,则B为KNO3,则
(1)B、C的化学式分别为KNO3,KAl(SO4)2,(2)铝离子与过量氢氧化钠生成偏铝酸根。
(3)将含1mol A的溶液与含1mol E的溶液反应,反应的化学方程式为NaHCO3+NaOH═Na2CO3+H2O,溶液反应后蒸干,得到的化合物为Na2CO3,故答案为:Na2CO3;
(4)在NaHCO3溶液中加少入量澄清石灰水,其离子方程式为2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+H2O,
(5)Al2(SO4)2常作净水剂,原因是Al3+离子水解生成具有较强吸附性的Al(OH)3胶体,反应的离子方程式为Al3++3H2O  Al(OH)3+3H+,
Al(OH)3+3H+,
考点:考查元素化合物知识、离子反应、盐类水解等知识。


科目:高中化学 来源:2016届浙江省杭州市高一上学期期末模拟考试化学试卷(解析版) 题型:选择题
NaCl的晶胞如图所示,将NaCl晶胞中的所有Cl-去掉,并将Na+全部换成C原子,再在晶胞的4个“小立方体”中心处各放置一个C原子,且这四个“小立方体”互不共面,位于“小立方体”中的碳原子均与最近的4个碳原子成键,以此表示金刚石的一个晶胞。若再将在成键的C原子中心联线的中点处增添一个O原子,则构成了某种CO2的晶胞。则下面说法正确的是( )(已知C-C键的键长1.54×10-10m)

A.一个金刚石的晶胞中有8个C原子
B.金刚石的密度为3.54g·cm-1
C.在该种CO2晶体中,一个CO2分子由一个C原子和二个氧原子构成
D.在该种CO2晶胞中含氧原子8个
查看答案和解析>>
科目:高中化学 来源:2016届浙江省宁波市高一上学期期末考试化学试卷(解析版) 题型:填空题
已知少量碳酸钠与足量盐酸反应,有二氧化碳气体放出;而少量盐酸与过量碳酸钠反应,则生成碳酸氢钠和氯化钠,无气体放出。现有A、B两瓶无色溶液,其中一瓶是稀盐酸,另一瓶是碳酸钠溶液。为测定两瓶溶液的成分及物质的量浓度,进行以下实验:
①取20mLA溶液,向其中缓慢滴入B溶液25mL,共收集到112mL(标准状况)气体。
②取25mLB溶液,向其中缓慢滴入A溶液20mL,共收集到56mL(标准状况)气体。
(1)写出少量盐酸与过量碳酸钠反应,无气体放出的离子方程式 ;
(2)为使上述①②反应完全,还需加入 ;(填“稀盐酸”或“碳酸钠溶液”)A溶液的物质的量浓度为 mol·L -1。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省宁波市高一上学期期末考试化学试卷(解析版) 题型:选择题
材料与化学密切相关,表中对应关系错误的是
材料主要化学成分
A刚玉、金刚石三氧化二铝
B大理石、石灰石碳酸钙
C普通水泥、普通玻璃硅酸盐
D光导纤维、石英二氧化硅
查看答案和解析>>
科目:高中化学 来源:2016届浙江省宁波市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列物质属于纯净物的是
A.青铜 B. CuSO4?5H2O C.水玻璃 D.Fe(OH)3胶体
查看答案和解析>>
科目:高中化学 来源:2016届浙江省宁波市八校高一上学期期末联考化学试卷(解析版) 题型:选择题
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是
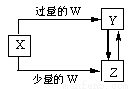
选项 W X
A 盐酸Na2CO3溶液
BNaOH溶液AlCl3溶液
CCO2Ca(OH)2溶液
DCl2Fe
查看答案和解析>>
科目:高中化学 来源:2016届浙江省宁波市八校高一上学期期末联考化学试卷(解析版) 题型:选择题
在含有Fe3+、Fe2+、Al3+、NH4+的稀溶液中,加入足量的Na2O2固体,充分反应后,再加入过量的稀盐酸,完全反应后,离子数目几乎没有变化的是
A.Fe3+ B.Al3+ C.NH4+ D.Fe2+
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高一下学期第一次质量检测化学试卷(解析版) 题型:填空题
(1)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。甲、乙两元素相比较,金属性较强的是 (填名称),
可以验证该结论的实验是 。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
(2)通常情况下,微粒X和Y为分子,Z和W为阳离子,E为阴离子,它们都含有10个电子;
Y溶于X后所得的物质可电离出Z和E;X、Y、W三种微粒反应后可得Z和一种白色沉淀。请回答:
①用化学符号表示下列4种微粒:X: Y : Z: E :
②写出两个X、Y、W三种微粒反应的离子方程式: 、
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高一上学期第一次质检化学试卷(解析版) 题型:选择题
某单质X能从化合物中置换出单质Y,由此可知
①当X是金属时,Y可能是金属 ②当X是金属时,Y可能是非金属
③当X是非金属时,Y可能是金属 ④当X是非金属时,Y可能是非金属
A.①②③ B.①②④ C.①③④ D.①②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com