
����Ŀ������һ���л����ת����ϵ��ͼ��ʾ��ת����ϵ�в��ַ�Ӧ��Ͳ���ʡ�ԣ��漰�Ļ�ѧ��Ӧ��Դ�ڽ̲ġ�
��![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ��
��
��֪������Ȼ�߷��ӻ����Mr(��)��Mr(��)��28�������й��ƶ���ȷ����(����)
A. �����л�������Ԫ����ͬ
B. �ס��ҡ������ܷ���������Ӧ
C. �췢����ȥ��Ӧ���ɼ�
D. ��ȥ��������������ķ���������NaOH��Һ������
���𰸡�A
������������������Ϊ������������������+������������α���Ӧ���˹���ΪRCH2OH![]() RCHO
RCHO![]() RCOOH��RCOOH+RCH2OH
RCOOH��RCOOH+RCH2OH![]() RCOOCH2R+H2O��Mr(��)��Mr(��)��28����RΪ��CH3�����������졢������ΪCH3CH2OH��CH3CHO��CH3COOH��CH3COOCH2CH3��������Ȼ�߷��ӻ����������C6H10O5��n������ˮ�ⷴӦ�����ң������������������Ƿ������ͷ�Ӧ����CH3CH2OH��A���Щ�л�������Ԫ�ض���C��H��O����ȷ��B��ҡ����к�ȩ���ܷ���������Ӧ�������ڷǻ�ԭ���Dz��ܷ���������Ӧ������C���ΪCH3COOH�����������������Ӧ���ɼ�������D���ΪCH3COOCH2CH3��CH3COOCH2CH3��NaOH��Һ�лᷢ��ˮ�⣬������NaOH��Һ��ȥ���������л��е����ᣬ��ȥ���������л��е�����Ӧ���뱥��Na2CO3��Һ����Һ������ѡA��
RCOOCH2R+H2O��Mr(��)��Mr(��)��28����RΪ��CH3�����������졢������ΪCH3CH2OH��CH3CHO��CH3COOH��CH3COOCH2CH3��������Ȼ�߷��ӻ����������C6H10O5��n������ˮ�ⷴӦ�����ң������������������Ƿ������ͷ�Ӧ����CH3CH2OH��A���Щ�л�������Ԫ�ض���C��H��O����ȷ��B��ҡ����к�ȩ���ܷ���������Ӧ�������ڷǻ�ԭ���Dz��ܷ���������Ӧ������C���ΪCH3COOH�����������������Ӧ���ɼ�������D���ΪCH3COOCH2CH3��CH3COOCH2CH3��NaOH��Һ�лᷢ��ˮ�⣬������NaOH��Һ��ȥ���������л��е����ᣬ��ȥ���������л��е�����Ӧ���뱥��Na2CO3��Һ����Һ������ѡA��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֽྻ��ȫ�����滷���ѳ�Ϊȫ����Ĺ�ʶ��
��1����ͥװ�����õĸ��ϰ���г���ų�������������Σ�������ʣ������к�������Ҫ��ָ________�������ƣ���
��2����Ȼˮ�к��е�ϸС�����������������������о�������������ˮ��õ���________��������ϸС����������
��3��Ϊ�˸��ƿ���������������ƴ����ж�������������̳�����Ⱦ����ŷ�����Ϊ���ƴ����ж���������ŷţ�����ȡ�Ĵ�ʩ����ú̿�м���ʯ��ʯ��ĩ�Ի�ʯȼ�Ͻ�������������ԭ���÷���ʽ�ɱ�ʾΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�����ҹ�ʹ������ĺϽ���________��Ŀǰ���������;��㷺�ĺϽ���________��
��2��0.5mol H2O ������Ϊ________g������________��ԭ�ӣ�
��3����������50g ��Cl2��NH3��CO2��O2 ���������У����з��������ٵ���________������ͬ���¶Ⱥ�ѹǿ�£����������________��
��4������100mL 0.2mol/L CuSO4��Һ����ҪCuSO45H2O________g��
��5������������������Һʱ�������������ۣ���˵��ԭ��________�������ӷ���ʽ��ʾ��
��6���������Ƹ�ˮ��Ӧ�Ļ�ѧ����ʽ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ���ֻ�����Ľṹ������������ȷ���ǣ� ��
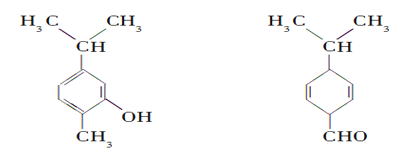
A. ����ͬ���칹��
B. �����й�ƽ���̼ԭ������ͬ
C. ��������ˮ��Ӧ
D. ���ú���������֣��������ú˴Ź�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����( )
A. ������ͨʽΪCnH2n��2����nֵ����̼Ԫ�ص������ٷֺ�����С
B. ��ϩ����ӳɷ�Ӧ�IJ���Ϊ������
C. 1 mol��ǡ����3 mol������ȫ�ӳɣ�˵����������������̼̼˫��
D. n��7����������5��̼ԭ�ӵ���������5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1��3-����ϩ������������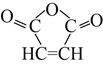 ������Ҫ�Ļ���ԭ�ϣ������ںϳɿɽ����PBS���Ϻ��¿��ᡣ
������Ҫ�Ļ���ԭ�ϣ������ںϳɿɽ����PBS���Ϻ��¿��ᡣ

��֪��
��1����Ӧ�ٵķ�Ӧ������_______________________��
��2��C�ķ���ʽ��C4H4O4����һ�ֶ�Ԫ���ᡣCΪ˳ʽ�ṹ���ṹ��ʽ��____________��
��3����Ӧ�ڵĻ�ѧ����ʽ��__________________________________________________��
��4��E�ķ���ʽC6H8O4��
i��G��������________________��
ii��H�Ľṹ��ʽ��____________________________��
��5�����¿��������ͬ�������Ŀ�Ĺ����ŵ�ͬ���칹�����Ŀ��_________��������˳���칹����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ȡȾ�Ϻ�һЩҩ�����Ҫ�м��壬���ɱ����ǻ��õ���
![]() ��H2SO4
��H2SO4![]()
![]() ��H2O
��H2O
ʵ���ҿ�������ͼ��ʾװ�úϳɶ��������ᡣʵ�鲽�����£�

����һ��250 mL������ƿ�м���10 mL������������ʯ����������ƿ������ˮ����ȴ��С�ĵؼ���18 mLŨ���ᡣ
�ڽ�������ƿ������ԡ�л���������170��180 ����ά�ִ��¶�2��2.5 h��
�۽���ӦҺ��ȴ��Լ50 ������ʢ��100 mL��ˮ���ձ��У����������Ͻ��裬��ʹ�������������ˣ���������ˮϴ�ӣ��õ��ľ����Ƕ���������ֲ�Ʒ��
�ܽ��ֲ�Ʒ�÷�ˮ�ܽ⣬��ȴ�ᾧ(����Һ��ɫ������û���̿��ɫ)�����ˣ��ռ���Ʒ������(100 mLˮ��20 ��ʱ���ܽ����������1.08 g����100 ��ʱ���ܽ�6.67 g)��
��1��װ���������ܵ�������____________________��
��2��������в�����ԡ���ȣ�����ԡ���ȵ��ŵ���____________________��
��3���������������ˮϴ�Ӿ���ĺô���____________________��
��4������ۺܾ͢����г��ˣ��ڳ��˺�ֹͣ����ʱ��Ӧע����__________________��Ȼ��__________________���Է�������
��5�����������ʱ��Ҫ�����ֲ�Ʒ�÷�ˮ�ܽ⣬��ȴ�ᾧ���������IJ������ж�Σ���Ŀ����____________________________��ÿ�γ��˺��Ӧ��ĸҺ�ռ����ʵ���������Ŀ����____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӳ�ʲ������е�A��B��C�����η��н���KBr��Һ��KI��Һ��������Һ������������ͼ��ʾ��������˵���Cl2����B�����ȣ��ɹ۲쵽A�������_________ɫ��B�������_________ɫ��C�������________ɫ�����Թ���ȴ����B��C֮��IJ���������________ɫ��________��������Ϊ_________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȼ��ر�����ڴ�������ͭ��������Ƶú��Ȼ��������ʵ��Ȼ�ͭˮ��Һ��Ϊ��ȡ������CuCl22H2O�����Ƚ����Ƴ�ˮ��Һ��Ȼ����ͼ��������ᴿ��

��֪Cu2+��Fe3+��Fe2+���������↑ʼ����ȫ����ʱ��pH����������ش�
Fe3+ | Fe2+ | Cu2+ | |
�������↑ʼ����ʱ��pH | 1.9 | 7 | 4.7 |
����������ȫ����ʱ��pH | 3.2 | 9 | 6.7 |
��1��������������Ŀ����___________________________ ��
��2�����ʺ���������X����_______������ţ���
A��K2Cr2O7 B��NaClO C��H2O2 D��KMnO4
�����������£�������X��Fe2+��Ӧ�����ӷ���ʽΪ________________________ ��
��3�����������Y�Ե�����ҺpH��Y�Ļ�ѧʽ�� _____��pH�ķ�Χ�� ________��
��4��ֻ����HCl�����м���Ũ�����ܵõ�CuCl22H2O���壬HCl������������ǣ�____________________________
��5����֪Ksp��ZnS����Ksp��CuS�����ر���ԭ��ͭ�����ᆳ������ˮ�����ú���CuSO4��Һ�����������������������ܵ�ZnS����ת��Ϊͭ����CuS���������ӷ���ʽ����ZnS��ת��ΪCuS��ԭ�� __________________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com