
| A. | 2.4g镁变成Mg2+时失去的电子数目为0.2NA | |
| B. | 常温常压下,11.2L氧气所含的O原子数为NA | |
| C. | 如果11.2LN2中含有n个分子,则阿伏加德罗常数一定为2n | |
| D. | 1 mol•L-1的KSCN和1mol•L-1KAl(SO4)2溶液中,所含K+数都是NA |
分析 A.根据n=$\frac{m}{M}$计算出镁的物质的量,然后计算出失去电子的物质的量及数目;
B.常温常压下,不能使用标况下的气体摩尔体积计算;
C.不是标况下,无法计算氮气的物质的量;
D.缺少溶液体积,无法计算含有钾离子数目.
解答 解:A.2.4g镁的物质的量为:$\frac{2.4g}{24g/mol}$=0.1mol,变成0.1mol Mg2+时失去0.2mol电子,失去电子的数目为0.2NA,故A正确;
B.不是标况下,不能使用标准状况下的气体摩尔体积计算,故B错误;
C.不是标准状况下,不能使用标况下的气体摩尔体积计算11.2LN2的物质的量,故C错误;
D.没有告诉1 mol•L-1的KSCN和1mol•L-1KAl(SO4)2溶液的体积,无法计算溶液中含有钾离子的数目,故D错误;
故选A.
点评 本题考查阿伏加德罗常数的有应用,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握以物质的量为中心的各化学量与阿伏加德罗常数的关系,试题侧重考查学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 清晨在密林中看到一缕缕的光束 | |
| B. | FeCl3溶液加入NaOH溶液产生红褐色沉淀 | |
| C. | 利用电泳将油漆、乳胶、橡胶等微粒均匀地沉积在镀件上 | |
| D. | 向豆浆中加入硫酸钙使蛋白质等聚沉,制成可口的豆腐 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.5 mL 2 mol•L-1KAl(SO4)2溶液 | B. | 30 mL 1 mol•L-1 MgSO4溶液 | ||
| C. | 20 mL 0.5 mol•L-1Al2(SO4)3溶液 | D. | 10 mL 3 mol•L-1 Na2SO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)=c(OH-) | B. | c(CH3COOH)+c(CH3COO-)=0.1 mol/L | ||
| C. | c(CH3COOH)>c(CH3COO-) | D. | c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的电子式: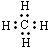 | |
| B. | 氟原子的结构示意图: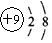 | |
| C. | 乙烯的结构简式:CH2CH2 | |
| D. | 碳酸钠的电离方程式:Na2CO3=Na2++CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com