
白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P akJ·mol-1、P-O bkJ·mol-1、P=O ckJ·mol-1、O=O dkJ·mol-1
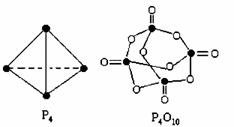
根据图示的分子结构和有关数据估算该反应的 H,其中正确的是
H,其中正确的是
A.(6a+5d-4c-12b) kJ·mol-1
B.(4c+12b-6a-5d) kJ·mol-1
C.(4c+12b-4a-5d) kJ·mol-1
D.(4a+5d-4c-12b) kJ·mol-1
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
下列关于乙烯的说法中错的是 ( )
A.能使酸性高锰酸钾溶液褪色
B.分子中6个原子都在同一平面上
C.分子中C、H元素的质量比为2∶1
D.可以和溴发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
NA为阿伏伽德罗常数,下列叙 述错误的是
述错误的是
A.标准状况下,11. 2 L氦气中含有0.5 NA原子
2 L氦气中含有0.5 NA原子
B.标准状况下,0.1 mol Cl2参加反应,转移的电子数目一定为0. 2 NA
C.常温常压下,46g NO2和N2O4混合气体中含有原子总数为3NA
D.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移电子总数NA个
查看答案和解析>>
科目:高中化学 来源: 题型:
近年来我国的航天事业取得了巨大的成就,在航天发射时,常用肼(N2H4)及其衍生物作火箭推进剂。
(1)液态肼作火箭燃料时,与液态N2O4混合发生氧化还原反应,已知每克肼充分反应后生成氮气和气态水放出热量为a KJ,试写出该反应的热化学方程式
(2)在实验室中,用N2H4·H2O与NaOH颗粒一起蒸馏,收集114~116℃的馏分即为无水肼。在蒸馏过程中需要的仪器有酒精灯、锥形瓶、冷凝管、牛角管(接液管)、蒸馏烧瓶,除上述必需的仪器外,还缺少的玻璃仪器是
(3)肼能使锅炉内壁的铁锈(主要成分Fe2O3)变成磁性氧化铁(Fe3O4)层,可减缓锅炉锈蚀。若反应过程中肼转化为氮气,则每生成1molFe3O4,需要消耗肼的质量为 g。
(4)磁性氧化铁(Fe3O4)的组成可写成FeO·Fe2O3。某化学实验小组通过实验来探究一黑色粉末是否由Fe3O4、CuO组成(不含有其它黑色物质)。探究过程如下:
提出假设:假设1. 黑色粉末是CuO; 假设2. 黑色粉末是Fe3O4;
假设3. 。
设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂。
①若溶液显蓝色,则假设1成立。
②若所得溶液显血红色,则假设 成立。
③为进一步探究,继续向②所得溶液加入足量铁粉,若有红色固体析出的现象,则假设3成立。
有另一小组同学提出,若混合物中CuO含量较少,可能加入铁粉后实验现象不明显。
查阅资料:Cu2+与足量氨水反应生成深蓝色溶液,Cu2++4NH3·H2O=Cu(NH3)42++4H2O。
④为探究是假设2还是假设3成立,另取少量粉末加稀硫酸充分溶解后,再加入足量氨水,若假设2成立,则产生 现象;若假设3成立,则产生红褐色沉淀,同时溶液呈深蓝色。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列热化学方程式书写正确的是(ΔH的绝对值均正确)( )
A.C2H5OH(l)+3O2(g)====2CO2(g)+3H2O(g);ΔH=-1 367.0 kJ/mol(燃烧热)
B.NaOH(aq)+HCl(aq)====NaCl(aq)+H2O(l);ΔH=+57.3 kJ/mol(中和热)
C.S(s)+O2(g)====SO2(g);ΔH=-296.8 kJ/mol(反应热)
D.2NO2====O2+2NO;ΔH=+116.2 kJ/mol(反应热)
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制备BaCl2的工艺流程图如下:
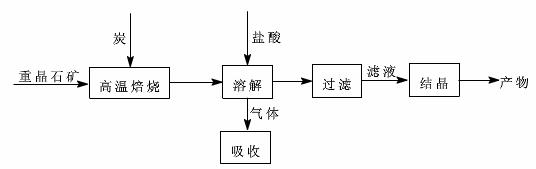
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得
BaSO4(s) + 4C(s)  4CO(g) + BaS(s) △H1 = 571.2
4CO(g) + BaS(s) △H1 = 571.2 kJ·mol-1 ①
kJ·mol-1 ①
BaSO4(s) + 2C(s)  2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
⑴气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为 。
⑵向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,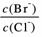 = 。
= 。
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
⑶反应C(s) + CO2(g)  2CO(g)的△H= kJ·mol-1。
2CO(g)的△H= kJ·mol-1。
⑷实际生产中必须加入过量的炭,同时还要通入空气,其目的是 , 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:CH3CH2CH2CH3(g)+6.5O2(g)→4CO2(g)+5H2O(l)+2878kJ
(CH3)2CHCH3(g)+6.5O2(g)→4CO2(g)+5H2O(l)+2869kJ
下列说法正确的是
A 正丁烷分子储存的能量大于异丁烷分子
B 正丁烷的稳定性大于异丁烷
C 异丁烷转化为正丁烷的过程是一个放热过程
D 异丁烷分子中的碳氢键比正丁烷的多
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.常温下,醋酸钠与醋酸的混合溶液PH=7,C(Na+)>c(CH3COO-)
B.0.1mol/LNa2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3)
C.将PH=6的H2SO4稀释1000倍后,c(H+)=2c(SO42-)
D.0.1mol/LNaHCO3溶液中:c(Na+)+c(H+)= c(HCO3-)+ c(OH-)+2c(CO32-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com