
��֪��CH3CH2CH2CH3(g)+6.5O2(g)��4CO2(g)+5H2O(l)+2878kJ
(CH3)2CHCH3(g)+6.5O2(g)��4CO2(g)+5H2O(l)+2869kJ
����˵����ȷ����
A ��������Ӵ�������������춡�����
B ��������ȶ��Դ����춡��
C �춡��ת��Ϊ������Ĺ�����һ�����ȹ���
D �춡������е�̼�����������Ķ�
���𰸡�A
�������������ǿ��������ȶ��Լ������仯����Ŀ��1 mol ������ȼ�շų�2 878 kJ������1 mol�춡��ȼ�շų�2 869 kJ������������ȼ�շų����������춡��ȼ�շų���������A��ȷ���������������ȶ��Բ��B������ʽ�����CH3CH2CH2CH3(g)
������ȼ�շų�2 878 kJ������1 mol�춡��ȼ�շų�2 869 kJ������������ȼ�շų����������춡��ȼ�շų���������A��ȷ���������������ȶ��Բ��B������ʽ�����CH3CH2CH2CH3(g)  (CH3)2CHCH3(g)+9 kJ���춡��ת��Ϊ��������һ�����ȹ��̡���������춡����ͬ���칹�壬������ͬC��H����������10��C��H����
(CH3)2CHCH3(g)+9 kJ���춡��ת��Ϊ��������һ�����ȹ��̡���������춡����ͬ���칹�壬������ͬC��H����������10��C��H����


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������ȵ������£�ֻ��һ���Լ��Ϳ��Լ�������李��Ȼ��ء��Ȼ�þ������������
������Һ�������Լ��ǣ� ��
A.NaOH B.NH3��H2O C.AgNO3 D.BaCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����һ�������¿���ʵ�ֵ���
�ٷǽ����û������ķ�Ӧ�������ᷴӦ��������ǿ�ᡡ��û��ˮ���ɣ�Ҳû�г������������ɵĸ��ֽⷴӦ�����е��ʲμӵķ�������ԭ��Ӧ��
A���٢ڢۢ� B���ڢ� C���٢ڢ� D���٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������ɷ������·�Ӧ��P4+5O2=P4O10����֪�������л�ѧ����Ҫ���յ������ֱ�Ϊ��P��P akJ��mol��1��P��O bkJ��mol��1��P=O ckJ��mol��1��O=O dkJ��mol��1
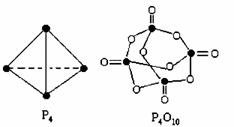
����ͼʾ�ķ��ӽṹ���й����ݹ���÷�Ӧ�� H��������ȷ����
H��������ȷ����
A.(6a+5d��4c��12b) kJ��mol��1
B.(4c+12b��6a��5d) kJ��mol��1
C.(4c+12b��4a��5d) kJ��mol��1
D.(4a+5d��4c��12b) kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����2��5��̼ԭ�ӵ�ֱ�������е��ȼ���ȵ����ݼ��±���
| �������� | ���� | ���� | ���� | ���� |
| �е�(��) | -88.6 | -42.1 | -0.5 | 36.1 |
| ȼ����(kJ��mol-1) | 1560.7 | 2219.2 | 2877.6 | 3535.6 |
*ȼ���ȣ�1Ħ��������ȫȼ�գ����ɶ�����̼��Һ̬ˮʱ���ų�������
���ݱ������ݣ������жϴ������( )��
A.�������ڳ��³�ѹ�¿϶���������
B.����ȼ���Ⱥ�������̼ԭ���������Թ�ϵ
C.��̼ԭ�������ӣ������е�������
D.��̼ԭ�������ӣ������е��ȼ���ȶ��ɱ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪����1 mol H2�����л�ѧ������ʱ��Ҫ����436kJ������
��1 mol Cl2�����л�ѧ������ʱ��Ҫ����243kJ������
����Hԭ�Ӻ�Clԭ���γ�1 mol HCl����ʱ�ͷ�431kJ������
����������ȷ����
A.������������Ӧ�����Ȼ���������Ȼ�ѧ����ʽ��H2(g)+Cl2(g)��2HCl(g)
B.������������Ӧ����2 mol�Ȼ������壬��Ӧ�ġ�H��183kJ/mol
C.������������Ӧ����2 mol�Ȼ������壬��Ӧ�ġ�H����183kJ/mol
D.������������Ӧ����1 mol�Ȼ������壬��Ӧ�ġ�H����183kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪���ϩ��a g��Ȳ����ʱ����1mol������̼�����Һ̬ˮ�����ų�����b k J������Ȳȼ�յ��Ȼ�ѧ����ʽ��ȷ����
A.2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ��H����4b k J/mol
B.C2H2(g)+ O2(g) ===2CO2��g��+H2O(l) ��H��2b k J/mol
O2(g) ===2CO2��g��+H2O(l) ��H��2b k J/mol
C.2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ��H����2b k J/mol
D.2C2H2(g)+5O2(g)=== 4CO2(g)+2H2O(l) ��H��b k J/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪X��Y��Z����Ԫ����ɵĻ����������Ӿ��壬
�侧������ͼ��ʾ���������ʾ�û�����Ļ�ѧʽ��ȷ���ǣ� ��
A��ZXY3 B��ZX2Y6 C��ZX4Y8 D��ZX8Y12

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
10000Cʱ�������ƿ�������������Ӧ:

 ����ش��������⣺
����ش��������⣺
��1��������Ӧ��ƽ�ⳣ������ʽΪ�� ��
��2��������Ӧ��������ͬ�����½��У�����H2��Ũ����ʱ��ı仯��ͼ��ʾ��

��������a�Ƚϣ�b��c�ֱ���ı�һ�ַ�Ӧ������������b�ı������Ϊ
�ڸ÷�Ӧ�ġ�H___0�����������������=���������ж������� ��
��3�����¶��£���2Lʢ��1.42g Na2SO4���ܱ�������ͨ��H2,5min����
��������Ϊ1.10g�����ʱ�䷶Χ�ڵ�ƽ����Ӧ����v(H2)= ��
��4����˵���÷�Ӧ�Ѵﵽƽ��״̬���� ������ĸ����ͬ����
a.������ѹǿ���ֲ���
b.�����������ܶȱ��ֲ���
c.c(H2)=c(H2O)d.v��(H2)=v��(H2O)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com