
含有2~5个碳原子的直链烷烃沸点和燃烧热的数据见下表:
| 烷烃名称 | 乙烷 | 丙烷 | 丁烷 | 戊烷 |
| 沸点(℃) | -88.6 | -42.1 | -0.5 | 36.1 |
| 燃烧热(kJ·mol-1) | 1560.7 | 2219.2 | 2877.6 | 3535.6 |
*燃烧热:1摩尔物质完全燃烧,生成二氧化碳、液态水时所放出的热量
根据表中数据,下列判断错误的是( )。
A.正庚烷在常温常压下肯定不是气体
B.烷烃燃烧热和其所含碳原子数成线性关系
C.随碳原子数增加,烷烃沸点逐渐升高
D.随碳原子数增加,烷烃沸点和燃烧热都成比例增加
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
2014年3月11某高速公路萧山路段一辆运送化学物品的槽罐车侧翻,罐内15 t苯泄漏
入路边300 m长的水渠,造成严重危险,许多新闻媒体进行了报道,以下报道中有科学性错误的是( )
A.由于大量苯溶入水中渗入土壤,会对周边农田、水源造成严重污染
B.由于苯是一种易挥发、易燃的物质,周围地区如果有一个火星就可能引起爆炸
C.可以采取抽吸水渠中上层液体的办法,达到部分清除泄漏物的目的
D.处理事故时,由于事故发生地周围比较空旷,有人提出用点火焚烧的办法来清除泄漏物,但由于苯燃烧会产生大量的黑烟扩大污染,所以该办法未被采纳
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中各微粒的浓度关系不正确的是
A.0.1 mol/L的HCOOH溶液中:c(HCOO—)+c(OH—)=c(H+)
B.1 L 0.1 mol/L的CuSO4·(NH4)2SO4·6H2O的溶液中: c(SO42—)>c(NH4+)>c(Cu2+)>c(H+)>c (OH—)
C.0.1 mol/L 的NaHCO3溶液中: c(Na+)+c(H+)=c(HCO3—)+2c(CO32—)+c(OH—)
D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X—)>c(H+)>c(OH—)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列热化学方程式书写正确的是(ΔH的绝对值均正确)( )
A.C2H5OH(l)+3O2(g)====2CO2(g)+3H2O(g);ΔH=-1 367.0 kJ/mol(燃烧热)
B.NaOH(aq)+HCl(aq)====NaCl(aq)+H2O(l);ΔH=+57.3 kJ/mol(中和热)
C.S(s)+O2(g)====SO2(g);ΔH=-296.8 kJ/mol(反应热)
D.2NO2====O2+2NO;ΔH=+116.2 kJ/mol(反应热)
查看答案和解析>>
科目:高中化学 来源: 题型:
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g) CH4(g)+HC≡CH(g)+H2(g) △H1=156.6 kJ·mol-1
CH4(g)+HC≡CH(g)+H2(g) △H1=156.6 kJ·mol-1
CH3CH=CH2(g) CH4(g)+HC≡CH(g) △H2=32.4 kJ·mol-1
CH4(g)+HC≡CH(g) △H2=32.4 kJ·mol-1
则相同条件下,反应C3H3(g) CH3CH=CH2(g)+H2(g)的△H=_____kJ·mol-1
CH3CH=CH2(g)+H2(g)的△H=_____kJ·mol-1
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应方程式为___________;放电时, 移向电池的_______(填“正”或“负”)极。
移向电池的_______(填“正”或“负”)极。
(3)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3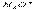
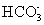 +H+的平衡常数K1=_____________。(已知:10-5.60=2.5×10-6)
+H+的平衡常数K1=_____________。(已知:10-5.60=2.5×10-6)
(4)常温下,0.1 mol·L-1NaHCO3溶液的pH大于8,则溶液c(H2CO3)______c( )(填“>”、“=”或“<”),原因是__________(用离子方程式和必要的文字说明)。
)(填“>”、“=”或“<”),原因是__________(用离子方程式和必要的文字说明)。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:CH3CH2CH2CH3(g)+6.5O2(g)→4CO2(g)+5H2O(l)+2878kJ
(CH3)2CHCH3(g)+6.5O2(g)→4CO2(g)+5H2O(l)+2869kJ
下列说法正确的是
A 正丁烷分子储存的能量大于异丁烷分子
B 正丁烷的稳定性大于异丁烷
C 异丁烷转化为正丁烷的过程是一个放热过程
D 异丁烷分子中的碳氢键比正丁烷的多
查看答案和解析>>
科目:高中化学 来源: 题型:
.25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2800 kJ/mol,则下列热化学方程式正确的是
A.C(s)+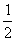 O2(g)==CO(g);△H=-393.5 kJ/mol
O2(g)==CO(g);△H=-393.5 kJ/mol
B.2H2(g)+O2(g)==2H2O(g);△H=+571.6 kJ/mol
C.CH4(g)+2O2(g)==CO2(g)+2H2O(g);△H=-890.3 kJ/mol
D.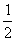 C6H12O6(s)+3O2(g) === 3CO2(g)+3H2O(1);△H=-1400 kJ/mol
C6H12O6(s)+3O2(g) === 3CO2(g)+3H2O(1);△H=-1400 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂溶解在亚硫酰氯(SOCl2)中形成,电池的总反应式为8Li+3SOCl2=6LiCl+Li2SO3+2S,则下列叙述正确的是 ( )
A.用该电池电解CuCl2溶液产生2.24LCl2时,有0.2mol电子转移
B.金属锂作电池的负极,石墨作电池的正极,加入硫酸可提高电解质的导电性
C.电池工作(放电)过程中,SOCl2被还原为Li2SO3
D.电池工作过程中,负极消耗的锂与正极生成的硫质量之比为7:8
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com