
����Ŀ��25��ʱ����0.25mol��L-1��NaOH��Һ���ֱ�ζ�ͬŨ�ȵ�����ϡ����Һ���ζ���������ͼ��ʾ�������ж�����ȷ����
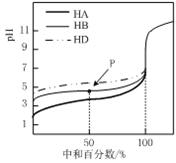
A. ͬŨ�ȵ�ϡ���У�c(A��)>c(B��)>c(D��)
B. �ζ���P��ʱ����Һ�У�c(B��)>c(HB)
C. pH=7ʱ��������Һ�У�c(A��)>c(B��)>c(D��)
D. ���кͰٷ�����100%ʱ����������Һ��Ϻ�c(HA)��c(HB) ��c(HD)�Tc(OH��)��2c(H��)
���𰸡�D
��������
A������ͼ���֪0.1mol��L��1��������(HA��HB��HD)��Һ����ʼpHֵHA��С��������ǿ��HD��pH�����������������Խǿ��������ӵ�Ũ��Խ��A��ȷ��B���ζ���P��ʱ����Ϊ�����ʵ���Ũ�ȵ�HB��NaB����Һ�����ԣ�HB�ĵ���Ϊ����������̶Ƚ�С�����c(B��)>c(HB)��B��ȷ��C��pH=7ʱ��������Һ�������ӵ�ˮ��̶Ȳ�ͬ��D��ˮ��̶������������Һ�У�c(A��)>c(B��)>c(D��)��C��ȷ��D�������Һ�������غ��ϵʽ��c(HA)��c(HB)��c(HD)=c(OH��)��c(H��)��D����ѡD��
���磺���ж���Һ����Ũ�ȴ�С�ıȽ�ʱ��Ҫ�ص�������غ��ϵ��������˼������1�������������ݣ���������ʵ������ۣ���������Ũ�ȴ��ڵ�����������Ũ�ȡ�����H2CO3��Һ�У�c(H2CO3)��c(HCO3��)c(CO32��)(��Ԫ�����һ������̶�ԶԶ���ڵڶ�������)����ˮ�����ۣ�ˮ�����ӵ�Ũ�ȴ���ˮ����������Ũ�ȡ�����Na2CO3��Һ�У�c(CO32��)��c(HCO3��)c(H2CO3)(��Ԫ��������ӵ�ˮ���Ե�һ��Ϊ��)����2�������غ��ϵ��������غ㣺����غ���ָ��Һ���뱣�ֵ����ԣ�����Һ�����������ӵĵ����Ũ�ȵ������������ӵĵ����Ũ�ȡ��������غ㣺�����غ�Ҳ����ԭ���غ㣬�仯ǰ��ij��Ԫ�ص�ԭ�Ӹ����غ㡣�������غ㣺��ˮ�������c(H��)������ˮ�������c(OH��)���ڼ�������Һ��OH���غ㣬����������Һ��H���غ㡣�����غ�Ĺ�ϵʽҲ�����ɵ���غ�ʽ�������غ�ʽ�Ƶ��õ��������ʱ���ܹ���ͼ�����ʼ��ó�����������ǿ���ǽ���Ĺؼ���


 ��Уͨ��֤��Ч��ҵϵ�д�
��Уͨ��֤��Ч��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���1 L���ܱ������У�X��Y��Z������������ʵ�����ʱ��仯��������ͼ��ʾ������������ȷ����
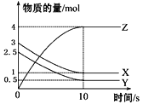
A.��Ӧ�Ļ�ѧ����ʽΪ2X��g��+Y��g��![]() 2Z��g��
2Z��g��
B.��Ӧ��ʼ��10 s����Z��ʾ�ķ�Ӧ����Ϊ0.3 mol��L-1��s-1
C.10 s�÷�Ӧֹͣ����
D.��Ӧ��ʼ��10 sʱ����Ӧ���ʣ�����X��=����Y��=0.2 mol��L-1��s-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I.������ ������ ���ױ� �������� ����ϩ ���Ҵ��У������ţ�
<1>�ܺͽ����Ʒ�Ӧ�ų�H2����______ <2>����NaOH��Һ��Ӧ����______
<3>������������ˮ��Ӧ����_________ <4>��ʹ����KMnO4��Һ��ɫ������_______
II.��֪ij�л���Ľṹ��ʽΪ�� ![]()
�����л��������������ŵ�������________________________��
�����л�����Ӿ۷�Ӧ�����ò���Ľṹ��ʽΪ__________��
��д�����л������ȥ��Ӧ�Ļ�ѧ����ʽ��ע����Ӧ��������_________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ijˮ��Һ�е�![]() ��
��![]() Ũ�ȱ仯������ͼ��ʾ������˵������ȷ����
Ũ�ȱ仯������ͼ��ʾ������˵������ȷ����
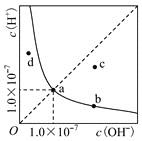
A.������ˮ�м���NaOH�������ܽ��ָ������£���Һ���տ�������b��
B.![]() ��HCl�Ļ����Һ��ˮ�������
��HCl�Ļ����Һ��ˮ�������![]() Ũ�ȿ��ܵ���d������
Ũ�ȿ��ܵ���d������
C.��b���ʾ��NaR��ˮ��Һ����������ε��������HR��Һ��������b��c�ı仯
D.��c���ʾij�¶�����NaHA��ˮ��Һ����![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������![]() ��Һ����μ���
��Һ����μ���![]() ��һԪ��HA����Һ��pH�ı仯������ͼ��ʾ�� ����ȷ����
��һԪ��HA����Һ��pH�ı仯������ͼ��ʾ�� ����ȷ����
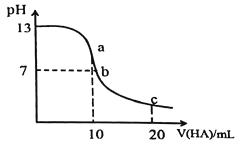
A.a��ʱ����Һ�д���![]()
B.b��ʱ��![]()
C.c��ʱ����Һ�д���![]()
D.ˮ�ĵ���̶ȣ�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CoCl2��6H2O��һ������Ӫ��ǿ������һ������ˮ�ܿ�(��Ҫ�ɷ�ΪCo2O3��Co(OH)3����������Fe2O3��Al2O3��MnO��)��ȡCoCl2��6H2O�Ĺ����������£�

��֪���ٽ���Һ�к��е���������Ҫ��H+��Co2+��Fe2+��Mn2+��Al3+�ȣ�
�ڲ���������������������ʽ����ʱ��Һ��pH���±���(��������Ũ��Ϊ��0��01mol/L)
������ | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
��ʼ���� | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
��ȫ���� | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
��CoCl2��6H2O�۵�Ϊ86�棬������110~120��ʱ��ʧȥ�ᾧˮ������ˮ�Ȼ��ܡ�
��1��д������������Co2O3������Ӧ�����ӷ���ʽ______________��
��2��д��NaClO3������Ӧ����Ҫ���ӷ���ʽ______________����������������Һ���мӹ���NaClO3ʱ�����ܻ������ж����壬д�����ɸ��ж���������ӷ���ʽ_____________��
��3������Na2CO3��pH��a��,�������õ������ֳ����Ļ�ѧʽΪ___________��
��4���Ƶõ�CoCl2��6H2O�ں��ʱ���ѹ��ɵ�ԭ����__________________��
��5����ȡ���Խ������ӵ���ȡ����pH�Ĺ�ϵ��ͼ��������Һ���м�����ȡ����Ŀ����_________����ʹ�õ����pH��Χ��________________��
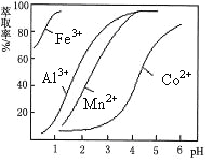
A��2.0~2.5 B��3.0~3.5 C��4.0~4.5 D��5.0~5.5
��6��Ϊ�ⶨ�ֲ�Ʒ��CoCl2��6H2O��������ȡһ�������Ĵֲ�Ʒ����ˮ����������AgNO3��Һ�����ˡ�ϴ�ӣ���������ɺ����������ͨ�����㷢�ֲִ�Ʒ��CoCl2��6H2O��������������100������ԭ�������________________������һ�����ɣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ 25����ʱ��NH3��H2O kb=1.77��10-5��H2CO3 ka1=4.30��10-7��ka2=5.61��10-11�� 25��ʱ�й�NH4HCO3��Һ��˵������ȷ����
A. ��������
B. c(OH-)+c(NH3��H2O)=c(H+)+c(H2CO3)
C. ����NaOH ��Һ������Ӧ:NH4++OH-=NH3��H2O��HCO3-+OH-=H2O+CO32-
D. ����NaOH��Һ����![]() ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������﮼��仯������;�㷺�����������Ĺ̶�����ת��������ͼ��ʾ��
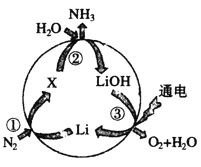
(1)ͼ��X�Ļ�ѧʽΪ__________��
(2)ͼ����ʾ���ʼȺ����ۼ����ֺ����Ӽ�����_______(�ѧʽ)�����ڵ���ʵ���______�֡�
(3)���������缫��ӦʽΪ____________________��
(4)ͼ����ʾ������ת����ϵʽΪ_______________��
(5)LiҲ�����ڿ�����CO2�Ĺ̶����乤��ԭ��Ϊ��4Li+3CO2![]() 2Li2CO3+C����صĵ���ʳ�Ϊ��ص���ѪҺ�����õ�صĵ����ӦΪ_______________(�ѧʽ)�������缫��ӦʽΪ_________________________________����Ӧ�е���3mol����������ԭ��ͨ������Ĥ��Li+Ϊ_________mol��
2Li2CO3+C����صĵ���ʳ�Ϊ��ص���ѪҺ�����õ�صĵ����ӦΪ_______________(�ѧʽ)�������缫��ӦʽΪ_________________________________����Ӧ�е���3mol����������ԭ��ͨ������Ĥ��Li+Ϊ_________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�����ͬŨ�ȵ�NaOH��Һ���ֱ�ζ�Ũ�Ⱦ�Ϊ0.1mol��L��1��������(HA��HB��HD)��Һ���ζ���������ͼ��ʾ�������жϴ������( )
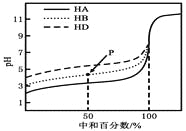
A. ������ĵ��볣����ϵ��KHA��KHB��KHD
B. �ζ���P��ʱ����Һ�У�c(B��)��c(Na��)��c(HB)��c(H��)��c(OH��)
C. pH=7ʱ��������Һ�У�c(A��)=c(B��)=c(D��)
D. ���кͰٷ�����100%ʱ����������Һ��Ϻ�c(HA)��c(HB)��c(HD)=c(OH��)��c(H��)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com