
【题目】金属锂及其化合物用途广泛。其在“氮的固定”中转化过程如图所示:
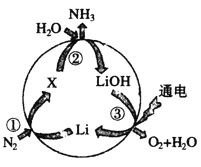
(1)图中X的化学式为__________。
(2)图中所示物质既含共价键、又含离子键的是_______(填化学式),属于电解质的有______种。
(3)③中阳极电极反应式为____________________。
(4)图中所示过程总转化关系式为_______________。
(5)Li也可用于空气中CO2的固定,其工作原理为:4Li+3CO2![]() 2Li2CO3+C。电池的电解质称为电池的“血液”,该电池的电解质应为_______________(填化学式)。正极电极反应式为_________________________________。反应中当有3mol氧化剂被还原,通过交换膜的Li+为_________mol。
2Li2CO3+C。电池的电解质称为电池的“血液”,该电池的电解质应为_______________(填化学式)。正极电极反应式为_________________________________。反应中当有3mol氧化剂被还原,通过交换膜的Li+为_________mol。
【答案】Li3N LiOH 3 4OH--4e-==2H2O+O2↑ 2N2+6H2O==4NH3+3O2 Li2CO3 3CO2+4e-==C+2CO32- 12
【解析】
(1)根据图中信息,锂和氮气反应得到答案。
(2)LiOH含有离子键和共价键, LiOH、NH3、Li3N是电解质。
(3)阳极是溶液中的氢氧根失去电子。
(4)根据图中信息得出氮气和水反应生成氨气和氧气,因此得总反应。
(5)根据电池工作原理分析得出负极为Li,正极为二氧化碳反应,电池的电解质称为电池的“血液”,该电池的电解质应为Li2CO3。正极电极反应式为3CO2 + 4e-= C+2CO32-,根据反应方程式中分析电子转移,再根据物质呈电中性原则,得到锂离子移动的物质的量。
(1)根据图中信息,锂和氮气反应生成氮化锂,因此X的化学式为Li3N,故答案为:Li3N。
(2)图中所示物质既含共价键、又含离子键的是LiOH,属于电解质的有LiOH、NH3、Li3N三种,故答案为:LiOH;3。
(3)③中是电解LiOH,因此阳极电极反应式为4OH--4e-==2H2O+O2↑,故答案为:4OH--4e-==2H2O+O2↑。
(4)根据图中信息得出氮气和水反应生成氨气和氧气,因此总转化关系式为2N2+6H2O = 4NH3 + 3O2,故答案为:2N2+6H2O = 4NH3 + 3O2。
(5)根据电池工作原理:4Li+3CO2![]() 2Li2CO3+C,分析得出负极为Li,正极为二氧化碳反应,电池的电解质称为电池的“血液”,该电池的电解质应为Li2CO3。正极电极反应式为3CO2 + 4e-= C+2CO32-,反应中3mol二氧化碳参与反应,转移4mol电子,只有1mol二氧化碳作氧化剂,因此反应中当有3mol氧化剂被还原,有12mol电子转移,有12mol负电荷,电荷守恒,因此通过交换膜的Li+为12mol,故答案为:3CO2 + 4e-= C+2CO32-;12。
2Li2CO3+C,分析得出负极为Li,正极为二氧化碳反应,电池的电解质称为电池的“血液”,该电池的电解质应为Li2CO3。正极电极反应式为3CO2 + 4e-= C+2CO32-,反应中3mol二氧化碳参与反应,转移4mol电子,只有1mol二氧化碳作氧化剂,因此反应中当有3mol氧化剂被还原,有12mol电子转移,有12mol负电荷,电荷守恒,因此通过交换膜的Li+为12mol,故答案为:3CO2 + 4e-= C+2CO32-;12。


 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
【题目】超纯氢氟酸主要用作芯片材料清洗和蚀刻。回答下列问题:
(1)氢氟酸可保存在聚四氟乙烯容器中,聚四氟乙烯的结构简式为_____________________。
(2)工业氢氟酸生产超纯氢氟酸时,需经除杂质(AsF3)、气化、洗涤等步骤。
①除去AsF3的反应为4AsF3+4KMnO4=4MnO4+2As2O5+4KF+3O2↑,该反应的氧化产物为___________。
②CoF3可与H2O反应生成HF,该反应的化学方程式为___________________________(CoF3还原为CoF2)
③在无水氟化氢汽化时,可向发生装置中掺入含有F2,NF3和OF2中的一种或多种的含氟气体,以氧化杂质。NF3的电子式为_________;OF2中氧元素的化合价为___________,OF2可由F2与稀NaOH溶液反应制取,该反应的离子方程式为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.25mol·L-1的NaOH溶液,分别滴定同浓度的三种稀酸溶液,滴定的曲线如图所示,下列判断不正确的是
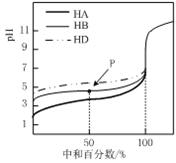
A. 同浓度的稀酸中:c(A-)>c(B-)>c(D-)
B. 滴定至P点时,溶液中:c(B-)>c(HB)
C. pH=7时,三种溶液中:c(A-)>c(B-)>c(D-)
D. 当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB) +c(HD)═c(OH-)-2c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t ℃时AgCl的Ksp=4×10-10 mol2·L-2,下列说法不正确的是( )
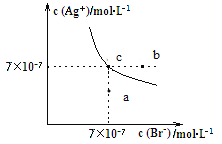
A.在t ℃时,AgBr的Ksp为4.9×10-13 mol2·L-2
B.在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点
C.图中a点对应的是AgBr的不饱和溶液
D.在t ℃时,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)的平衡常数K≈816
AgBr(s)+Cl-(aq)的平衡常数K≈816
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库,人类可以从海水中提取各种化工产品。下图是某工厂对海水综合利用的示意图:
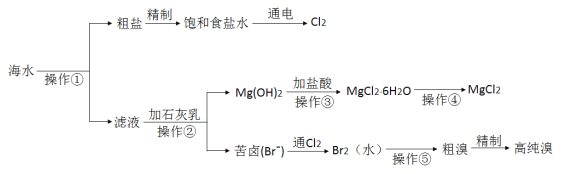
完成下列填空:
(1)写出电解饱和食盐水的化学方程式_____________,检验氯气生成的方法是_________。
(2)液氯储存在钢瓶中,钢瓶上应贴的标签为_________________(选填编号)。
a.自燃品 b.爆炸品 c.有毒品 d.易燃品
(3)Mg(OH)2加入盐酸充分反应后,操作③ 是从MgCl2溶液中获得MgCl26H2O晶体,此处需要进行的实验操作依次为____________________________。
(4)操作④是加热MgCl26H2O获得MgCl2,简述其实验操作及其原因________________。
(5)操作⑤是向溶液中鼓入__________,即可将溴单质从溶液中分离出来,此方法的成功应用是基于溴单质有____________性。
(6)粗溴的精制过程是先将粗溴用SO2水溶液吸收,将其转变成Br,再通Cl2,最后蒸馏得到高纯溴。用SO2水溶液吸收Br2的吸收率可达95%,有关反应的离子方程式为_________。由此反应可知,除环境保护外,在工业生产中应解决的主要问题是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于如图所示的锂离子电池体系的叙述错误的是( )
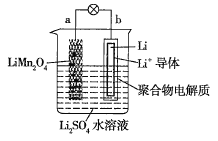
A.a极为电池的正极
B.放电时,b极的电极反应式为Li-e-=Li+
C.放电时,a极锂元素的化合价发生变化
D.放电时,溶液中Li+向a极迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为体现节能减排的理念,中国研制出了新型固态氧化物燃料电池(SOFC),该电池的工作原理如图所示。下列说法正确的是( )
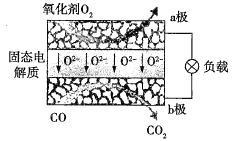
A.可以选用NaOH固体作固态电解质
B.正极的电极反应式为O2+4e-+2H2O=4OH-
C.电子从b极经导线流向a极
D.若反应中转移1 mol电子,则生成22.4 L(标准状况下)CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.50℃时,水在0.1mol/L盐酸中与在0.1mol/LNaOH溶液中的电离程度相同
B.pH等于7的溶液一定呈中性
C.水的离子积表示在水溶液中由水电离出的H+和OH-浓度符合Kw=c(H+)·c(OH-)
D.将0.06mol·L-1氢氧化钡溶液与0.1mol·L-1盐酸溶液等体积混合,该混合溶液的pH等于13(忽略混合过程中溶液体积变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或处理事故的方法正确的是( )
A.用干燥的pH试纸测定NaClO溶液的pH
B.在耐高温的石英坩埚中进行熔化氢氧化钠固体的实验
C.用分液漏斗分离乙酸乙酯和水的混合物时,水从下口放出,乙酸乙酯从上口倒出
D.欲配制质量分数为10%的硫酸铜溶液,可准确称取10 g硫酸铜晶体溶于90 g水中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com