
(7分)火箭推进器中盛有强还原剂液态胼(N![]() H
H![]() 凰)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.4 mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256 KJ的热量。
凰)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.4 mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256 KJ的热量。
(1)反应的热化学方程式为 。
(2)又已知H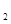 0(I)=H
0(I)=H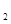 0(g);△H=+44 kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是 KJ。
0(g);△H=+44 kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是 KJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 。
(4)已知N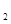 (g)+2O
(g)+2O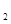 (g)=2N0
(g)=2N0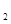 (g) △H=+67.7kJ/mol
(g) △H=+67.7kJ/mol
N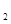 H
H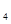 (g)+0
(g)+0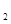 (g)=N
(g)=N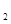 (g)+2H
(g)+2H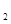 0(g) △H=-534kJ/mol
0(g) △H=-534kJ/mol
则肼与N0![]() 完全反应生成氮气和液态水的热化学方程式为
完全反应生成氮气和液态水的热化学方程式为
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案科目:高中化学 来源: 题型:
( 6 分)回答下列问题:
(1)反应A(g)+B(g)![]() C(g)+D(g)过程中的能量变化如右图所示,判断该反应△H 0 (填“>”、“<”、“无法确定”)。
C(g)+D(g)过程中的能量变化如右图所示,判断该反应△H 0 (填“>”、“<”、“无法确定”)。
(2)在Al2O3、Ni催化下气态甲酸发生下列反应:
甲酸(g)=CO (g)+ H2O (g) △H1= + 34.0 kJ/mol
甲酸(g)=CO2 (g)+ H2(g) △H2=—7.0 kJ/mol
则甲酸的分子式为 ,在该条件下,气态CO2 和气态H2生成气态CO和气态H2O的热化学方程式为 。
(3)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水(H2O2)。
当把0.4mol液态肼和0.8mol液态H2O2混合反应,生成氮气和水蒸气,放出256.7kJ
的热量(相当于25℃、101 kPa下测得的热量)。反应的热化学方程式为
。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山东省德州一中高二模块检测化学试卷 题型:填空题
( 6 分)回答下列问题:
(1)反应A(g)+B(g) C(g)+D(g)过程中的能量变化如右图所示,判断该反应△H 0 (填“>”、“<”、“无法确定”)。
C(g)+D(g)过程中的能量变化如右图所示,判断该反应△H 0 (填“>”、“<”、“无法确定”)。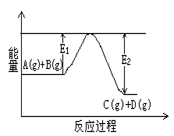
(2)在Al2O3、Ni催化下气态甲酸发生下列反应:
甲酸(g)=" CO" (g)+ H2O (g) △H1=" +" 34.0 kJ/mol
甲酸(g)= CO2 (g)+ H2(g) △H2= —7.0 kJ/mol
则甲酸的分子式为 ,在该条件下,气态CO2和气态H2生成气态CO和气态H2 O的热化学方程式为 。
O的热化学方程式为 。
(3)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧 化剂液态双氧水(H2O2)。
化剂液态双氧水(H2O2)。
当把0.4mol液态肼和0.8mol 液态H2O2混合反应,生成氮气和水蒸气,放出256.7kJ
的热量(相当于25℃、101 kPa下测得的热量)。反应的热化学方程式为
。
查看答案和解析>>
科目:高中化学 来源:2013届河南省濮阳市高二上学期期末考试化学试卷 题型:填空题
(7分)火箭推进器中盛有强还原剂液态胼(N H
H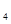 凰)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.4 mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256 KJ的热量。
凰)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.4 mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256 KJ的热量。
(1)反应的热化学方程式为 。
(2)又已知H 0(I)=H
0(I)=H 0(g);△H=+44 kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是
KJ。
0(g);△H=+44 kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是
KJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 。
(4)已知N (g)+2O
(g)+2O (g)=2N0
(g)=2N0 (g)
△H=+67.7kJ/mol
(g)
△H=+67.7kJ/mol
N H
H (g)+0
(g)+0 (g)=N
(g)=N (g)+2H
(g)+2H 0(g)
△H=-534kJ/mol
0(g)
△H=-534kJ/mol
则肼与N0 完全反应生成氮气和液态水的热化学方程式为
完全反应生成氮气和液态水的热化学方程式为
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河南省濮阳市高二上学期期末考试化学试卷 题型:填空题
(7分)火箭推进器中盛有强还原剂液态胼(N H
H 凰)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.4 mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256 KJ的热量。
凰)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.4 mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256 KJ的热量。
(1)反应的热化学方程式为 。
(2)又已知H 0(I)=H
0(I)=H 0(g);△H="+44" kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是 KJ。
0(g);△H="+44" kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是 KJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 。
(4)已知N (g)+2O
(g)+2O (g)=2N0
(g)=2N0 (g) △H=+67.7kJ/mol
(g) △H=+67.7kJ/mol
N H
H (g)+0
(g)+0 (
( g)=N
g)=N (g)+2H
(g)+2H 0(g) △H=-534kJ/mol
0(g) △H=-534kJ/mol
则肼与N0 完全反应生成氮气和液态水的热化学方程式为
完全反应生成氮气和液态水的热化学方程式为 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com