
【题目】在一10 L的密闭容器中充入SO2和O2,发生反应:2SO2(g)+O2(g)![]() 2SO3(g)。测得4 min内,O2的物质的量由开始的18 mol降到14 mol,再过t min,O2的物质的量变为10 mol。求:
2SO3(g)。测得4 min内,O2的物质的量由开始的18 mol降到14 mol,再过t min,O2的物质的量变为10 mol。求:
(1)4 min末SO3的浓度。
(2)4 min内用SO2表示的反应速率。
(3)t (填“>”“<”或“=”)4 min,理由是 。
科目:高中化学 来源: 题型:
【题目】常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后(假设混合液体积为二者之和),所得溶液中部分微粒组分及浓度如图所示,下列说法不正确的是
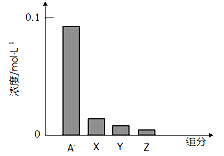
A.HA是弱酸
B.该混合液pH > 7
C.该混合溶液中:c(A-)+c(Y)=c(Na+)
D.图中x表示HA,Y表示OH-,Z表示H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知键能数据:C-H为akJ/mol,O2中看作O=O为bkJ/mol,C=O为mkJ/mol,H-O为nkJ/mol。则可计算CH4(g)+2O2(g)=CO2(g)+2H2O(g)H,此反应H是
A.(+4a+2b-2m-4n)
B.(+4a+2b-2m-4n)KJ/mol
C.-(+4a+2b-2m-4n)KJ/mol
D.(+4a+2b-m-2n)KJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列设计的实验方案能达到实验目的是

A. 制备Fe(OH)2:用图1所示装置,向试管中加入NaOH溶液,振荡
B. 测定H2的生成速率:用图2所示装置,制取一定体积的H2,记录时间
C. 除去苯中少量苯酚:向苯和苯酚的混合液中加入浓溴水,过滤
D. 检验淀粉是否水解:取0.5 g淀粉于洁净的试管中,先加入5 mL稀硫酸,水浴加热,一段时间后再加入少量新制氢氧化铜悬浊液,水浴加热,观察实验现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化工厂常用浓氨水检验管道是否漏氯气,反应的化学方程式为:3Cl2+8NH3=6NH4Cl+N2,当有10.65gCl2消耗时,被氧化的氨的质量为( )
A.3.4g B.1.7g C.6.8g D.0.85g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g); △H= +49.0 kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H= -192.9 kJ·mol-1
下列说法正确的是
A. CH3OH的燃烧热为192.9 kJ·mol-1
B. 反应①中的能量变化如图所示
C. CH3OH转变成H2的过程一定要吸收能量
D. 根据②推知反应: CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微量元素在生物体内虽很少,却是维持正常生命活动不可缺少的,这可以通过下面哪一实例得到说明( )
A. Mg是叶绿素的组成成分 B. 油菜缺少B时会出现“花而不实”
C. 缺P会影响ATP的合成 D. 动物血液Ca盐含量太低会抽搐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请认真观察下图,然后回答问题:

①图中所示反应是_________(填“吸热”或“放热”)反应,该反应________(填“需要”或“不需要”)加热,该反应的ΔH= kJ/mol(用含E1、E2的代数式表示)。
②已知热化学方程式:H2(g)+![]() O2(g)=H2O(g) ΔH=-241.8 kJ/mol。该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为__________kJ/mol。
O2(g)=H2O(g) ΔH=-241.8 kJ/mol。该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为__________kJ/mol。
③对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子的百分数增多,反应速率加快,你认为最可能的原因是:________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com