
【题目】短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四种元素原子的最外电子数纸盒为21。下列关系正确的是
W | X | |||
Y | Z |
A.氢化物沸点:W<Z B.氧化物对应水化物的酸性:Y>W
C.化合物熔点:Y2X3<YZ3 D.简单离子的半径:Y<X
科目:高中化学 来源: 题型:
【题目】在一定温度下,将2mol A和2molB 两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4 mol·L-1,请填写下列空白:
xC(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4 mol·L-1,请填写下列空白:
(1)x值等于________________;
(2)A的转化率为 ;
(3)如果增大反应体系的压强,则平衡体系中C的质量分数 (增大、减小、不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列性质的比较正确的是( )
A.酸性:H2SiO3>H2CO3
B.碱性:Mg(OH)2>Al(OH)3
C.稳定性:SiH4>PH3
D.原子半径:N>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列判断正确的是
A.在pH = 13的溶液中,K+、Cl—、HCO3—、Ba2+可以大量共存
B.在pH=0的溶液中,Na+、NO3—、Fe2+、K+可以大量共存
C.由0.1mol/L一元碱BOH溶液的pH=10,可知:BOH=B++OH—
D.由0.1 mol/L一元酸HA溶液的pH=3,可知:A—+ H2O ![]() HA+ OH—
HA+ OH—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置测定中和热的实验步骤如下:
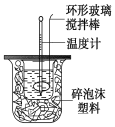
①用量筒量取50 mL 0.25 mol/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50 mL 0.55 mol/L NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。
回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应,表示中和热的热化学方程式(中和热数值为57.3 kJ/mol) 。
(2)倒入NaOH溶液的正确操作是 (从下列选出)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)使硫酸与NaOH溶液混合均匀的正确操作是 (从下列选出)。
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃棒搅拌棒轻轻地搅动
(4)实验数据如下表:
①请填写下表中的温度差平均值:
温度 实验次数 | 起始温度 t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | |
2 | 25.9 | 25.9 | 25.9 | 29.2 | |
3 | 26.4 | 26.2 | 26.3 | 29.8 | |
②近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃),则中和热ΔH= (取小数点后一位)。
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母) 。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时平视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后,用另一支温度计测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓H2SO4 密度1.84g/mL,物质的量浓度为18.4mol/L,质量分数为98%,取10mL浓H2SO4和a mL水混合得物质的量浓度为C mol/L,质量分数为b%.下列组合正确的是
(1)若C=9.2则a>10 b>49%
(2)若C=9.2则a>10 b<49%
(3)若b=49则a=18.4 C<9.2
(4)若b=49则a=18.4 C>9.2.
A.(1)(3) B.(1)(4) C.(2)(3) D.(2)(4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐是一种常用的食品添加剂。新鲜鱼、肉用食盐腌渍后可以延长保存期,是因为( )
A.NACl中的Cl-有杀菌作用 B.浓食盐水中含O2少,细菌无法生存
C.由于渗透作用使细菌失水死亡 D.由于渗透作用使鱼、肉细胞失水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com