
【题目】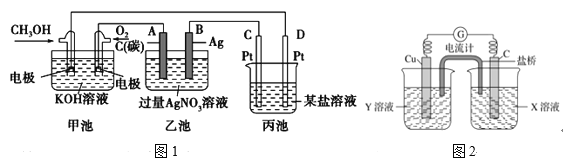
(1)如图1是一个化学过程的示意图。
①甲池中OH-移向______极(填“CH3OH”或“O2”)。
②写出通入CH3OH的电极的电极反应式_________。
③乙池中总反应的离子方程式____________。
④当乙池中B(Ag)极的质量增加5.40g,此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是________
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
(2)利用反应Cu+2FeCl3=CuCl2+2FeCl2设计成如图2所示原电池,回答下列问题:
①写出电极反应式:正极________;负极___________。
②图中X溶液是________,Y溶液是_________。
③原电池工作时,盐桥中的______(填“阳”或“阴”)离子向X溶液方向移动。
【答案】阳 CH3OH CH3OH-6e-+8OH-=CO32-+6H2O 4Ag++2H2O![]() 4Ag+O2↑+4H+ BD 2Fe3++2e-=2Fe2+ Cu-2e-=Cu2+ FeCl3 CuCl2
4Ag+O2↑+4H+ BD 2Fe3++2e-=2Fe2+ Cu-2e-=Cu2+ FeCl3 CuCl2
【解析】
(1)根据图像可知,图1甲池为原电池,且通入甲醇的一极为负极,与负极相连的乙池、丙池中的D、B为阴极;通入氧气的一极为正极,与正极相连的A、C为阳极;
(2)图2为原电池,Cu失电子生成铜离子,作负极;C电极上铁离子得电子作正极;
(1)①分析可知,甲池为原电池,电池内部,阴离子向负极移动,则OH-移向CH3OH电极移动;
②甲醇失电子与氢氧根离子反应生碳酸根离子,电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O;
③乙池为电解池,阳极上水失电子生成氧气和氢离子,阴极银离子得电子生成银,总电极方程式4Ag++2H2O![]() 4Ag+O2↑+4H+;
4Ag+O2↑+4H+;
④当乙池中B(Ag)极的质量增加5.40g,转移电子0.05mol,
A.电解MgSO4溶液时,无金属生成,与题意不符,A错误;
B.电解CuSO4溶液时,若全部为Cu生成1.6g金属,符合题意,B正确;
C.电解NaCl溶液时,无金属生成,与题意不符,C错误;
D.电解AgNO3溶液时,若全部为Ag,生成5.4g金属,只生成1.6g时,说明硝酸银溶液不足,银离子反应完毕生成1.6g银,还有氢气生成,符合题意,D正确;
答案为BD;
(2)①反应Cu+2FeCl3=CuCl2+2FeCl2中,Cu失电子作负极,电极反应式为Cu-2e-=Cu2+;铁离子得电子做正极,电极反应式为2Fe3++2e-=2Fe2+;
②为了使电池减少损耗,使用持久,则Cu电极电解液为硫酸铜;X池电解液为氯化铁;
③原电池工作时,电池内部阳离子向正极移动,阴离子向负极移动;


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】根据如图的转化关系判断下列说法正确的是(反应条件已略去)( )

A.反应①②③④⑤均属于氧化还原反应,反应③还属于置换反应
B.反应⑤说明该条件下铝可用于制熔点较高的金属
C.相同条件下生成等量的O2,反应③和④转移的电子数之比为1∶1
D.反应①中氧化剂与还原剂的物质的量之比为1∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列提供的一组物质回答问题:
①NH4Cl ②MgCl2 ③H2S ④Na2O2 ⑤MgO ⑥Cl2 ⑦NaOH
(1)仅含有共价键的是_________;既有离子键又有共价键的是_________(用序号表示)
(2)离子化合物有_____________________;(用序号表示)
(3)Na2O2 的电子式_____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以“物质的量”为中心的计算是化学计算的基础,下列与“物质的量”相关的计算正确的是( )
A. 现有CO、CO2、O3三种气体,它们分别都含有1 mol O,则三种气体的物质的量之比为3∶2∶1
B. 28 g CO和22.4 L CO2中含有的碳原子数一定相等
C. 标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32
D. a g Cl2中有b个氯原子,则阿伏加德罗常数NA的数值可表示为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】17.4g MnO2与240 mL 10 mol/L(密度为1.10g/mL)的盐酸(足量)混合加热(不考虑盐酸挥发),使其充分反应后,再向溶液中加入足量的AgNO3溶液。(已知:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O)
MnCl2+Cl2↑+2H2O)
试求:(1)10 mol/L的盐酸的质量分数____________
(2)产生的气体在标准状况下的体积______________;
(3)产生沉淀的质量_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在101kPa、25℃条件下,2 mol氢气完全燃烧生成水蒸气放出484kJ的热量,下列热化学方程式正确的是( )
A.H2O(g)=H2(g)+![]() O2(l) △H=+242kJ/mol
O2(l) △H=+242kJ/mol
B.2H2 (g)+O2(g)=2H2O(l) △H=-484kJ/mol
C.H2(g)+![]() O2(g)=H2O(g) △H=-242kJ/mol
O2(g)=H2O(g) △H=-242kJ/mol
D.2H2(g)+O2(g)=2H2O(g) △H=+484kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )
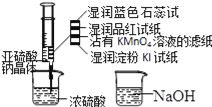
A. 湿润淀粉碘化钾试纸未变蓝说明硫元素的非金属性强于碘元素
B. 沾有KMnO4溶液的滤纸褪色证明了SO2具有漂白性
C. 实验后,可把注射器中的物质缓缓推入NaOH溶液中,以减少环境污染
D. 蓝色石蕊试纸变红说明SO2显酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)用于漂白织物、纤维、纸浆,具有对纤维损伤小的特点.其在溶液中可生成ClO2、HClO2、ClO2﹣、Cl﹣等,其中HClO2和ClO2都具有漂白作用.已知pOH=﹣lgc(OH﹣),经测定25℃时各组分含量随pOH变化情况如图所示(Cl﹣没有画出),此温度下,下列分析正确的是
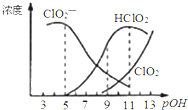
A.HClO2的电离平衡常数的数值Ka=10﹣6
B.亚氯酸钠在酸性条件下较稳定
C.pH=7时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2﹣)>c(ClO2)>c(Cl﹣)
D.同浓度的HClO2溶液和NaClO2溶液等体积混合,则混合溶液中有c(HClO2)-2c(H+)=c(ClO2﹣)-2c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高分子材料PET聚酯树脂和PMMA的合成路线如下图:
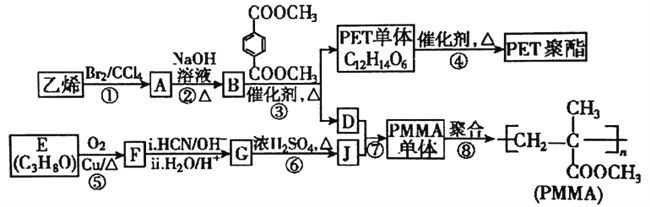
已知:
I.RCOOR+R "OH![]() RCOOR "+ROH (R.R'、R"代表烃基)
RCOOR "+ROH (R.R'、R"代表烃基)
II.  (R代表烃基)。
(R代表烃基)。
(1)PMMA单体的结构简式为_______,PET单体中的官能团名称为________。
(2)反应⑤的反应类型是________;反应②的化学方程式为_________。
(3)若反应④得到的某一条链状产物聚合度为n,则缩聚反应中脱去的小分子有(___)个。
(4)PMMA单体有多种同分异构体,某种异构体K具有如下性质:①不能发生银镜反应②不能使溴水褪色③分子内没有环状结构④核磁共振氢谱有面积比为3:1的两种峰,则K的结构简式为:__________;另一种异构体H含有醛基、羟基和碳碳双键,在铜催化下氧化,官能团种类会减少一种,则H合理的结构共有___种(不考虑立体异构和空间异构)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com