
| A.加热后,HAc的电离程度减小 |
| B.加水稀释后,溶液的酸性增强 |
| C.加入NaAc固体后,HAc的电离程度减小 |
| D.加入少量并醋酸后,溶液的酸性减弱 |
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.为了减缓反应速率,但又不影响生成H2的总量,可向该溶液中加入少量CaCO3固体 |
| B.为了减缓反应速率,但又不影响生成H2的总量,可向该溶液中加入10 mL 0.1 mol/L醋酸溶液 |
| C.为了减缓反应速率,但又不影响生成H2的总量,可向该溶液中加入少量NaNO3溶液 |
| D.若向该溶液中加入少量醋酸钠固体,反应速率可能变成v(H2)="0.3" mol/(L·h) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
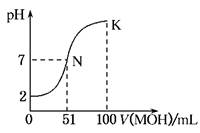
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入适量的氯化铵晶体后,两溶液的pH均碱小 |
| B.温度下降10oC,两溶液的pH均不变 |
| C.分别加水稀释10倍,两溶液的pH仍相等 |
| D.用盐酸中和,消耗的盐酸体积相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.H2S 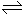 2H+ + S2- 2H+ + S2- | B.HF = H+ + F- |
| C.NaHSO3 = Na+ + H+ +SO32- | D.H2CO3+ H2O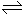 H3O+ + HCO3- H3O+ + HCO3- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.浓度相同时HA溶液的导电性比强酸弱 |
| B.10 mL 1 mol/L的HA溶液与10 mL 1 mol/L的NaOH溶液恰好完全反应 |
| C.NaA溶液的pH>7 |
| D.0.1 mol/L HA溶液的pH=1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HA一定是强酸 | B.HB一定是强酸 |
| C.NaA溶液的碱性弱于NaB溶液的碱性 | D.反应开始时二者生成H2的速率相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 NH4+ +OH-的平衡,如果使平衡向逆反应方向移动,同时使c(OH-)增大,应加入 ( )
NH4+ +OH-的平衡,如果使平衡向逆反应方向移动,同时使c(OH-)增大,应加入 ( ) | A.氯化铵固体 | B.硫酸 | C.NaOH固体 | D.大量水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.②④ | C.③④ | D.②③[ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com