
【题目】酸雨是大气污染的危害之一,二氧化硫(SO2)的含量是空气质量监测的一个重要指标。某兴趣小组拟用下列装置定量分析空气中SO2的含量:

(1)该组同学查资料得到的反应原理为:SO2与酸性KMnO4溶液反应的离子方程式为5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+,SO2在该反应中是___________(填“氧化剂”或“还原剂”)。
(2)通入空气前应进行的实验操作是___________。
(3)该实验中已经知道的数据有气体流速a L/min、酸性KMnO4溶液的体积b L,其浓度为c mol/L。若从气体通入到紫色恰好褪去,用时5分钟。则此次取样处的空气中二氧化硫含量为____________g/L。(写出计算过程)
科目:高中化学 来源: 题型:
【题目】N2和O2生成NO的反应在密闭容器中进行,下列条件中一定能够加快化学反应速率的是
A.扩大体积
B.体积不变,充入N2
C.扩大体积,充入氦气
D.体积不变,充入氦气,增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种元素的核电荷数都小于18,A元素的原子最外层电子数是1,B元素原子的最外层得到1个电子就达到稳定结构,C元素原子最外层电子数是次外层电子数的3倍,则这三种元素组成的化合物不可能的是( )。
A. A2BC3 B. ABC3 C. ABC4 D. ABC
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 反应 NH3(g) +HCl(g)![]() NH4Cl(s)的 △H<0,△S<0
NH4Cl(s)的 △H<0,△S<0
B. 若在海轮外壳上附着一些钢块,则可以减缓海轮外壳的腐蚀
C. 用pH均为11的氨水和氢氧化钠溶液分别中和等体积、等浓度的盐酸,消耗氨水的体积大
D. H2O与Na2O2反应生成1 mol O2,反应中转移的电子数为4×6. 02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废弃的电池已成为重要的环境污染物,有资料表明一节废弃的镍镉电池可使1 m2面积的耕地失去使用价值,因此废旧电池必须集中回收处理,主要原因是( )
A. 回收其中的电极
B. 利用电池外壳的金属材料
C. 不使电池中渗出的电解液腐蚀其他物品
D. 防止电极中汞、镉、镍和铅等重金属离子对土壤和水源造成污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学 方程式为:Ca(C10)2+CaCl2+2H2S04![]() 2CaS04+2Cl2↑+2H20。设计如下实验装置制取氯气并验证其性质。
2CaS04+2Cl2↑+2H20。设计如下实验装置制取氯气并验证其性质。

(1)该实验中A部分的装置为__________(填写装置的代号)。
(2)欲检查A装置的气密性,首先用弹簧夹夹住装置A、B间橡皮管,然后进行的操作为_________。
(3)实验过程中,装置B中的现象是_______________,装置C中发生反应的离子方程式为______________;
(4)设计一个实验证明装置D中有FeCl3生成(请简述实验:步骤)______________ 。
(5)该实验存在明显的错误,改正的方法为 _______________________。
(6)称取该漂白粉样品ag,研磨后溶解,配制成250 mL溶液,取25 mL加入到锥形瓶中,再加入过量的KI溶液和过量的H2S04溶液,静置。待完全反应后,用0.1 molL-1的 Na2S2O3溶液做标准液滴定反应生成的碘,已知反应式为:2Na2S2O3+I2=Na2S4O6+2NaI,共用去Na2S203溶液b mL0则该漂白粉中Ca(ClO)2的质量分数为__________。(用含ab的表达式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以白云石(化学式表示为MgCO3·CaCO3)为原料制备氢氧化镁的工艺流程如下:
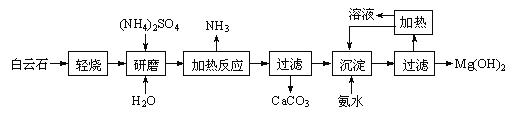
已知:①白云石加热过程中,固体失重百分比与温度的关系如下图所示:

② Ksp[Mg(OH)2]=5.61×10-12。
(1)根据流程图判断白云石“轻烧”后固体产物的主要成份 _____(填化学式)。结合上图判断“轻烧”温度应不超过 _____。
(2)“加热反应”的化学方程式为_________________________。
(3)沉淀过程溶液的pH=9.5,此时溶液中c(Mg2+)= _______(已知)。
(4)该工艺中可以循环使用的物质是________(填化学式)。
(5)传统工艺将白云石分解为氧化镁和氧化钙后提取,从环境保护的用度分析,该工艺采用轻烧白云石的方法,其优点是__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com