
【题目】氨甲环酸(G)别名止血环酸,是一种已被广泛使用半个世纪的止血药,它的一种合成路线如下(部分反应条件和试剂略):
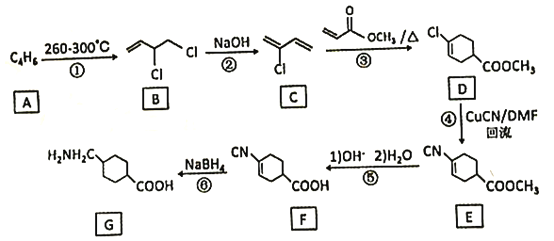
回答下列问题:
(1)A的结构简式是____。C的化学名称是_______。
(2)G在NaOH催化下发生双分子脱水形成仅含两个环的有机物,写出该反应的化学反应方程式____。
(3)①~⑥中属于取代反应的是_________。
(4)E中不含N原子的官能团名称为___________。
(5)氨甲环酸(G)的分子式为__________。
(6)满足以下条件的所有E的同分异构体有_____种。
a.含苯环 b.含硝基 c.苯环上只有两个取代基
(7)写出以![]() 和CH2=CHCOOCH2CH3为原料,制备
和CH2=CHCOOCH2CH3为原料,制备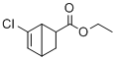 的合成路线:_______(无机试剂任性)
的合成路线:_______(无机试剂任性)
【答案】CH2=CHCH=CH2 2-氯-1,3-丁二烯 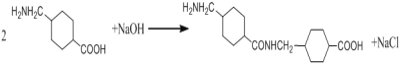 ④⑤ 酯基、碳碳双键 C8H15O2N 15
④⑤ 酯基、碳碳双键 C8H15O2N 15 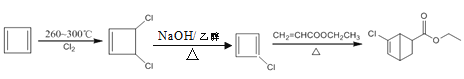
【解析】
根据A分子式及B结构简式知,A为CH2=CHCH=CH2,A→B的反应为加成反应;B发生消去反应生成C,C发生加成反应生成D,D发生取代反应生成E,E发生水解反应生成F,F发生还原反应生成G。
(7)以![]() 和为CH2=CHCOOCH2CH3原料制备
和为CH2=CHCOOCH2CH3原料制备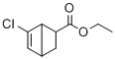 ,
,![]() 先发生加成反应生成
先发生加成反应生成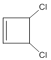 ,然后
,然后 发生消去反应生成
发生消去反应生成 ,
, 再与CH2=CHCOOCH2CH3发生加成反应生成目标产物。
再与CH2=CHCOOCH2CH3发生加成反应生成目标产物。
(1)根据A的分子式及A与Cl2在260—300℃时发生加成反应产生B,根据B的结构简式可知A结构简式是CH2=CHCH=CH2;C的结构简式是![]() ,选择含有2个碳碳双键在内的碳链为主链,把-Cl原子作取代基,给机物命名,可知C的化学名称是2-氯-1,3-丁二烯;
,选择含有2个碳碳双键在内的碳链为主链,把-Cl原子作取代基,给机物命名,可知C的化学名称是2-氯-1,3-丁二烯;
(2)G结构简式是 ,G分子中含有-COOH和-NH2,在NaOH催化下发生分子之间的取代反应,一个分子的羧基脱去-OH,另一个分子的氨基脱去H原子,羟基与氢原子结合形成H2O,剩余部分结合在一起形成含两个环的有机物
,G分子中含有-COOH和-NH2,在NaOH催化下发生分子之间的取代反应,一个分子的羧基脱去-OH,另一个分子的氨基脱去H原子,羟基与氢原子结合形成H2O,剩余部分结合在一起形成含两个环的有机物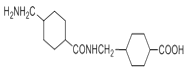 ,则该反应的化学反应方程式为:
,则该反应的化学反应方程式为: 。
。
(3)在上述反应中,①是加成反应,②是消去反应,③是加成反应,④是取代反应,⑤是酯的水解反应,也属于取代反应,⑥是还原反应,所以①~⑥中属于取代反应的是④⑤;
(4)E结构简式是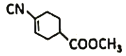 ,E中不含N原子的官能团名称为是酯基和碳碳双键;
,E中不含N原子的官能团名称为是酯基和碳碳双键;
(5)氨甲环酸(G)的结构简式是 ,根据C原子价电子数目是4个,知G分子式为C8H15NO2;
,根据C原子价电子数目是4个,知G分子式为C8H15NO2;
(6)E是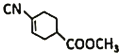 ,E的分子式是C9H11O2N,E的同分异构体符合下列条件:
,E的分子式是C9H11O2N,E的同分异构体符合下列条件:
a.E的不饱和度是5,E的同分异构体中含有苯环,苯环的不饱和度是4,说明含有一个双键;
b.分子含有硝基;c. 苯环上只有两个取代基,符合条件两个取代基可能为-NO2、-CH2CH2CH3;-NO2、-CH(CH3) 2;-CH3、-CH2CH2NO2;-CH3、-CHNO2CH3;-CH2NO2、-CH2CH3五种情况,两个取代基在苯环上的位置有邻、间、对三种位置,所以E的符合要求的同分异构体的种类是5×3=15种;
(7)以![]() 和为CH2=CHCOOCH2CH3原料制备
和为CH2=CHCOOCH2CH3原料制备 ,首先是
,首先是![]() 与Cl2按1:1发生1,2-加成反应生成
与Cl2按1:1发生1,2-加成反应生成 ,然后
,然后 与NaOH的乙醇溶液共热,发生消去反应生成
与NaOH的乙醇溶液共热,发生消去反应生成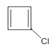 ,
, 再与CH2=CHCOOCH2CH3发生加成反应生成
再与CH2=CHCOOCH2CH3发生加成反应生成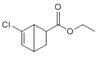 ,故合成路线为:
,故合成路线为: 。
。


 全能测控期末小状元系列答案
全能测控期末小状元系列答案 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
I.CO 还原NO 的脱硝反应:2CO(g)+2NO(g) 2CO2(g)+N2(g) △H
(1)已知:CO(g)+NO2(g) CO2(g)+NO(g) △H1=-226 kJ·mol-1
N2(g)+2O2(g) 2NO2(g) △H2=+68 kJ·mol-1
N2(g)+O2(g) 2NO(g) △H3=+183 kJ·mol-1
脱硝反应△H=__________,有利于提高NO 平衡转化率的条件是________________(写出两条)。
(2)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。某研究小组在实验室以Ag-ZSM-5为催化剂,对CO、NO催化转化进行研究,测得NO转化为N2的转化率随温度、CO混存量的变化情况如下图所示,

①若不使用CO,温度超过775℃,发现NO的分解率降低,其可能的原因为_________________;在n(NO)/n(CO)=1的条件下,应控制最佳温度在____________左右。
②用CxHy(烃)催化还原NOx也可消除氮氧化物的污染,写出C2H6与NO2发生反应的化学方程式:_________。
③NO2尾气常用NaOH溶液吸收,生成NaNO3和NaNO2。已知NO2-的水解常数K=2×10-11,常温下某NaNO2和HNO2混合溶液的pH为5,则混合溶液中c(NO2-)和c(HNO2)的比值为__________。
II.T ℃时,在刚性反应器中发生如下反应:CO(g)+NO2(g) CO2(g)+NO(g),化学反应速率v =k Pm(CO)Pn(NO2),k 为化学反应速率常数。研究表明,该温度下反应物的分压与化学反应速率的关系如下表所示:

(3)若反应初始时P(CO)=P(NO2)=a kPa,反应t min时达到平衡,测得体系中P(NO)=b kPa,则此时v =___________ kPa·s-1(用含有a和b的代数式表示,下同),该反应的化学平衡常数Kp=_____(Kp是以分压表示的平衡常数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向稀硫酸和稀硝酸的混合溶液200 mL中逐渐加入铁粉,产生气体的量随铁粉质量的变化如图所示(已知硝酸只被还原为NO气体)。下列分析错误的是( )
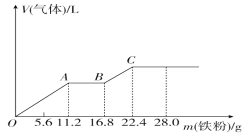
A.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生H2
B.A点溶液中的溶质为Fe(NO3)3和H2SO4
C.原混合酸中NO3-物质的量为0.2 mol
D.原混合酸中H2SO4的物质的量浓度为2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体,经历了下列过程(已知 Fe3+在 pH=5时沉淀完全).其中分析错误的是
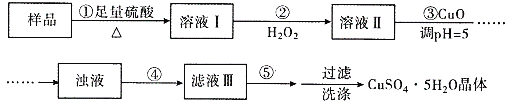
A. 步骤②发生的主要反应为:2Fe2++H2O2+2H+=2Fe3++2H2O
B. 步骤②不能用氯水、硝酸等强氧化剂代替H2O2
C. 步骤④为过滤,步骤⑤蒸发结晶
D. 步骤③用 CuCO3代替CuO也可调节溶液的pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取溴的工业流程如图:

(1)步骤I中将卤水酸化,再通入Cl2,是为了防止Cl2与碱反应,写出Cl2与碱反应的离子方程式_____。
(2)步骤I中已获得游离态的溴,步骤II又将之转变成化合态的溴,其目的是__________。
(3)实验室保存液溴时,通常在盛液溴的试剂瓶中加少量的水,这与液溴的_____性质有关(填写序号)。
A.氧化性 B.还原性 C.挥发性 D.密度比水大
(4)步骤II中将吹出的溴蒸汽用纯碱溶液吸收时还有CO2生成,写出吸收时发生反应的离子方程式:___。
(5)步骤II中通入热空气吹出的Br2用纯碱溶液吸收前先经过NaBr溶液,其目的是______________。
(6)步骤III中蒸馏出工业溴后残留液的主要溶质是_______________。
(7)步骤III中若使用硝酸酸化,缺点是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成药物异搏定路线中某一步骤如下:

下列说法正确的是( )
A. 物质X在空气中不易被氧化
B. 物质Z的分子式为C13H14O3
C. 物质Y可以发生取代、加成、消去反应
D. 等物质的量的Y、Z分别与NaOH溶液反应,最多消耗NaOH的物质的量之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炔烃的偶联反应在开发新型发光材料、超分子等领域有重要研究价值。乙炔发生的偶联反应为 2CH≡CH ![]() CH≡CC≡CH+H2。乙炔偶联反应过程中能量变化如图甲中曲线Ⅰ所示,曲线Ⅱ为改变某一条件的能量变化。下列说法不正确的是( )
CH≡CC≡CH+H2。乙炔偶联反应过程中能量变化如图甲中曲线Ⅰ所示,曲线Ⅱ为改变某一条件的能量变化。下列说法不正确的是( )
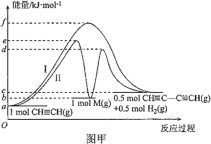
A.曲线Ⅰ,反应物的总键能大于生成物的总键能
B.曲线Ⅱ改变的条件是加入了催化剂
C.曲线Ⅱ对应条件下,第一步反应的 ΔH=+(b-a)kJ·mol-1
D.曲线Ⅱ对应条件下,决定总反应速率的大小是第二步反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯噁洛芬是一种消炎镇痛药,可用于治疗风湿性关节炎、类风湿性关节炎及其它炎性疾病。某研究小组按下列路线合成药物苯噁洛芬:
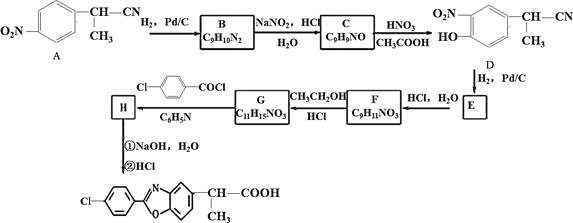
已知:
![]()
![]()
(1)化合物F 中的含氧官能团的名称为_____。
(2)下列说法正确的是_____。
A.化合物A 能发生取代反应、加成反应、还原反应
B.化合物 F 可以形成内盐
C.化合物 C 遇到 FeCl3 显紫色,可以和甲醛在一定条件下发生缩聚反应
D 苯噁洛芬的分子式是C16H11O3NCl
(3)化合物C 的结构简式_____。
(4)写出G→H 的化学方程式_____。
(5)写出化合物B 同时符合下列条件的同分异构体的结构简式_____。
①核磁共振氢谱表明分子中有 4 种氢原子;
②红外光谱显示有苯环且其含有邻位二取代的五元环,并有N-H 键。
(6)请设计由苯和乙烯为原料制备化合物A 的合成路线(用流程图表示,无机试剂任选)。___________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D是1~18号元素中的四种,0.5molA元素的离子得到6.02×1023个电子被还原为中性原子,0.4g A的氧化物恰好与100mL0.2mol/L的盐酸完全反应,A原子核内质子数与中子数相等。B是地壳中含量最多的金属元素。C得到一个电子后与氩的电子层结构相同,其最高价氧化物的水化物为自然界最强的含氧酸。D元素是构成有机物的主要元素,其最内层电子数是最外层电子数的一半。
(1)A的单质可在D的最高价氧化物中燃烧得到一种白色固体和一种黑色固体,试写出其化学方程式______________________________。
(2)A、B、C的离子半径由大到小顺序为:______________。(用离子符号表示)
(3)向10mL浓度为1mol/L的B、C两元素形成的化合物的水溶液里逐滴滴入35mL浓度为1mol/L的苛性钠溶液,现象是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com