
����Ŀ��ʵ�����ú������ʣ�FeO��Fe2O3���ķ�CuO�Ʊ��������壬���������й��̣���֪ Fe3+�� pH=5ʱ������ȫ�������з����������
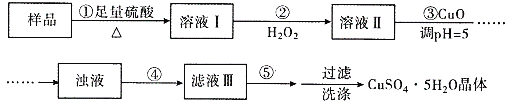
A. ����ڷ�������Ҫ��ӦΪ��2Fe2++H2O2+2H+=2Fe3++2H2O
B. ����ڲ�������ˮ�������ǿ����������H2O2
C. �����Ϊ���ˣ�����������ᾧ
D. ������� CuCO3����CuOҲ�ɵ�����Һ��pH
���𰸡�C
��������
A. �����Ϊ������������������������ԭ��Ӧ�����ӷ�ӦΪ2Fe2++H2O2+2H+=2Fe3++2H2O����A��ȷ��
B. �����������ˮ�������ǿ����������H2O2���������������ӡ���������ӵȣ����Գ�ȥ��ͬʱ������NO���壬���Բ���ڲ�������ˮ�������ǿ����������H2O2����B��ȷ��
C. �����Ϊ���ˣ�����ͭ��Һ������ͭ���岽��Ӧ��Ϊ����Ũ������ȴ�ᾧ�����������ᾧ�����Բ���������ᾧ����C����
D. CuCO3��CuO������Һ��H+��Ӧ��������ҺpH�����ã����������µ����ʣ���D��ȷ��


 ͬ����ϰ���ϴ�ѧ������ϵ�д�
ͬ����ϰ���ϴ�ѧ������ϵ�д� ͬ����ϰ���ϴ�ѧ������ϵ�д�
ͬ����ϰ���ϴ�ѧ������ϵ�д� ����ϰ�⽭��ϵ�д�
����ϰ�⽭��ϵ�д� ѧ���쳵��������������������ϵ�д�
ѧ���쳵��������������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ǵ�ƹ�ҵ�ز����ٵĻ���ԭ�ϡ��Ӳ���ַ���(��Ҫ��Fe 42.35%��Cr 9.67%��Ni 5.1%��C 4.7%��Si 3.39%��)����ȡ����������Ĺ����������£�

��֪����Cr3+�백ˮ��Ӧʱ������Cr3+����[Cr(NH3)6]3+��������ʱ��������ֽ⡣Ni2+�백ˮ��Ӧ����[Ni(NH3)6]2+������������ʱ�ȶ����������ữʱ������Ӧ�������Ρ�
��Na2CrO4��Һ�м������pHΪ3.5ʱ��CrO42��ת��ΪCr2O72����
����������ڲ�ͬ�¶�ʱ�ܽ�����±���
�¶��ܽ��/g���� | 20�� | 30�� | 40�� | 60�� | 80�� | 90�� |
Na2SO4 | 19.5 | 40.8 | 48.8 | 45.3 | 43.7 | 42.7 |
Na2Cr2O7 | 183 | 198 | 215 | 269 | 376 | 405 |
(1)���������õ�����Һ����Ҫ����FeSO4��NiSO4��Cr2(SO4)3������NiSO4�Ļ�ѧ����ʽΪ_____���������ʱ������¶�Ϊ90�����ң����Բ��õļ��ȷ�ʽ��_____��
(2)��������ǰ���ʵ����ȵ�Ŀ����_____��
(3)�������������õ���������ϴ�ӣ�����������ϴ�Ӹɾ��ķ�����_____��
(4)��������ʱ�����������������Ʊ�Na2Cr2O7���塣
���������������Na2CO3����ڿ�������������Na2CrO4��CO2���˷�Ӧ�Ļ�ѧ����ʽΪ_____��
���벹�������������պ������Ʊ�Na2Cr2O7����(�Ⱥ�ɫ)��ʵ�鷽����ˮ�������ˣ�_____����Na2Cr2O7����(����ʹ�õ��Լ��У����ᣬ����ˮ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D��E����Ԫ�ء��������Ϣ���£�
Ԫ�� | �����Ϣ |
A | Aԭ�ӵ�1s�����ֻ��1������ |
B | B�ǵ縺������Ԫ�� |
C | C�Ļ�̬ԭ��2p�����������δ�ɶԵ��� |
D | D������Ԫ������Eͬ���ڣ��������ܲ����������˶�״̬��ͬ�ĵ��� |
E | E���γɺ�ɫ(��ש��ɫ)��E2O�ͺ�ɫ��EO���������� |
��ش��������⣺
(1)д��EԪ��ԭ�ӻ�̬ʱ�ĵ����Ų�ʽ_______��
(2)CԪ�صĵ�һ�����ܱ���Ԫ�صĵ�һ������_____(������������С��)��
(3)CA3������Cԭ�ӵ��ӻ����������______��CA3���ӵĿռ乹����_____��
(5)A��C��E����Ԫ�ؿ��γ�[E(CA3)4]2�������ӣ����д��ڵĻ�ѧ��������________(�����)��
����λ�� �ڽ����� �ۼ��Թ��ۼ� �ܷǼ��Թ��ۼ� �����Ӽ� �����
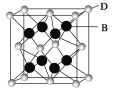
(5)B��D���γ����ӻ�����侧���ṹ��ͼ��ʾ������D���ӵ���λ��Ϊ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ӱ�����ǵ������뽡����ij�����������п��ܺ������¿����������ӣ�Na+��NH4+��Mg2+��Al3+��SO42����NO3����Cl�� ��ijͬѧ�ռ��˸õ���������������Ҫ��Ԥ������������Һ����Ʋ���������µ�ʵ�飺
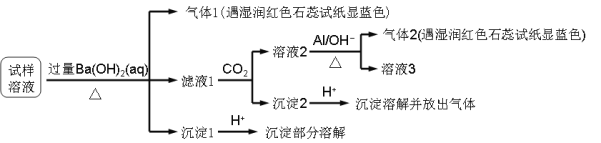
��֪��3NO3��+ 8Al + 5OH�� + 2H2O![]() 3NH3 + 8AlO2��
3NH3 + 8AlO2��
�������ϵ�ʵ�����������ͬѧ�ó��Ľ�������ȷ����
�����п϶�����NH4+��Mg2+��SO42����NO3��
������һ������Al3+
�����п��ܴ���Na+��Cl��
�������п��ܴ���NaNO3 ��NH4Cl��MgSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��W��Ϊ��ѧ�����Ĵ��������֮��������ת����ϵ(�������P��Ӧ��������ȥ����Ӧ������ˮ��Һ�н���)![]() ��A
��A![]() B
B![]() C��
C��
����AΪ�д̼�����ζ�����壬ˮ��Һ�ʼ��ԣ�CΪ����ɫ���壬��ˮ��Ӧ����һԪǿ��D��D����ǿ�����ԡ�
(1)�ڴ��������£�A��C��Ӧ��������������Ⱦ���ʣ��÷�Ӧ��ѧ����ʽΪ_______��
(2)��ҵ�ϳ��ù�����Na2CO3��Һ����C�����ɵ����ʵ��������������Σ��÷�Ӧ�����ӷ���ʽΪ___��
����A��C��W���dz������壬C�ǵ����������Ҫ���壬������A��C��Ӧ����B����÷�Ӧ�Ļ�ѧ����ʽΪ_____��
ij��ѧ�С�齫�Ѽ�����һ���������걣�����ܱ������У�ÿ��һ��ʱ��������pH����������ʼһ��ʱ���ڣ������pH�ʼ�С���ƣ������ӷ���ʽ����ԭ��________��
��A��B��C�������ʵ���Һ���Լ��ԣ���ɫ��Ӧ��Ϊ��ɫ��C����������ķ��ݼ������ȷֽ������B��������״����2.24L��Wͨ��150mL1 molL-1 ��A��Һ�У���ַ�Ӧ���ܷ�Ӧ�����ӷ���ʽΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ȼ���������ýȾ����������ͼ��ʾװ�ÿ����Ʊ����Ȼ���(���ּг�װ����ȥ)��
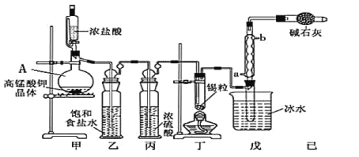
�й���Ϣ���±�

�ش��������⣺
(1)��װ��������A������Ϊ_________��
(2)�ü�װ����������MnO4-����ԭΪMn2+���÷�Ӧ�����ӷ���ʽΪ_____________��
(3)��װ����ͼ���Ӻã���������ԣ���������Ũ���ᣬ���۲쵽______��������ʼ���ȶ�װ�ã����ۻ����ʵ����������������������ȶ�װ�ã���ʱ�������ȶ�װ�õ�Ŀ���ǣ� �ٴٽ�����������Ӧ�� ��_________��
(4)��װ�õ����� __________�����ȱ����װ�ã����ܷ����ĸ���Ӧ�Ļ�ѧ����ʽΪ___________����װ�õ�������__________������ţ�
A.��ֹ������CO2���������װ��
B.��ȥδ��Ӧ����������ֹ��Ⱦ����
C.��ֹˮ����������װ�õ��Թ���ʹ����ˮ��
D.��ֹ������O2������װ�õ��Թ���ʹ��������
(5)��Ӧ����ȥ����1.19g����Ӧ������װ�õ��Թ����ռ���2.04g SnCl4����SnCl4�IJ���Ϊ________��������2λ��Ч���֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(G)����ֹѪ���ᣬ��һ���ѱ��㷺ʹ�ð�����͵�ֹѪҩ������һ�ֺϳ�·�����£����ַ�Ӧ�������Լ��ԣ���
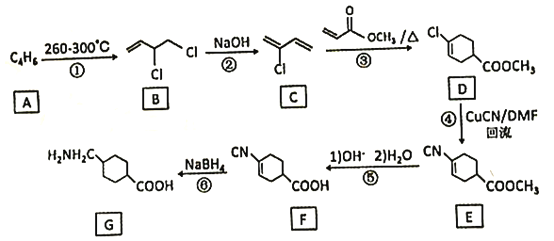
�ش��������⣺
(1)A�Ľṹ��ʽ��____��C�Ļ�ѧ������_______��
(2)G��NaOH���·���˫������ˮ�γɽ������������л��д���÷�Ӧ�Ļ�ѧ��Ӧ����ʽ____��
(3)��~��������ȡ����Ӧ����_________��
(4)E�в���Nԭ�ӵĹ���������Ϊ___________��
(5)������(G)�ķ���ʽΪ__________��
(6)������������������E��ͬ���칹����_____�֡�
a.������ b.������ c.������ֻ������ȡ����
(7)д����![]() ��CH2=CHCOOCH2CH3Ϊԭ�ϣ��Ʊ�
��CH2=CHCOOCH2CH3Ϊԭ�ϣ��Ʊ�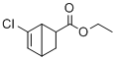 �ĺϳ�·�ߣ�_______�����Լ����ԣ�
�ĺϳ�·�ߣ�_______�����Լ����ԣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʯ���ܵõ������л������������ʵ�ת����ϵ����ͼ��ʾ������A�IJ����Ǻ���һ������ʯ�ͻ�����չˮƽ����Ҫ��־������£�B������ܶ�Ϊ0.71gL-1��C��һ�ֺ�ɫ���嵥�ʣ�D��һ�ֻ�����塣
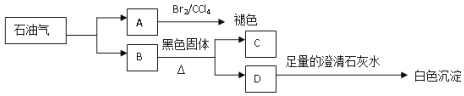
��ش�
��1��A�Ľṹ��ʽΪ__��A��������Ȼ�̼��Һ�ķ�Ӧ����Ϊ___��
��2��B��CuO��Ӧ�Ļ�ѧ����ʽ___��
��3������˵������ȷ��__��
a.A������ԭ�ӹ�ƽ��
b.A��������Ȼ�̼��Һ��Ӧ����A����ˮ��Ӧ��������ȫ��ͬ
c.�����ʵ���A��B�������������������ȫȼ�գ�����ˮ�����ʵ������
d.B����������ЧӦ������֮һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɷ�ɹ˪����Ҫ�ɷ�E��һ��·��ͼ���£�
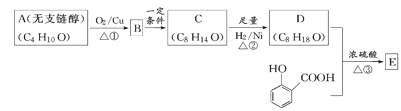
��֪:2RCH2CHO![]()
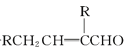
�밴Ҫ��ش��������⣺
(1)D�Ĺ����Žṹ��ʽΪ____________________
(2)��Ӧ�۵ķ�Ӧ����Ϊ__________��
(3)��Ӧ�ٵĻ�ѧ����ʽ��____________________
(4)E�Ľṹ��ʽ��____________________��
(5)A��ͬ���칹���ж��֣�д�����к˴Ź����������շ����֮��Ϊ1��9�Ľṹ��ʽ��_________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com