
【题目】某酸的酸式盐NaHY在水溶液中,HY-的电离程度小于HY-的水解程度。有关的叙述正确的是
A. H2Y的电离方程式为:H2Y+2H2O![]() 2H3O++Y2-
2H3O++Y2-
B. 在该酸式盐溶液中c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+)
C. HY-的水解方程式为HY-+H2O![]() H3O++Y2-
H3O++Y2-
D. 在该酸式盐溶液中c(Na+)>c(HY-)>c(OH-)>c(H+)
【答案】D
【解析】A.H2Y是二元弱酸,电离时分两步电离,第一步电离生成氢离子和酸式酸根离子,电离方程式为:H2Y+H2O![]() H3O++HY-,A错误;B.NaHY的水溶液中,阴离子水解,钠离子不水解,所以c(Na+)>c(HY-);HY-的电离程度小于HY-的水解程度,但无论电离还是水解都较弱,阴离子还是以HY-为主,溶液呈碱性,说明溶液中c(OH-)>c(H+);因溶液中还存在水的电离,则c(H+)>c(Y2-),所以离子浓度大小顺序为:c(Na+)>c(HY-)>c(OH-)>c(H+)>c(Y2-),B错误;C.HY-水解生成二元弱酸和氢氧根离子,水解方程式为:HY-+H2OOH-+H2Y,选项中是电离方程式,C错误;D.根据B的分析可知:c(Na+)>c(HY-)>c(OH-)>c(H+),D正确;答案选D。
H3O++HY-,A错误;B.NaHY的水溶液中,阴离子水解,钠离子不水解,所以c(Na+)>c(HY-);HY-的电离程度小于HY-的水解程度,但无论电离还是水解都较弱,阴离子还是以HY-为主,溶液呈碱性,说明溶液中c(OH-)>c(H+);因溶液中还存在水的电离,则c(H+)>c(Y2-),所以离子浓度大小顺序为:c(Na+)>c(HY-)>c(OH-)>c(H+)>c(Y2-),B错误;C.HY-水解生成二元弱酸和氢氧根离子,水解方程式为:HY-+H2OOH-+H2Y,选项中是电离方程式,C错误;D.根据B的分析可知:c(Na+)>c(HY-)>c(OH-)>c(H+),D正确;答案选D。


科目:高中化学 来源: 题型:
【题目】下列为四个常用的电化学装置,关于它们的叙述正确的是
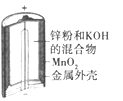
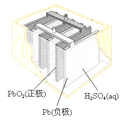
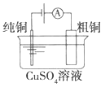
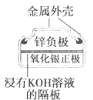
(a)碱性锌锰电池 (b)铅硫酸蓄电池 (c)电解精炼铜 (d)银锌纽扣电池
A.图(a)所示电池中,MnO2的作用是催化剂
B.图(b)所示电池放电过程中,硫酸浓度不断增大
C.图(c)所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D.图(d)所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄樟脑(结构简式如下图)可作为洋茉莉和香兰素的原料,能除肥皂的油脂臭,常作廉价的香料使用于皂用香精中。下列有关叙述正确的是

A. 黄樟脑属于酯、烯烃、芳香族化合物
B. 黄樟脑分子中最少有9个碳原子共面
C. 黄樟脑与H2、Br2均能发生加成反应
D. 与黄樟脑互为同分异构体且含苯环、羧基及一个支链的结构有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,改变反应物用量或浓度,不会改变反应产物的是( )
A. 铁在硫蒸气中燃烧 B. SO2通入石灰水
C. 氯气通入KI溶液 D. H2SO4中加入铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫一钠原电池具有输出功率较高、循环寿命长等优点。其工作原理可表示为:![]() 。但工作温度过高是这种高性能电池的缺陷。科学家研究发现,采用多硫化合物[如
。但工作温度过高是这种高性能电池的缺陷。科学家研究发现,采用多硫化合物[如 ]作为电极反应材料,可有效地降低电池的工作温度,且原材料价廉、低毒,具有生物降解性。下列关于此种多硫化合物的叙述正确的是
]作为电极反应材料,可有效地降低电池的工作温度,且原材料价廉、低毒,具有生物降解性。下列关于此种多硫化合物的叙述正确的是
A. 这是一种新型无机非金属材料 B. 此化合物可能发生加成反应
C. 原电池的负极反应将是单体![]() 转化为
转化为 t的过程 D. 当电路中转移0.02mol电子时,将消耗原电池的正极反应材料1.48g
t的过程 D. 当电路中转移0.02mol电子时,将消耗原电池的正极反应材料1.48g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷为VA族元素,金属冶炼过程产生的含砷有毒废弃物需处理与检测。
Ⅰ.冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如下:

已知:①As2S3与过量的S2存在以下反应:As2S3(s)+3S2(aq)![]() 2
2![]() (aq);
(aq);
②亚砷酸盐的溶解性大于相应砷酸盐。
(1)亚砷酸中砷元素的化合价为________;砷酸的第一步电离方程式为_______________________。
(2)“一级沉砷”中FeSO4的作用是_____________________;“二级沉砷”中H2O2与含砷物质反应的化学方程式为_______________________。
(3)沉淀X为___________(填化学式)。
Ⅱ.冶炼废渣中的砷元素主要以As2S3的形式存在,可用古氏试砷法半定量检测(As的最低检出限为3.0×106 g)。
步骤1:取10 g废渣样品,粉碎后与锌粉混合,加入H2SO4共热,生成AsH3气体。
步骤2:将AsH3气体通入AgNO3溶液中,生成银镜和As2O3。
步骤3:取1 g废渣样品,重复上述实验,未见银镜生成。
(4)AsH3的电子式为_______________。
(5)步骤2的离子方程式为___________________________。
(6)固体废弃物的排放标准中,砷元素不得高于4.0×105 g·kg1,请通过计算说明该排放的废渣中砷元素的含量_______(填“符合”、“不符合”)排放标准,原因是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液可能含有Na+、Ba2+、Al3+、Fe3+、Br-、CO32-等离子,取少量溶液往其中滴加氯水,有无色无味气体产生,溶液仍为无色;另取少量逐滴滴入NaOH 溶液至过量,无现象。关于该溶液的推测正确的是
A. 溶液中可能存在A13+ B. 溶液中可能存在Br-
C. 溶液中一定存在CO32- D. 溶液中可能存在Ba2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com