
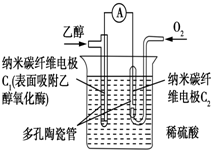
| A�� | C1��Ϊ��ظ�����C2��Ϊ������� | |
| B�� | ��Һ�е�H+��C1�缫�ƶ� | |
| C�� | ������ȼ�ϵ�ص��ܷ�Ӧ����ʽΪC2H5OH+3O2�T2CO2+3H2O | |
| D�� | ������C2�������·����C1�� |
���� �Ҵ�ȼ�ϵ���У��������Һ�����ԣ��Ҵ��ڸ����ϱ��������缫��ӦΪC2H5OH+3H2O-12e-=2CO2+12H+�������������ϵõ��ӱ���ԭ���缫��ӦʽΪO2+4H++4e-=2H2O���ܷ�ӦΪC2H5OH+3O2=2CO2+3H2O��ԭ����У������ɸ��������·����������
��� �⣺A��C1��ͨȼ�ϵ�һ��Ϊ������ͨ������һ��C2��Ϊ��Դ����������A��ȷ��
B��ԭ������������������ƶ���������Һ�е�H+��C1�缫�ƶ�����B����
C������������Ӧʽ��ӿɵ��ܷ�Ӧʽ�����Ҵ�ȼ�յĻ�ѧ����ʽ��ͬ��ΪC2H5OH+3O2=2CO2+3H2O����C��ȷ��
D��ԭ����У������ɸ��������·���������������е�����C1�������·��������C2�������Ե�����C2�������·����C1������D��ȷ��
��ѡB��
���� ���⿼�黯ѧ��Դ���͵�أ������ѶȲ���ע��缫��Ӧʽ����д���Դ��жϸ��缫�ı仯��


 ��ĩ��ϰ���ϵ�д�
��ĩ��ϰ���ϵ�д� ����ѧ�䵥Ԫ������ĩר����100��ϵ�д�
����ѧ�䵥Ԫ������ĩר����100��ϵ�д� �Ƹ�360�ȶ����ܾ�ϵ�д�
�Ƹ�360�ȶ����ܾ�ϵ�д� ���⿼����Ԫ���Ծ�ϵ�д�
���⿼����Ԫ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��������3��4-�������飮
��������3��4-�������飮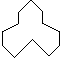 �����ǻ�ʮ���飬1mol������ȫȼ�գ�����������18mol��
�����ǻ�ʮ���飬1mol������ȫȼ�գ�����������18mol�� ������3-��-4-�һ�-3-��ϩ
������3-��-4-�һ�-3-��ϩ ������2��2��3-��������
������2��2��3-���������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| X | Y | Z | |
| �� | NaOH��Һ | Al��OH��3 | ϡ���� |
| �� | KOH��Һ | SiO2 | ����� |
| �� | O2 | N2 | H2 |
| �� | FeC13��Һ | Cu | Ũ���� |
| A�� | �٢ۢ� | B�� | �٢ڢ� | C�� | �ڢ� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Һ�У�Mg2+��Fe3+��SO42-��Cl- | |
| B�� | ������Һ�У�NH4+��Na+��ClO-��SO42- | |
| C�� | ����Һ�У�MnO4-��K+��Na+��NO3- | |
| D�� | ����KSCN��Һ�Ժ�ɫ����Һ�У�Na+��K+��SO42-��OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO��SO2��NO2 | B�� | N2��O2��CO2 | C�� | H2��N2��SO2 | D�� | CO��CO2��SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
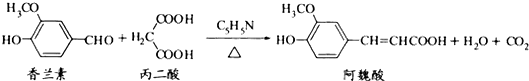
| A�� | �������ػ�Ϊͬ���칹�壬��������5�ֲ�ͬ��ѧ�������⣬���ܷ���������Ӧ�ķ��������2�� | |
| B�� | �����ء���κ�������NaHCO3��NaOH��Һ��Ӧ | |
| C�� | ͨ�������£������ء���κ�ᶼ�ܷ���ȡ�����ӳɡ���ȥ��Ӧ | |
| D�� | �����ء���κ���������ˮ��Ӧ���ҷ�Ӧ������ȫ��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | m+2-a | B�� | n+m+a | C�� | 2n+3m-a | D�� | m+2n+2-a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com