
【题目】X、Y、Z三种气体,取X和Y按1∶1的物质的量之比混合,放入密闭容器中发生如下反应:X+2Y![]() 2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于
2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于
A. 33% B. 40% C. 50% D. 65%
科目:高中化学 来源: 题型:
【题目】在番茄幼苗的培养液中,除了必需的微量元素、NH4+、PO43-和CO2外,还必需的大量元素有()
A. C.H、O、N
B. K、CA.Mg、Fe
C. Mn、Mo、Cu、Zn
D. K、CA.Mg、S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均是短周期主族元素,其原子序数依次增大,A和B同周期,A和D同主族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C的阳离子电子层结构相同,C的单质与B的单质在不同条件下反应,可生成C2B或C2B2,E是所在周期中原子半径最小的元素,请回答:
(1)D在元素周期表中的位置是 。
(2)C2B2的电子式是 ;AB2的结构式是 。
(3)B、C、E的离子半径由大到小的顺序为 (用化学式回答,下同);A、D、E元素最高价氧化物对应水化物的酸性由强到弱为 。
(4)B的气态氢化物与H2S相比沸点高的是 (用化学式回答),原因是 。
(5)水中锰含量超标,容易使洁具和衣物染色,使水产生异味,EB2可以用来除去水中超标的Mn2+,生成黑色沉淀MnO2,当消耗13.50gEB2时,共转移了1mol电子,则反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素 W、X、Y、Z 在元素周期表中的位置如图所示。其中 Z 的单质是一种重要半导体材料,广泛应用于电子工业的各个领域。
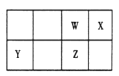
(1)W 在元素周期表中的位置是____________。
(2)W、X、氢元素形成的三原子分子的电子式____________。
(3)下列选项中,能证明元素非金属性X强于W的是____________。
A.相对原子质量:X>W | B.最低化合价:X>W |
C.最简单氢化物的稳定性:X>W | D.最高价氧化物的水化物酸性:X>W |
(4)元素周期表中与 Z 同周期的某金属元素形成的单质 A,可发生如下图所示的转化:
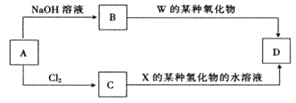
其中化合物D是一种白色沉淀,则 B 中溶质的化学式为____________;
B与 C也可直接转化生成 D 写出对应的离子方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把500 mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含bmol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为 ( )
A. 0.1(b-2a)mol·L-1 B. 10(2a-b) mol·L-1
C. 10(b-2a) mol·L-1 D. 10(b-a) mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物。试回答下列问题:
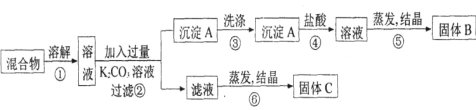
(1) B物质的化学式为 。
(2) 该方案的明显失误是因某一步设计不当而使分离产物不纯,该步骤是 (填序号)如何改进 ,所涉及反应的离子方程式为 。
(3)写出 ② ④ 两步中对应的离子方程式:
② ;
④____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式__________________。
(2)下列三种情况下,离子方程式与(1)相同的是__________(填序号)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
若在A项所得溶液中,继续滴加Ba(OH)2溶液,此步反应的离子方程式为:________________
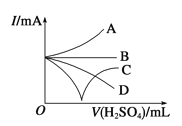
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用右上图中的 曲线表示(填序号)。
(4)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图所示,向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应。在此实验过程中,小球将 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用稀硝酸腐蚀废锌板后得到“烂版液”(含有微量的Cl-、Fe3+),某化学兴趣小组拟用该“烂版液”制取Zn(NO3)2·6H2O的过程如下:
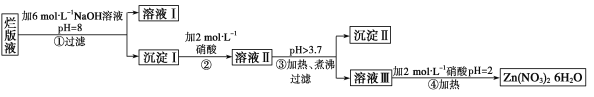
已知: Zn(NO3)2能与碱反应,得到的产物具有两性。
(1)为检验“烂版液”中的Fe3+,下列试剂可选择的是 (填选项的代号)
A、NaOH溶液 B、KSCN溶液 C、K3[Fe(CN)6] 溶液 D、NaCl溶液
(2)若稀硝酸腐蚀锌板产生的气体为N2O,写出稀硝酸腐蚀锌板反应的主要化学方程式_________。
(3)在操作①中保持pH=8的目的是___________;操作④保持pH=2的目的是__________________;
(4)操作③中加热、煮沸的目的是___________________________;
(5)沉淀Ⅱ的主要成分是______________________。
(6)已知金属活泼性不同,其硝酸盐的分解产物也不同。
2KNO3=2KNO2+O2↑ 4Fe(NO3)2=2Fe2O3+8NO2↑+O2↑ 2Zn(NO3)2=2ZnO+4NO2↑+O2↑
某同学取KNO3、Zn(NO3)2、Fe(NO3)2混合粉末充分加热后,用排水法未收集到任何气体,则KNO3、 Zn(NO3)2、Fe(NO3)2的物质的量之比为 (填选项的代号)
A、2︰1︰3 B、1︰2︰2 C、1︰2︰3 D、3︰8︰5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com