
【题目】下列叙述正确的是( )
A. 标准状况下,11.2LSO2气体中含氧原子数等于18g水中含有的氧原子数
B. 5.6 g铁与足量稀硫酸反应失去的电子的物质的最为0.3 mol
C. 100g98%的浓硫酸所含的氧原子个数为4mol
D. 20gNaOH溶于1L水,所得溶液中c(Na+)=0.5mol·L-1
【答案】A
【解析】A.标准状况下,11.2LSO2的物质的量=![]() =0.5mol,含有1mol氧原子,18g水的物质的量=
=0.5mol,含有1mol氧原子,18g水的物质的量=![]() =1mol,也含有1molO原子,故二者含有的氧原子数相等,故A正确;B.Fe与硫酸反应生成硫酸亚铁,硫酸足量,Fe完全反应,5.6gFe的物质的量=
=1mol,也含有1molO原子,故二者含有的氧原子数相等,故A正确;B.Fe与硫酸反应生成硫酸亚铁,硫酸足量,Fe完全反应,5.6gFe的物质的量=![]() =0.1mol,反应中Fe元素化合价由0价升高为+2价,故转移电子物质的量=0.1mol×2=0.2mol,故B错误;C.100g98%的浓硫酸中含有98g硫酸和2g水,其中水中也含有氧原子,故C错误;D.20gNaOH的物质的量=
=0.1mol,反应中Fe元素化合价由0价升高为+2价,故转移电子物质的量=0.1mol×2=0.2mol,故B错误;C.100g98%的浓硫酸中含有98g硫酸和2g水,其中水中也含有氧原子,故C错误;D.20gNaOH的物质的量=![]() =0.5mol,溶于水配成1L溶液,所得溶液中c(Na+)=0.5mol/L,体积1L是指溶液的体积,不是溶剂的体积,故D错误;答案为A。
=0.5mol,溶于水配成1L溶液,所得溶液中c(Na+)=0.5mol/L,体积1L是指溶液的体积,不是溶剂的体积,故D错误;答案为A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】向2 L的密闭容器中加入一定量的A、B、C三种气体,一定条件下发生反应,各物质的物质的量随时间变化如图甲所示。图乙为t2时刻后改变条件平衡体系中反应速率随时间变化的情况,且4个阶段所改变的外界条件均不相同,已知t3——t4阶段为使用催化剂。观察下图,回答下列问题:
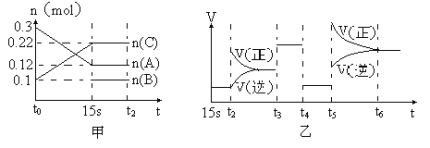
(1)甲图中从反应至达到平衡状态,生成物C的平均反应速率为 。
(2)乙图中t2时引起平衡移动的条件是 ,t5时引起平衡移动的条件是 。
(3)乙图中表示平衡混合物中,在这4个阶段中C的含量最高的一段时间是 。
(4)该反应的化学方程式可以表示为: ,正反应为 (填“放热”或“吸热”)反应。
(5)反应开始时加入的B的物质的量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制铵明矾晶体的工艺流程如图所示:
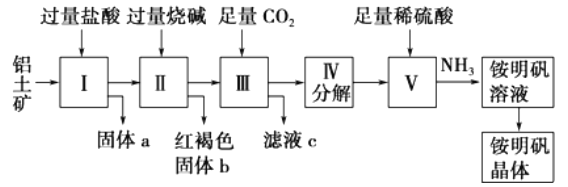
请回答下列问题:
(1)固体a的化学式为____,固体b化学式为____,Ⅲ中通入足量CO2气体发生反应的离子方程式为________________.
(2)由Ⅴ制取铵明矾溶液的化学方程式为______________.
(3)由I→II→III→IV都要用到的分离方法是______,由铵明矾溶液中制铵明矾晶体的操作是______________.
(4)如果先向铝土矿加入过量氢氧化钠,再加入过量盐酸,此时首先出现的固体a是__.
(5)向10gFe2O3、SiO2和Al2O3的混合物中,加入100ml稀硫酸,过滤后,向滤液中加入10mol/L NaOH溶液,产生沉淀的质量和加入NaOH溶液体积的关系曲线如图所示.则混合物中三氧化二铝的质量分数为______.
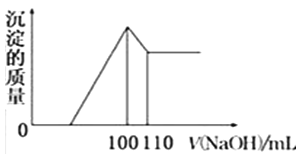
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气脱硝脱碳主要原理为:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g) △H<0。在一定条件下的密闭容器中,用传感器测得该反应在不同时间NO和CO浓度如下表:
N2(g)+2CO2(g) △H<0。在一定条件下的密闭容器中,用传感器测得该反应在不同时间NO和CO浓度如下表:
时间/s | 0 | 1 | 2 | 3 | 4 |
C(NO)/mol L-1 | 9.50×10-3 | 4.50×10-3 | 2.50×10-5 | 1.50×10-3 | 1.5×10-3 |
C(CO)/mol L-1 | 9.00×10-3 | 4.00×10-3 | 2. 00×10-3 | 1.00×10-3 | .1.00×10-3 |
下列说法正确的是
A. —定温度下,从开始到平衡,该反应的平衡常数逐渐增大
B. 前2s内的平均反应速率v(N2) = 1.75×10-3 mol·L-1·s-1
C. 达到平衡时,CO的转化率为11. 11%
D. 3s时NO和CO的浓度都不再变化,反应停止进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色透明溶液,可能含有下列离子:Mg2+、A13+、Fe3+、Ba2+、H+、NH4+、SO42-、HCO3-、Cl-。取该溶液进行如下实验:①取溶液少许,滴入AgNO3溶液产生白色沉淀;②取溶液少许,滴入BaCl2溶液产生白色沉淀,加入足量稀硝酸沉淀不溶解;③取一定量的原溶液,加入一种淡黄色粉末状的固体X,产生气体的物质的量(n气体)、沉淀的物质的量(n沉淀)与加入淡黄色粉末的量(nx)的关系如下图所示(假设生成的气体全部逸出)。

根据实验现象和数据分析正确的是
A. 溶液中肯定大量存在的阳离子只有Mg2+、A13+、NH4+
B. 溶液中肯定没有的离子只有Fe3+、Ba2+
C. 当加入0.6mol淡黄色粉末时,生成两种气体分别为NH3和O2,其对应的体积比为2:3
D. 溶液中可能存在Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药用有机化合物A(C8H8O2)为一种无色液体。从A出发可发生如图所示的一系列反应。

则下列说法正确的是( )
A.根据D和浓溴水反应生成白色沉淀可推知D为三溴苯酚
B.G的同分异构体中属于酯且能发生银镜反应的只有一种
C.上述各物质中能发生水解反应的有A、B、D、G
D.A的结构简式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是

A. 用石墨作阳极,铁作阴极
B. 阳极的电极反应式为:Cl-+ 2OH--2e-= ClO-+ H2O
C. 阴极的电极反应式为:2H2O + 2e-= H2↑ + 2OH-
D. 除去CN-的反应:2CN-+ 5ClO-+ 2H+= N2↑ + 2CO2↑ +5Cl-+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家用氮化镓、铜等材料组装成人工光合系统(如下图),利用该装置成功地实现了以CO2和H2O合成CH4。

(1)写出铜电极表面的电极反应式:_______________________________________________________。
(2)为提高该人工光合系统的工作效率,可向装置中加入少量_________(选填“盐酸”或“硫酸”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】异戊二烯是重要的有机化工原料,其结构简式为 ![]() 。
。
异戊二烯的一种制备方法如图所示:
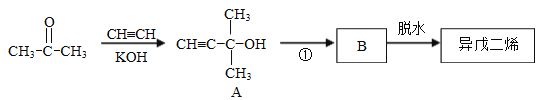
请回答:
(1)A分子中官能团的名称是_______。
(2)①的反应类型是_______。
(3)B的结构简式为___________________________。
(4)写出在一定条件下由异戊二烯制备聚异戊二烯的化学方程式_____________。
(5)设计一条由异戊二烯制得有机合成中间体![]() 的合成路线。
的合成路线。
(合成路线常用的表示方式为:![]() )
)
_____________________________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com