
【题目】有关物质的转化关系如下图所示(部分条件已略去),在通常状况下,B是黑色的金属氧化物,D、E、F是气体单质,C是一种水溶液显碱性的气体,I为红棕色气体,G为紫红色的金属。

(1)B的化学式为__________;A的结构式为___________;
(2)写出反应①的化学方程式:_____________________________;
(3)写出反应②的离子方程式: ___________ ,该反应是________(填“放热”或“吸热”)反应;
(4)实验室制备C时,检验是否收集满C的方法是____________________。
【答案】CuO H-O-H 4NH3+5O2![]() 4NO+6H2O Cu+4H++2NO3﹣=Cu2++2NO2↑+2H2O 放热 用湿润的红色石蕊试纸放在集气瓶口,若试纸变蓝说明氨气收集满(或用玻璃棒蘸取浓盐酸靠近集气瓶口,若产生白烟说明氨气收集满)
4NO+6H2O Cu+4H++2NO3﹣=Cu2++2NO2↑+2H2O 放热 用湿润的红色石蕊试纸放在集气瓶口,若试纸变蓝说明氨气收集满(或用玻璃棒蘸取浓盐酸靠近集气瓶口,若产生白烟说明氨气收集满)
【解析】
在通常状况下,B是黑色的金属氧化物的固体,C、D、E、F、H、I均为气体,C的水溶液显碱性为NH3,G为紫红色的金属单质为Cu,所以B为CuO,NH3与Cu反应产生Cu、N2、H2O,A电解产生D、E、两种单质气体,则A为H2O,D是O2,E是H2、F是N2,NH3与O2反应产生NO和水,则H是NO,I为红棕色为NO2,NO2与H2O反应产生HNO3和H2O,K与Cu反应产生Cu(NO3)2、NO2、H2O,所以J是Cu(NO3)2,据此分析回答。
根据上述分析可知:A是H2O,B是CuO,C是NH3,D是O2,E是H2、F是N2,G是Cu,H是NO,I是NO2,J是Cu(NO3)2,K是HNO3。
(1)根据上述分析可知B的化学式为CuO,A是H2O,结构式是H-O-H;
(2)反应①是氨气的催化氧化反应生成NO和H2O,反应的化学方程式为:4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
(3)反应②是铜和浓硝酸反应生成硝酸铜、二氧化氮和水,反应的离子方程式:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O;该反应发生时会放出大量的热,因此是放热反应;
(4)C是NH3,该气体是碱性气体,实验室制备C时,检验是否收集满C的方法是用湿润的红色石蕊试纸放在集气瓶口,若试纸变蓝说明氨气收集满;也可以用玻璃棒蘸取浓盐酸靠近集气瓶口,若产生白烟说明氨气收集满。


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】以下实验能获得成功的是( )
A.用酸性高锰酸钾溶液鉴别乙烯和乙炔
B.将稀硫酸、稀硝酸和苯混合加热制硝基苯
C.苯和硝基苯混合物采用分液的方法分离
D.用氢氧化钠溶液除去溴苯中含有的杂质溴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学的发展离不开科学家的贡献,下列科学家与贡献不匹配的是( )
A.门捷列夫~元素周期律
B.诺贝尔~硝化甘油
C.汤姆逊~原子结构的行星模型
D.凯库勒~苯的结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】震惊全国的天津港“8.12”爆炸事故中,因爆炸冲击导致氰化钠泄漏而造成环境污染,可以通过喷洒双氧水或硫代硫酸钠溶液来处理。
资料:氰化钠化学式NaCN(N元素-3价),白色结晶颗粒,剧毒,易溶于水
(1)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,写出该反应的化学方程式________________。
(2)某化学兴趣小组实验室制备硫代硫酸钠(Na2S2O3),并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放。
【实验一】实验室通过下图装置制备Na2S2O3。
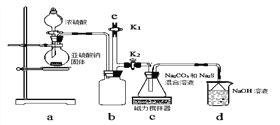
①a装置中盛浓硫酸的仪器名称是_______________;
b装置的作用是________________。
②c装置中的产物有Na2S2O3和CO2等,d装置中的溶质有NaOH、Na2CO3,还可能有___________________。
③实验结束后,在e处最好连接盛_________(选填“NaOH溶液”、“水”、“CCl4”中任一种)的注射器,再关闭K2打开K1,目的是__________________
【实验二】测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。
已知:
① 废水中氰化钠的最高排放标准为0.50 mg/L。
② Ag++2CN- = [ Ag (CN)2]-, Ag++I- = AgI↓, AgI呈黄色,且CN-优先与Ag+反应。
实验如下:
取25.00 mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.000 ×10-4 mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为2.50 mL。
④滴定终点的判断方法是____________________
⑤处理后的废水中氰化钠的含量为__________mg/L,_______(选填“能”、“不能”)排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某H2SO4和Fe2(SO4)3混合液中,测得c(H+)为0.2mol·L-1,c(SO42-)为0.4 mol·L-1,则混合液中c(Fe3+)为
A. 0.1 mol·L-1 B. 0.2mol·L-1 C. 0.3mol·L-1 D. 0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某 NaOH 溶液中通入 CO2 气体后得到溶液 M,因 CO2 通入的量不同, 溶液 M 的组成也不同,若向溶液 M 中逐滴加入盐酸,产生的气体体积 V(CO2)与加入盐酸的体积 V(HCl)的关系如图所示。则下列分析与判断 不正确的是(不计CO2溶解)
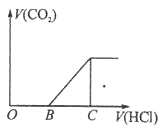
A. 若 OB=0,则形成溶液的过程中所发生反应的离子方程式为OH-+CO2=HCO3-
B. 若 OB=BC,则溶液 M 为Na2CO3 溶液
C. 若 OB>BC,则溶液 M 中大量存在的阴离子为 CO32-和HCO3-
D. 若 3OB=BC,则溶液 M 中 c(NaHCO3)=2c(Na2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)COC12俗称光气,分子中C原子采取sp2杂化成键,光气分子的结构式为________,其中碳氧原子之间共价键是________(填序号)。
a.2个σ键b.2个π键c.1个σ键,1个π键
(2)CaC2中C22﹣与O22+互为等电子体,O22+的电子式可表示为________。
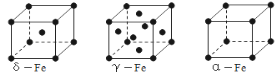
(3)铁有δ、γ、α三种同素异形体,γ晶体晶胞中所含有的铁原子数为________,δ、α两种晶胞中铁原子的配位数之比为______(填元素符号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com