
����Ŀ��þ���Ͻ����Ͻ𡢹����ζ��ǹ㷺�Ľ������ϡ��ش���������
��1������ԭ�ӽṹʾ��ͼΪ___________�������ڱ��е�___���ڣ���____�壻����һ�ֻ��õĽ��������ڿ����в��ױ���ʴ��ԭ����________________________________���û�ѧ����ʽ��ʾ����д�������ռӦ�����ӷ���ʽ___________________��
��2��������;��㡢�����������Ͻ�ij�ָ���������һ��Ԫ����ɣ��������ĸ���Ʒ�������ȵ�Ũ�����ַ�Ӧ�����������壬д��������������Ļ�ѧ����ʽ________________________���ó��ι�������������Һ�еμ���й�������������Һ���۲쵽��������______________����Ӧ�Ļ�ѧ����ʽΪ_________________________��______________��
��3����ʯ�۵���Ҫ�ɷ���Mg3[Si4O10](OH)2,���������ʾ����ɣ�______��������������һ���ᷴӦ���ɸ��ݴ˷�Ӧԭ���Ƶ�������������_______�����õĹ����β�Ʒ��_____�� _______��______��
���𰸡�![]() �� IIIA 4Al+3O2==2Al2O3 2Al+2OH- +2H2O==2AlO2- +3H2�� C+2H2SO4��Ũ��
�� IIIA 4Al+3O2==2Al2O3 2Al+2OH- +2H2O==2AlO2- +3H2�� C+2H2SO4��Ũ��![]() CO2��+2SO2��+2H2O ������ɫ������Ѹ�ٱ���̣�����ɺ��ɫ�� FeSO4+2NaOH==Fe(OH)2��+Na2SO4 4Fe(OH)2 +O2+2H2O==4Fe(OH)3 3MgO��4SiO2��H2O ����� ���� ˮ�� �մ�
CO2��+2SO2��+2H2O ������ɫ������Ѹ�ٱ���̣�����ɺ��ɫ�� FeSO4+2NaOH==Fe(OH)2��+Na2SO4 4Fe(OH)2 +O2+2H2O==4Fe(OH)3 3MgO��4SiO2��H2O ����� ���� ˮ�� �մ�
��������
��1������13��Ԫ�أ���3�����Ӳ㣬�������ֱ�Ϊ2��8��3����ԭ�ӽṹʾ��ͼΪ![]() �������ڱ��е������ڣ���IIIA�壻����һ�ֻ��õĽ��������ڿ����в��ױ���ʴ��ԭ������������е����������γ����ܵ�����Ĥ���û�ѧ����ʽ��ʾΪ4Al+3O2==2Al2O3�������ռӦ����ƫ�����ƺ���������Ӧ�����ӷ���ʽΪ2Al+2OH- +2H2O==2AlO2- +3H2����
�������ڱ��е������ڣ���IIIA�壻����һ�ֻ��õĽ��������ڿ����в��ױ���ʴ��ԭ������������е����������γ����ܵ�����Ĥ���û�ѧ����ʽ��ʾΪ4Al+3O2==2Al2O3�������ռӦ����ƫ�����ƺ���������Ӧ�����ӷ���ʽΪ2Al+2OH- +2H2O==2AlO2- +3H2����
��2��������;��㡢�����������Ͻ�ij�ָ���������һ��Ԫ����ɣ���Ԫ����̼���������ĸ���Ʒ�������ȵ�Ũ�����ַ�Ӧ�������������������Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪC+2H2SO4��Ũ��![]() CO2��+2SO2��+2H2O���ó��ι�������������Һ�еμ���й�������������Һ���۲쵽�������Dz�����ɫ������Ѹ�ٱ���̣���������������������ɺ��ɫ����������������������Ӧ�Ļ�ѧ����ʽ�ֱ�ΪFeSO4+2NaOH==Fe(OH)2��+Na2SO4��4Fe(OH)2 +O2+2H2O==4Fe(OH)3;
CO2��+2SO2��+2H2O���ó��ι�������������Һ�еμ���й�������������Һ���۲쵽�������Dz�����ɫ������Ѹ�ٱ���̣���������������������ɺ��ɫ����������������������Ӧ�Ļ�ѧ����ʽ�ֱ�ΪFeSO4+2NaOH==Fe(OH)2��+Na2SO4��4Fe(OH)2 +O2+2H2O==4Fe(OH)3;
��3��Mg��������ΪMgO�����������ΪSiO2�����������ΪH2O������ݻ��ý���������ϻ��ý���������SiO2H2O��˳���֪Mg3Si4O10��OH��2�ɸijɣ�3MgO4SiO2H2O��������������һ���ᷴӦ���ɸ��ݴ˷�Ӧԭ���Ƶ��������������������õĹ����β�Ʒ�в�����ˮ�ࡢ�մɡ�


 �����ҵ���������ϵ�д�
�����ҵ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�ĵ���������ǿ����
A. 10mL 18.4mol/L���� B. 20mL 1.0mol/L����
C. 30mL 1.0mol/L���� D. 40mL 1.0mol/L��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������[CO(NH2)2] ��һ����Ҫ�ĵ��ʣ��ڹ�ũҵ�����й㷺Ӧ�á�
(1)��ҵ�Ʊ����صķ�Ӧ2NH3(g)��CO2(g)![]() CO(NH2)2(l)��H2O(g)���¶�ΪTKʱ����68gNH3��88gCO2�����ݻ�Ϊ100L�ĺ����ܱ������У�����������Ӧ�����ƽ��ʱCO2��H2O(g)���ʵ�����ȡ�����������ȷ����____________��
CO(NH2)2(l)��H2O(g)���¶�ΪTKʱ����68gNH3��88gCO2�����ݻ�Ϊ100L�ĺ����ܱ������У�����������Ӧ�����ƽ��ʱCO2��H2O(g)���ʵ�����ȡ�����������ȷ����____________��
a��ƽ��ʱ��NH3��Ũ��Ϊ0.02 molL1
b����v(NH3)��=2v(H2O)��ʱ����Ӧ�ﵽƽ��״̬
c�����ں��º�ѹ�����³���ϡ�����壬ƽ�ⷢ�������ƶ�
d�������ʵ��Ĵ��������CO2��ת����
(2)��������ˮ����ˮ�����̼��泥�̼�����Һ�Լ��ԣ�ԭ����___________��̼�����Һ������Ũ���ɴ�С��˳��Ϊ_____________�������һ��Ũ�ȵ�̼�����Һ���뵽��ͬŨ�ȵ�ϡBaCl2��ZnCl2���Һ�У����������ij�����__________��(��֪Ksp(BaCO3)=5.1��10��9mol2L��2��Ksp(ZnCO3)=1.4��10��11 mol2L��2)
(3)�ü�ȩ�����Լ�Ӳⶨ���غ�����������ͨ������ת��Ϊ��Σ���ȩ��NH4+���ã��䷴Ӧ���£�4NH4����6HCHO=(CH2)6N4H����3H����6H2O�������ɵ�H+��(CH2)6N4H��������NaOH��Һ��Ӧ����NaOH����Һ�ζ�ʱ���÷�̪��ָʾ����
��ȡWg������Ʒ����ת����õ�1000mL��Һ����ȡ25.00mL������ƿ�У��μ�2�η�̪����0.1000molL��1NaOH����Һ�ζ����ζ����յ�ʱ�����ļ�Һ���20.50mL��
�� �ζ����յ��������__________________________��
�� ��������Ʒ�Ĵ���Ϊ__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA���������ӵ�������ֵ�������ж���ȷ����
A. 1LpH=13��Ba(OH)2��Һ�к�OH������ĿΪ0.2NA
B. 46gCH3CH2OH��C��H����ĿΪ6NA
C. 4.6gNa�뺬0.1 mol CH3COOH��ϡ������ȫ��Ӧ��ת�Ƶĵ�����Ϊ0.1NA
D. 2.24LCH4��0.5 molCl2��ַ�Ӧ���û��������ԭ����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ҫ������������⡣
��1�������ͼʾ�ش�
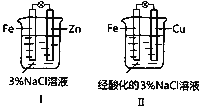
���ڢ��У�ZnΪ_____________�����������������
���ڢ��У�������ӦʽΪ_____________��������________������_____________�����Fe����Cu��������Һ��Na+����_____________�����Fe����Cu������
���ڢ��У����������ġ��������˱�״����5.6 L�����壬��ת��_________mol e-��
��2��Ǧ���ص��ܷ�ӦΪ��Pb��PbO2��2H2SO4![]() 2PbSO4��2H2O���õ�صĸ���������_________�����ѧʽ��
2PbSO4��2H2O���õ�صĸ���������_________�����ѧʽ��
��3����32 g Cu��300 mL 12 mol/L��Ũ���ᷴӦ����ͭȫ���ܽ���ռ�����״���µ�����11.2 L��������NO2ת��ΪN2O4������Ӧ���ĵ���������ʵ�����_____mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʵ����Ҫ�ռ�һƿSO2���壬����ȷ���ռ������ǣ� ��
A.��ˮ������B.�����ſ�����
C.�����ſ�����D.�ű���ʳ��ˮ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������������пa��b���ֱ���������ϡH2SO4��ͬʱ��a�м���������CuSO4��Һ�����и�ͼ��ʾ����H2�����(V)��ʱ��(t)�Ĺ�ϵ��������ȷ���� (����)
A. 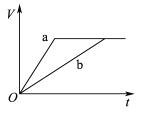 B.
B. 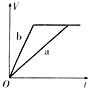
C. 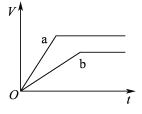 D.
D. 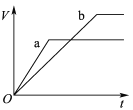
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˳�ȥ�����е�Ca2+��Mg2+��SO42-�������������������������ȷ�IJ���˳���ǣ� ��
�ٹ���
�ڼӹ���NaOH��Һ
�ۼ���������
�ܼӹ���Na2CO3��Һ
�ݼӹ���BaCl2��Һ
A.�٢ܢڢݢ�B.�ܢ٢ڢݢ�C.�ݢڢ٢ܢ�D.�ڢݢܢ٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ�ض����彡���к�����ˣ�����������֯��ʽ����ȷ��ΪʳƷ��ȾԴ֮һ�����Կ��ơ��������г���ʹ��ʱӦ���Կ��Ƶ��ǣ� ��
�������Ͻ���Ƶ��ߢ��ƴ��ߢ�����ɫ�����Ϣ���������ˮ��������С�մ���ʳƷ���ɼ����������ޢ�����������������θҩ���װ�ǹ���СʳƷ
A.�ۢݢ��B.�ޢ��C.�ۢݢ�D.�ۢݢޢߢ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com