
����Ŀ���ں����ܱ�������ͨ��X��������Ӧ��2X��g��Y��g�����¶�T1��T2��X�����ʵ���Ũ��c��X����ʱ��t�仯��������ͼ��ʾ������������ȷ���ǣ� �� 
A.�÷�Ӧ���е�M��ų����������ڽ��е�W��ų�������
B.T2�£���0��t1ʱ���ڣ�v��Y��= ![]() mol?L��1?min��1
mol?L��1?min��1
C.M�������Ӧ����V������N����淴Ӧ����V��
D.M��ʱ�ټ���һ����X��ƽ���X��ת���ʼ�С
���𰸡�C
���������⣺��ͼ��֪���¶�ΪT1�ȵ���ƽ�⣬����T1��T2 �� �¶�Խ�ߣ�ƽ��ʱX�����ʵ���Ũ��Խ��˵�������¶�ƽ�����淴Ӧ�ƶ��������¶�ƽ�������ȷ�Ӧ�ƶ������淴ӦΪ���ȷ�Ӧ������ӦΪ���ȷ�Ӧ��A�����е�M��X��ת���ʽϵͣ����������Ƿ��ȷ�Ӧ�����Է�Ӧ���е�M��ų��������٣���A����
B��T2�£���0��t1ʱ���ڣ�X��Ũ�ȱ仯Ϊ��c��X��=��a��b��mol/L����Y��Ũ�ȱ仯Ϊc��Y��= ![]() c��X��=
c��X��= ![]() mol/L������v��Y��=
mol/L������v��Y��= ![]() molL��1min��1 �� ��B����
molL��1min��1 �� ��B����
C������ͼ���֪���¶�ΪT1ʱ��Ӧ���ȴﵽƽ��״̬���¶ȸ߷�Ӧ���ʿ죬����ƽ���ʱ���٣����¶���T1��T2��M���¶ȸ���N���¶ȣ���N�㷴Ӧû�дﵽƽ��״̬����ʱ��Ӧ������Ӧ������У���N����淴Ӧ����С��N�������Ӧ���ʣ����M�������Ӧ���ʴ���N����淴Ӧ���ʣ���C��ȷ��
D��M��ʱ�ټ���һ����X���ﵽ����ƽ����ԭƽ��Ƚϣ�ѹǿ��������ѹǿƽ�����ƣ���X��ת������������M��ʱ�ټ���һ����X��ƽ���X��ת��������D����
��ѡC��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�����ͻ�������Dz��õͶ������Ͻ�(������������)����ͥ���õ�Ư��ˮ��ʳ�Ρ���������(��ѧҩƷ�곣���Լ�)��ԭ�������ġ���ص��ܷ�Ӧ����ʽΪ2Al��3ClO����2OH��=3Cl����2AlO2-��H2O������˵������ȷ���ǣ� ��
A. �õ�ص��ŵ��ǵ缫���Ϻ͵�����������Ը���
B. �õ�ط���������Ӧ���ǽ�����
C. �缫��������ӦʽΪ3ClO����3H2O��6e��=3Cl����6OH��
D. ����0.1 mol Al��ȫ�ܽ�ʱ���������Һ�ĵ��Ӹ���Ϊ1.806��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ڶԻ�����������Ⱦ�Ķ�����Դ���ǣ� ��
A.ú̿
B.����
C.����
D.����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����٤������������˵������ȷ���ǣ�������
A.58.5 g�Ȼ��ƹ����к���NA���Ȼ��Ʒ��ӣ�
B.1 mol Fe���뷴Ӧʧȥ������Ŀһ��Ϊ2NA
C.1 molNa����ȫ��������Na2O2 �� ʧȥ2NA������
D.�����£�46 g NO2��N2O4�Ļ�����к��еĵ�ԭ����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���£� ![]() ������Ϊ�����������ȼ�ϣ�NH3��NaClO��Ӧ�ɵõ��£�
������Ϊ�����������ȼ�ϣ�NH3��NaClO��Ӧ�ɵõ��£�
��1��ʵ�������Ȼ�狀����������Ʊ������Ļ�ѧ����ʽ��
��2����֪����N2��g��+2O2��g��=N2O4��l����H1=��195kJmol��1
��N2H4��l��+O2��g��=N2��g��+2H2O��g����H2=��534kJmol��1
д��Һ̬�º�N2O4��l����Ӧ����N2��ˮ�������Ȼ�ѧ����ʽ��
��3����֪����1mol��ѧ�������������kJ�����£�N��NΪ942��O=OΪ498��N��NΪ154��H��OΪ464�������N2H4��l��+O2��g��=N2��g��+2H2O��g����H2=��534kJmol��1�����ݼ������1molN��H�������������kJ���ǣ�
��4��д��NH3��NaClO��Ӧ�õ��µĻ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڿ��淴Ӧ��2A��g��+B��g��2C��g����H��0�����и�ͼ����ȷ���ǣ� ��
A.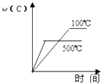
B.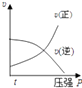
C.
D.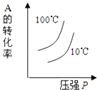
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£�ͨ�����з�Ӧ�����Ʊ������մɵ�ԭ��MgO��MgSO4��s��+CO��g��MgO��s��+CO2��g��+SO2��g����H��0�÷�Ӧ�ں��ݵ��ܱ������дﵽƽ��������ı�ͼ�к�����x��ֵ�����´ﵽƽ���������y��x�仯���ƺ������ǣ� ��
ѡ�� | x | y |
A | MgSO4����������������� | CO��ת���� |
B | CO�����ʵ��� | CO2��CO�����ʵ���֮�� |
C | SO2��Ũ�� | ƽ�ⳣ��K |
D | �¶� | �����ڻ��������ܶ� |

A.A
B.B
C.C
D.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A. ͬ��ͬѹ�£���ͬ��������ʣ������ʵ���һ�����
B. �κ��������������ʵ�����CH4��C0�����ķ�����һ�����
C. 1LCO����һ����1LO2������С
D. ��״���£�2.24LCCl4��6.02��1022������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ�������
A.��KClO3���KCl������뻹ԭ��
B.�������Һ�м�����������������Һ�������кͷ�Ӧ����Һ�ĵ�����������
C.��֪��ˮ���ܶȱ�ˮС����Ũ��Խ���ܶ�ԽС�������������ֱ�Ϊ5%��15%�İ�ˮ�������ϣ��õ�����Һ��������������10%
D.һ�������£�H2��O2�Ļ������Ե���������ܶ�Ϊ1����H2��O2�����ʵ���֮��Ϊ2��13
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com