
| A、5.8 | B、11.6 |
| C、23.2 | D、46.4 |
| n |
| M |
| 8g |
| 32g/mol |
| 11.6g |
| 0.5mol |


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:
+ 4 |
2- 3 |
2- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将NaHCO3固体加入新制氯水中,有无色气泡(H+) |
| B、使红色布条退色(HCl) |
| C、向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈红色(Cl2) |
| D、滴加AgNO3溶液生成白色沉淀(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
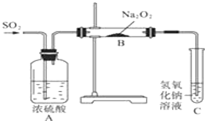 有两个实验小组探究Na2O2与SO2的反应,都用如图所示装置进行实验.
有两个实验小组探究Na2O2与SO2的反应,都用如图所示装置进行实验.
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
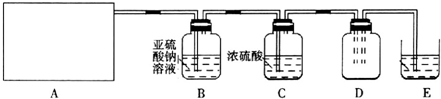
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量洗气瓶B中溶液于试管Ⅰ中,滴加 | 若产生的白色沉淀,则洗气瓶B溶液中存在SO42-. |
| 步骤2:另取适量洗气瓶B中溶液于试管Ⅱ中,滴加 过量Ba(NO3)2溶液振荡,静置. | 产生白色沉淀. |
| 步骤3:取步骤2后试管Ⅱ中的上层清液于试管Ⅲ中,滴加 | 若产生白色沉淀,则洗气瓶B溶液中存在Cl- |
| 实验步骤 | 实验操作 | ||||
| Ⅰ | 取少量质量的FeCO2固体置于坩埚中,高温煅烧至质量不再减轻,冷却至室温 | ||||
| Ⅱ | 取少量实验步骤Ⅰ所得固体放于一洁净的试管中,用足量的稀硫酸溶解 | ||||
| Ⅲ | 向实验步骤Ⅱ所得溶液中滴加KSCN溶液,溶液变红 | ||||
甲同学的结论:4FeCO3+O2
| |||||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Na+、AlO2-、SO42- |
| B、Mg2+、Al3+、NO3-、SO42- |
| C、Na+、K+、SO42-、MnO4- |
| D、NH4+、Na+、HCO3-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
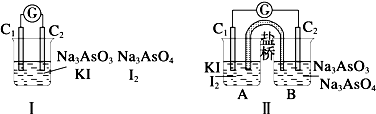
| A、甲组操作时,电流计(G)指针发生偏转 |
| B、乙组操作时,C1上发生的电极反应为 I2+2e-═2I- |
| C、甲组操作时,溶液颜色变浅 |
| D、乙组操作时,C2做正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| I |
| II |
| 催化剂 |
| 时间(s) | 0 | 2 | 4 | 6 | 8 | 10 |
| n(NO)(mol) | 0.4 | 0.32 | 0.26 | 0.22 | 0.20 | 0.20 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com