
【题目】铋及其化合物在工业生产中用途广泛,某研究小组用浮选过的辉铋矿(主要成分是Bi2S3,还含少量SiO2等杂质)制备NaBiO3,其流程如下:

已知:水解能力:Bi3+>Fe3+。
回答下列问题:
(1)“浸取”时,为了提高浸取速率,可采取的措施有______(任写一条);过滤1的滤渣的主要成分有______(填化学式)。
(2)浸取时加入过量浓盐酸的目的是______;“母液”中通入气体X后可循环利用,气体X为______(填名称)。
(3)写出焙烧时生成铋酸钠的化学方程式______;当消耗标准状况下4.48 L O2时,转移电子的数目是______。
(4)25℃时,向浓度均为0.04 mol·L-1的Cu2+、Pb2+、Bi3+的混合溶液中滴加(NH4)2S溶液(设溶液体积增加1倍),当c(Pb2+)=10-5 mol·L-1时恰好完全沉淀,所得溶液中c(Cu2+)∶c(Bi3+)=______。[已知:Ksp(CuS)=6.0×10-36、Ksp(PbS)=3.0×10-28、Ksp(Bi2S3)=1.6×10-20]
(5)用双硫腙(H2Dz,二元弱酸)~CC14络合萃取法可从工业废水中提取金属离子:H2Dz先将金属离子络合成电中性的物质[如Cu(HDz)2等],再用CCl4萃取此络合物。下图是用上述方法处理含有Hg2+、Bi3+、Zn2+的废水时的酸度曲线(E%表示金属离子以络合物形式被萃取分离的百分率)。
①当调节pH=2.5时,铋(Bi)的存在形式有______。
②向萃取后的CCl4中加入NaOH溶液可将铋元素以氢氧化物的形式沉淀下来,相应的离子方程式为______。
【答案】 粉碎矿石,适当提高浸取时温度、适当提高溶液浓度、搅拌等 S、SiO2 防止FeCl3及BiCl3水解生成不溶性沉淀,提高原料的浸出率 氯气 2Bi + 2O2 + Na2O2 ![]() 2NaBiO3 NA或6.02×1023 10-11﹕1 Bi3+、Bi(HDz)3 Bi(HDz)3 + 6OH- === Bi(OH)3 + 3H2O + 3Dz3-
2NaBiO3 NA或6.02×1023 10-11﹕1 Bi3+、Bi(HDz)3 Bi(HDz)3 + 6OH- === Bi(OH)3 + 3H2O + 3Dz3-
【解析】(1)“浸取”时,为了提高浸取速率,可采取的措施有粉碎矿石、适当提高浸取时温度、适当提高溶液浓度、搅拌等;二氧化硅与盐酸和氯化铁不反应,Bi2S3中的-2价S被氧化为单质硫,则滤渣的主要成分有S、SiO2。(2)由于铁离子、Bi3+易水解,因此溶浸时加入过量浓盐酸的目的是防止FeCl3及BiCl3水解生成不溶性沉淀,提高原料的浸出率;加入铁粉后铁离子转化为亚铁离子,Bi3+转化为单质铋,氯气能把氯化亚铁氧化为氯化铁而循环利用,所以气体X为氯气。(3)焙烧时生成铋酸钠的化学方程式为2Bi+2O2+Na2O2![]() 2NaBiO3;反应中只有Bi元素化合价升高,从0价升高到5价,当消耗标准状况下4.48LO2即0.2mol氧气时,转移电子的个数是NA。(4)根据溶度积常数可知此时Bi3+未沉淀,浓度是0.02 mol/L。铜离子浓度是
2NaBiO3;反应中只有Bi元素化合价升高,从0价升高到5价,当消耗标准状况下4.48LO2即0.2mol氧气时,转移电子的个数是NA。(4)根据溶度积常数可知此时Bi3+未沉淀,浓度是0.02 mol/L。铜离子浓度是![]() ,所以所得溶液中c(Cu2+)∶c(Bi3+)=10-11∶1。(5)①当调节pH=2.5时铋的萃取率是0.8,所以铋(Bi)的存在形式有Bi3+、Bi(HDz)3;②向萃取后的CCl4中加入NaOH溶液可将铋元素以氢氧化物的形式沉淀下来,相应的离子方程式为Bi(HDz)3+6OH-=Bi(OH)3↓+3H2O+3Dz2-。
,所以所得溶液中c(Cu2+)∶c(Bi3+)=10-11∶1。(5)①当调节pH=2.5时铋的萃取率是0.8,所以铋(Bi)的存在形式有Bi3+、Bi(HDz)3;②向萃取后的CCl4中加入NaOH溶液可将铋元素以氢氧化物的形式沉淀下来,相应的离子方程式为Bi(HDz)3+6OH-=Bi(OH)3↓+3H2O+3Dz2-。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
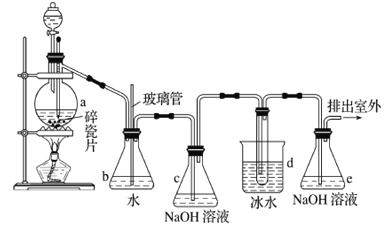
【题目】1,2-二溴乙烷可作抗爆剂的添加剂。如图为实验室制备1,2-二溴乙烷的装罝图, 图中分液漏斗和烧瓶a中分别装有浓H2SO4和无水乙醇,d装罝试管中装有液溴。
已知:CH3CH2OH![]() CH2=CH2↑+H2O;2CH3CH2OH
CH2=CH2↑+H2O;2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
相关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | 溴 | |
状态 | 无色液体 | 无色液体 | 无色液体 | 红棕色液体 |
密度/g·cm-3 | 0.79 | 2.18 | 0.71 | 3.10 |
沸点/℃ | 78.5 | 131.4 | 34.6 | 58.8 |
熔点/℃ | -114.3 | 9.79 | - 116.2 | -7.2 |
水溶性 | 混溶 | 难溶 | 微溶 | 可溶 |
(1)实验中应迅速将温度升高到170℃左右的原因是______________________________。
(2)安全瓶b在实验中有多重作用。其一可以检查实验进行中d装罝中导管是否发生堵塞,请写出发生堵塞时瓶b中的现象:_______________________________;如果实验时d装罝中导管堵塞,你认为可能的原因是_______________________________________________;安全瓶b还可以起到的作用是__________________。
(3)容器c、e中都盛有NaOH溶液,c中NaOH溶液的作用是________________________________。
(4)除去产物中少量未反应的Br2后,还含有的主要杂质为___________,要进一步提纯,下列操作中必需的是_____________ (填字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(5)实验中也可以撤去d装罝中盛冰水的烧杯,改为将冷水直接加入到d装罝的试管中,则此时冷水除了能起到冷却1,2-二溴乙烷的作用外,还可以起到的作用是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对水垢的主要成分是CaCO3和Mg(OH)2而不是CaCO3和MgCO3的解释,说法正确的是
A. Mg(OH)2的溶度积大于MgCO3的溶度积,且在水中发生了沉淀转化
B. Mg(OH)2比MgCO3更难溶,且在水中发生了沉淀转化
C. MgCO3电离出的CO![]() 发生水解,使水中OH-浓度减小,对Mg(OH)2沉淀溶解平衡而言,Qc<Ksp,生成Mg(OH)2沉淀
发生水解,使水中OH-浓度减小,对Mg(OH)2沉淀溶解平衡而言,Qc<Ksp,生成Mg(OH)2沉淀
D. 二者不能相互转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】4种相邻主族短周期元素的相对位置如表,元素X的原子核外电子数是M的2倍,Y的氧化物具有两性。回答下列问题:
![]()
(1)元素X在周期表中的位置是第________周期、第________族,其单质可采用电解熔融________的方法制备。
(2)M、N、Y三种元素最高价氧化物对应的水化物中,酸性最强的是____________,碱性最强的是______。(填化学式)
(3)气体分子(MN)2的电子式为___________。(MN)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式为________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学上常用AG表示溶液中的lg 。25℃时,用0.100 molL-1的NaOH溶液滴定20.00 mL 0.100 molL-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是
。25℃时,用0.100 molL-1的NaOH溶液滴定20.00 mL 0.100 molL-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是

A. D点溶液的pH = 11.25
B. B点溶液中存在 c(H+)-c(OH-)=c(NO2-)-c(HNO2)
C. C点时,加入NaOH溶液的体积为20 mL
D. 25℃时,HNO2的电离常数Ka=1.0×10-5.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可用甲苯合成苯甲醛:
 ,
,
下列说法正确的是
A. 甲苯分子中所有原子都在同一平面内 B. 反应①②③的反应类型相同
C. 一氯甲苯的同分异构体有3种 D. 苯甲醇可与金属钠反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)已知:pOH=-lgc(OH-)。常温下,某弱酸的钠盐(Na2XO3)溶液中微粒浓度的变化关系如下图所示。下列说法正确的是

A. 溶液加水稀释,![]() 先增大后不变
先增大后不变
B. 在NaHXO3溶液中:![]() >1
>1
C. 向Na2XO3溶液中滴加稀盐酸至溶液显中性时:c(Na+)+2c(H+)=c(HXO3-)+2c(XO32-)+2c(OH-)
D. 实线M表示pOH与![]() 的变化关系
的变化关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下图烧杯中各盛有40 mL的溶液。

(1)甲溶液pH=__________,水电离的c(OH-)=________mol/L。
(2)若分别取20 mL甲溶液和乙溶液充分混合,所得的混合溶液丙的pH=6,水电离的c(H+)=________mol/L;溶液中离子浓度大小顺序是__________。
(3)若将剩余的乙溶液全部倒入上述混合溶液丙中,所得的混合溶液pH>7,该溶液中离子浓度大小顺序是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳热还原法广泛用于合金及材料的制备。回答下列问题:
(1)一种制备氮氧化铝的反应原理为23Al2O3+15C+5N2==2Al23O27N5+15CO,产物Al23O27N5中氮的化合价为______________________________。
(2)真空碳热冶铝法包含很多反应,其中的三个反应如下:
Al2O3 (s)+3C(s)==Al2OC(s)+2CO(g)△H1
2Al2OC(s)+3C(s)==Al4C3(s)+2CO(g)△H2
2Al2O3 (s)+9C(s)== Al4C3 (s)+6CO(g)△H3
①△H3=_________(用△H1、△H2表示)。
②Al4C3可与足量盐酸反应制备一种最简单的烃,该反应的化学方程式为__________________________。(3)下列是碳热还原制锰合金的三个反应,CO与CO2平衡分压比的自然对数值(1nK=2.303lgK)与温度的关系如图所示(已知Kp是用平衡分压代替浓度计算所得的平衡常数。分压=总压×气体的物质的量分数)。

I.Mn3C(s)+4CO2(g) ![]() 3MnO(s)+5CO(g)Kp(I)
3MnO(s)+5CO(g)Kp(I)
II.Mn(s)+CO2(g) ![]() MnO(s)+CO(g) Kp(II)
MnO(s)+CO(g) Kp(II)
III.Mn3C(s)+CO2(g) ![]() 3Mn(s)+2CO(g)Kp(III)
3Mn(s)+2CO(g)Kp(III)
①△H>0的反应是__________________(填“I”“II”或“I”)。
②1200K时,在一体积为2L的恒容密闭容器中有17.7gMn3C(s)和0.4molCO2,只发生反应I,5min后达到平衡,此时CO的浓度为0.125mol/L,则0~5min内V(CO2)=____________。
③在一体积可变的密闭容器中加入一定量的Mn(s)并充入一定量的CO2(g),只发生反应II,下列能说明反应II达到平衡的是____________(填字母)。
A.容器的体积不再改变 B.固体的质量不再改变 C.气体的总质量不再改变
④向恒容密闭容器中加入Mn3C并充入0.1molCO2,若只发生反应III,则在A点反应达到平衡。当容器的总压为akPa时,CO2的转化率为______________;A点对应温度下的Kp(III)=____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com