
【题目】下列关于苯乙烷(![]() )的叙述,正确的是
)的叙述,正确的是
①能使酸性高锰酸钾溶液褪色 ②可以发生加聚反应 ③可溶于水 ④可溶于苯 ⑤能与浓硝酸发生取代反应 ⑥所有原子可能共面
A. ①④⑤ B. ①②⑤⑥ C. ①②④⑤⑥ D. ①②③④⑤⑥
科目:高中化学 来源: 题型:
【题目】关于下图的说法不正确的是( )
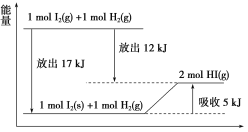
A.1 mol I2(s)与1 mol H2(g)化合生成2 mol HI(g)时,需要吸收5 kJ的能量
B.2 mol HI(g)分解生成1 mol I2(g)与1 mol H2(g)时,需要吸收12 kJ的能量
C.1 mol I2(s)变为1 mol I2(g)时需要吸收17 kJ的能量
D.I2(g)与H2(g)生成2HI(g)的反应是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与纯水的电离相似,液氨中也存在着微弱的电离:2NH3![]() NH4++NH2-据此判断以下叙述错误的是
NH4++NH2-据此判断以下叙述错误的是
A. 液氨中含有NH3、NH4、NH2-三种微粒
B. 一定温度下液氨中c(NH4+)·c(NH2-)是一个常数
C. 液氨的电离达到平衡c(NH3)= c(NH4+)=c(NH2-)
D. 只要不加入其他物质,液氨中c(NH4+)=c(NH2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某试液中只可能含有K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO32-、AlO2-中的若干种离子,离子浓度均为0.1mol/L,某同学进行了如下实验:(已知:稀HNO3可与Fe2+发生氧化还原反应产生NO气体,Fe2+被氧化为Fe3+),下列说法正确的是

A.无法确定原试液中是否含有Al3+、Cl-
B.滤液X中大量存在的阳离子有NH4+、Fe2+和Ba2+
C.原溶液中存在的离子为NH4+、Fe2+、Cl-、SO42-
D.无法确定沉淀C的成分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.已知X是某单质, X、A、B、C含同一种元素,可发生如转化:

(1)写出下列物质的化学式:A________,C__________。
(2)写出以下反应的离子方程式:
②_________________________________________;
④_________________________________________。
II.如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制480mL、1mol/L的稀硫酸。可供选用的仪器有:①烧瓶②烧杯③玻璃棒④药匙⑤量筒

请回答下列问题:
(1)配制稀硫酸时,上述仪器中不需要的仪器是____________(填序号),还缺少的仪器有_____(填写仪器名称)
(2)经计算,配制480mL、1mol/L的稀硫酸需要用量筒量取上述浓硫酸的体积为______mL。
(3)对所配制的稀硫酸进行测定,发现其浓度大于1mol/L,配制过程中下列各项操作可能引起该误差的原因有____________
A.定容时俯视容量瓶刻度线进行定容。
B.在烧杯中将浓硫酸进行稀释后立即转入容量瓶中。
C.转移溶液时,不慎有少量溶液洒到容量瓶外面。
D.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水 。
E.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无机酸有机酯在生产中具有广泛的应用,回答下列问题:
(1)硫酸氢乙酯( )可看作是硫酸与乙醇形成的单酯,工业上常通乙烯与浓硫酸反应制得,该反应的化学方程式为_________,反应类型为__________,写出硫酸与乙醇形成的双酯—硫酸二乙酯(
)可看作是硫酸与乙醇形成的单酯,工业上常通乙烯与浓硫酸反应制得,该反应的化学方程式为_________,反应类型为__________,写出硫酸与乙醇形成的双酯—硫酸二乙酯(![]() )的结构简式_____。
)的结构简式_____。
(2)磷酸三丁酯常作为稀土元素富集时的萃取剂,工业上常用正丁醇与三氯氧磷(![]() )反应来制备,该反应的化学方程式为__________,反应类型为________。写出正丁醇的任意一个醇类同分异构体的结构简式___________。
)反应来制备,该反应的化学方程式为__________,反应类型为________。写出正丁醇的任意一个醇类同分异构体的结构简式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自门捷列夫发现元素周期律以来,人类对自然的认识程度逐步加深,元素周期表中的成员数目不断增加。回答下列问题:
(1)2016年![]() 确认了四种新元素,其中一种为
确认了四种新元素,其中一种为![]() ,中文名为“
,中文名为“![]() ”。元素
”。元素![]() 可由反应:
可由反应:![]() +
+![]() =
=![]() +3
+3![]() 得到。该元素的质子数为______,
得到。该元素的质子数为______,![]() 与
与![]() 互为_________。
互为_________。
(2)![]() 位于元素周期表中第
位于元素周期表中第![]() 族,同族元素N的一种氢化物为NH2NH2,写出该化合物分子的电子式________________.该分子内存在的共价键类型有_______。
族,同族元素N的一种氢化物为NH2NH2,写出该化合物分子的电子式________________.该分子内存在的共价键类型有_______。
(3)该族中的另一元素P能呈现多种化合价,其中![]() 价氧化物的分子式为______,
价氧化物的分子式为______,![]() 价简单含氧酸的分子式为______。
价简单含氧酸的分子式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置(电极均为惰性电极)可吸收SO2,并用阴极排出的溶液吸收NO2。下列说法正确的是

A. N极的电极反应式为2HSO3-+2H++e-==S2O42-+2H2O
B. M极的电极反应式为SO2+2H2O-2e-==SO42-+4H+
C. 离子交换膜为阴离子交换膜
D. b为直流电源的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,可逆反应A+B![]() mC变化如图所示。
mC变化如图所示。

已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后容器内增加压强的变化情况,问:
(1)温度T1________T2(填“大于”、“等于”或“小于”),正反应是________反应(填“吸热”或“放热”)。
(2)如果A、B、C均为气体,则m________2(填“大于”、“等于”或“小于”)。
(3)当温度和容积不变时,如向平衡体系中加入一定量的某稀有气体,则体系的压强________(填“增大”、“减小”或“不变”),平衡________移动(填“向正反应方向”、“向逆反应方向”或“不”,下同)。
(4)当温度和压强不变时,如向平衡体系中加入一定量的某稀有气体,平衡______移动。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com