
【题目】苯丙酸苯酯(![]() )是合成高聚酚酯的原料,其合成路线(部分反应条件略去)如下图所示:
)是合成高聚酚酯的原料,其合成路线(部分反应条件略去)如下图所示:
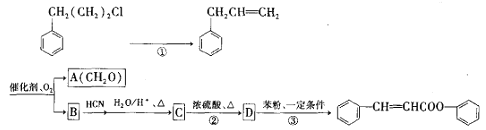
已知: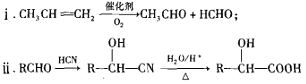
(1)A的化学名称为______,B的结构简式为_______。
(2)C分子中官能团名称是______,由C生成D的反应类型为_______。
(3)反应①的化学方程式为_________。
(4)反应③的化学方程式为____________。
(5)D的同分异构体中,含有碳碳双键和-COO-的芳香族化合物还有__种,其中核磁共振氢谱为5组峰,且峰面积比为2:1:2:2:1的结构简式为______。(任写一种)
(6)根据题目信息,写出以丙烯为原料合成乳酸(![]() )的合成路线______(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
)的合成路线______(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
【答案】 甲醛 ![]() 羟基、羧基 消去反应
羟基、羧基 消去反应  ;
; ![]() 11
11 ![]() 或
或![]() ;
; 
【解析】根据流程图知,①为消去反应、②为醇消去反应、③为羧酸的酯化反应,则A为HCHO、B为![]() ,B发生信息ii的反应,C结构简式为
,B发生信息ii的反应,C结构简式为![]() ,C发生消去反应生成D,D结构简式为
,C发生消去反应生成D,D结构简式为![]() ,D和苯酚发生酯化反应生成
,D和苯酚发生酯化反应生成![]() ;
;
(1)HCHO的化学名称为甲醛,B的结构简式为![]() ;
;
(2)有机物![]() 分子中官能团名称是羟基、羧基,C发生消去反应生成D;
分子中官能团名称是羟基、羧基,C发生消去反应生成D;
(3)反应①是卤代烃的消去,反应的化学方程式为 ;
;
(4)D和苯酚发生酯化反应生成![]() 的化学方程式为
的化学方程式为![]() ;
;
(5)![]() 的同分异构体中,含有碳碳双键和-COO-的芳香族化合物,如果苯环上只有一个支链,有5种,其中羧基位置异构有一种,官能团异构即酯基有4种,如果有两个取代其,其中可能是—COOH,也可能是—OOCH,另一个为乙烯基,苯环上有邻、间、对位,有6种;共有11种结构,其中核磁共振氢谱为5组峰,且峰面积比为2:1:2:2:1的结构简式为
的同分异构体中,含有碳碳双键和-COO-的芳香族化合物,如果苯环上只有一个支链,有5种,其中羧基位置异构有一种,官能团异构即酯基有4种,如果有两个取代其,其中可能是—COOH,也可能是—OOCH,另一个为乙烯基,苯环上有邻、间、对位,有6种;共有11种结构,其中核磁共振氢谱为5组峰,且峰面积比为2:1:2:2:1的结构简式为![]() 或
或![]() ;
;
(6)以丙烯为原料合成乳酸(![]() )的合成路线为
)的合成路线为 ;
;


科目:高中化学 来源: 题型:
【题目】短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上),戊、己分别是空气、地壳中含量最多的元素。下列判断正确的是( )
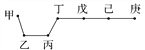
A. 甲一定是金属元素
B. 气态氢化物的稳定性:庚>己>戊
C. 乙、丙、丁的最高价氧化物的水化物可以相互反应
D. 庚的最高价氧化物的水化物酸性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸镧[La2(CO3)3]可用于治疗终末期肾病患者的高磷酸盐血症。制备反应原理为:LaC13+6NH4HCO3= La2(CO3)3↓+6NH4Cl+ 3CO2↑+3H2O;某化学兴趣小组利用下列装置实验室中模拟制备碳酸镧。
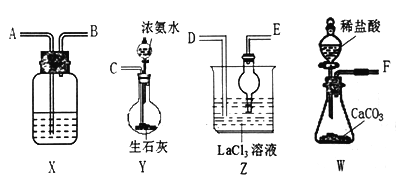
(l)盛放稀盐酸的仪器为____________。
(2)制备碳酸镧实验流程中导管从左向右的连接顺序为:F→___→___ →___ →___ →___ 。
(3)Y中发生反应的化学反应式为________________。
(4)X中盛放的试剂是_____,其作用为________________。
(5)Z中应先通入NH3,后通入过量的CO2,原因为_________。
(6)La2(CO3)3质量分数的测定:准确称取10.0g产品试样,溶于10.0mL稀盐酸中,加入10 mLNH3 —NH4Cl缓冲溶液,加入0.2g紫脲酸铵混合指示剂,用0.5mol/LEDTA(Na2H2Y)标准溶液滴定至呈蓝紫色(La3++H2Y-=LaY-+2H+),消耗EDTA 溶液44.0 mL。则产品中La2(CO3)3的质量分数ω[La2(CO3)3]=_________。
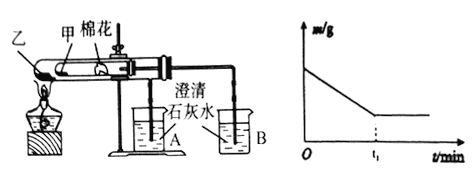
(7)该化学兴趣小组为探究La2(CO3)3和La(HCO3)3的稳定性强弱,设计了如下的实验装置,则甲试管中盛放的物质为_______;实验过程中,发现乙试管中固体质量与灼烧时间的关系曲线如图所示,试描述实验过程中观察到的现象为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.03molCu投入到一定量的浓HNO3中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下672mL气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入O2的体积为
A. 504mL B. 336mL C. 224mL D. 168mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质所含原子数目,按由大到小顺序排列的是( )
①0.5mol NH3 ②标准状况下22.4L He ③4℃ 9mL 水 ④0.2mol H3PO4
A. ①④③② B. ④③②①
C. ②③④① D. ①④②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A. 含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B. 在常温常压下,11.2L Cl2含有的分子数为0.5NA
C. 25℃,1.01×105Pa,64gSO2中含有的原子数为3NA
D. 标准状况下,11.2LH2O含有的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl2广泛应用于工业生产,溶于水形成绿色溶液。CuCl晶体呈白色,难溶于水, 露置于潮湿空气中易被氧化,实验室用下图所示的实验仪器及药品来制备纯净、千燥的氯气并与粗铜(含杂质铁)反应制备氯化铜(铁架台、铁夹及酒精灯省略)。

(1)完成上述实验,气流方向连接各仪器接口的顺序是a→______________________________________;反应时,圆底烧瓶中发生反应的离子方程式为_________。盛粗铜粉的试管中现象是________________________。
(2)实验完毕,取试管中的固体用盐酸溶解后,欲提纯氯化铜,可向溶解液中加入过量__________。(填物质化学式,己知:室温下Fe(OH)3)沉淀完全的pH为3.2)
(3)向制得的氯化铜溶液中通入SO2,加热一段时间即可制得CuCl,写出该反应的离子方式:________________________________。
(4)己知:i.CuCl的盐酸溶液能吸收CO形成Cu(CO)Cl·H2O
ii.保险粉(Na2S2O4)和KOH的混合溶液能吸收氧气
某同学利用如下图所示装置,测定某混合气体中H2、CO、SO2和O2的百分组成

①D瓶测定的气体是_________________;
②E瓶中发生反应的离子方程式为__________________________________。
③为了准确读取G中量气管的数据,读数时除了视线与凹液面最低处相平以外,还要注意_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将某份镁铝合金样品均分为两份,一份加入足量盐酸,另一份加入足量NaOH溶液,同温同压下产生的气体体积比为3∶2,则样品中镁、铝物质的量之比为( )
A. 3∶2 B. 2∶1 C. 4∶3 D. 3∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素性质或原子结构的递变,叙述不正确的是( )
A. Na、Mg、Al原子最外层电子数依次增多 B. P、S、Cl得电子能力依次增强
C. Li、Na、K的电子层数依次增多 D. C、N、O元素最高正化合价依次增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com