
【题目】某一可逆反应的正反应是放热反应,温度对此反应的正、逆反应速率影响的曲线正确的是( )
A.
B.
C.
D.
【答案】C
【解析】解:对应可逆反应,无论吸热还是放热反应,升高温度,正逆反应速率一定同时增大;该反应为吸热反应,所以达到平衡后,温度升高,平衡向着正向移动,正反应速率增大的幅度要大于逆反应速率,图象中满足该变化的为C,
故选C.
【考点精析】利用化学平衡状态本质及特征对题目进行判断即可得到答案,需要熟知化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:
【题目】将物质的量都为amol的金属钠和铝一同放入mg足量的水中,所得溶液的密度为ρg/cm3 , 则此溶液的物质的量浓度为( )
A.![]()
B.![]() mol/L
mol/L
C.![]()
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PCl5的热分解反应如下:PCl5(g)PCl3(g)+Cl2(g)
(1)写出反应的平衡常数表达式;
(2)已知某温度下,在容积为10.0L的密闭容器中充入2.00mol PCl5 , 达到平衡后,测得容器内PCl3的浓度为0.150mol/L.计算该温度下的平衡常数.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 一般来说,不纯的金属与电解质溶液接触时,会发生原电池反应
B. 溶液中Fe2+ 可以用K3[Fe(CN)6]溶液来检测
C. 铁锈覆盖在钢铁表面,阻止钢铁继续腐蚀
D. 在船身上装锌块来避免船体遭受腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图两个电解槽中,a、b、c、d均为石墨电极.若电解过程中共有0.02mol电子通过,下列叙述中正确的是( ) 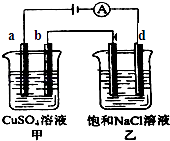
A.甲烧杯中a极上最多可析出铜0.64g
B.甲烧杯中b极上电极反应式4OH﹣﹣4e﹣═2H2O+O2↑
C.乙烧杯中滴入酚酞试液,d极附近先变红
D.烧杯中c极上电极反应式为4H++4e﹣═2H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在病人的尿液中,加入新制的氢氧化铜悬浊液共热,如果有砖红色沉淀生成,说明在病人的尿液中含有( )
A. 淀粉 B. 乙醇
C. 乙酸 D. 葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示常见的单质及其化合物之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物.(反应条件图中已省略). 
(1)向C、D反应后的溶液中加入A,写出该反应的化学方程式
(2)反应②中,若B与F物质的量之比为4:3,G、H分别是、(填化学式)
(3)反应④的离子方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com