
已知常温下B、D、E、L为密度比空气大的气体,D、E为单质,其他为化合物。A是一种淡黄色固体,C微溶于水,F、G均能与L的水溶液反应放出B。据下边反应框图填空。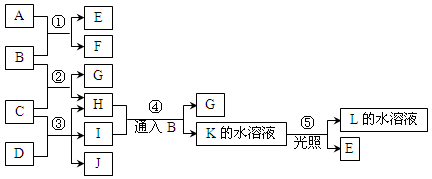
(1)F的俗名是 ,B分子的结构式为________工业上利用反应③生产 。
(2)反应④的离子方程式为 。
(3)有一种单质能与H反应生成E,该反应的化学方程式为 。
(4)某气体M具有漂白作用,既有氧化性,又有还原性,M通入D的溶液中反应的离子方程式为 。
(1)纯碱或苏打(1分),O=C=O (1分)漂白粉(1分)
(2)Ca2++2ClO-+CO2+H2O=CaCO3+2HClO(2分)
(3)2F2+2H2O=4HF+O2(2分)
(4)SO2+Cl2+2H2O=SO42-+2Cl-+4H+(2分)
解析试题分析:A是一种淡黄色固体,且A是化合物,所以A是过氧化钠。A和B反应生成E和F,其中B、D、E、L为密度比空气大的气体,D、E为单质,所以B是CO2,E是氧气,F是碳酸钠。C微溶于水,F、G均能与L的水溶液反应放出B,这说明L应该是酸,因此L是氯化氢。C是氢氧化钙,氢氧化钙和CO2反应生成碳酸钙和水,即H是水。将CO2通入到I的水溶液中生成碳酸钙和K,K光照生成氯化氢和氧气,这说明K是次氯酸,所以I是次氯酸钙,J是氯化钙,D是氯气。
(1)碳酸钠的俗名是纯碱或苏大,CO2分子中含有碳氧双键,其结构式为O=C=O ,氯气与氢氧化钙反应可以制备漂白粉,所以工业上利用反应③生产漂白粉。
(2)碳酸的酸性强于次氯酸,因此CO2通入到次氯酸钙溶液中生成次氯酸,所以反应④的离子方程式为Ca2++2ClO-+CO2+H2O=CaCO3+2HClO。
(3)能和水反应生成氧气的单质可以是单质氟,反应的化学方程式为2F2+2H2O=4HF+O2。
(4)M具有漂白作用,既有氧化性,又有还原性,所以M是SO2,与氯气在水溶液中反应的离子方程式为SO2+Cl2+2H2O=SO42-+2Cl-+4H+。
考点:考查无机框图题的有关判断和应用


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:填空题
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
| 族 周期 | IA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | ② | ③ | ④ | | |
| 3 | ⑤ | | ⑥ | ⑦ | | | ⑧ | |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如图为一些常见无机物之间的转化关系,已知X是一种盐,H是金属单质,F、I是常见非金属单质,E、G都是工业上重要的碱性物质,它们有如图所示的关系.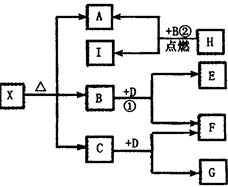
试回答下列问题:
(1)G的化学式为:______________;
(2)写出反应②的化学方程式__________;
(3)碱式盐X在医药上用作解酸剂,与盐酸作用时,生成B的物质的量与消耗盐酸中HCl的物质的量之比为3 :8,则其与盐酸反应的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
生铁中一般含有化合物B,B只有两种元素组成,它的含量、形状、分布对生铁性能影响很大,使生铁硬而脆,不宜进行机械加工。已知:(1)E、F、H、I、P常温下为气体,H、I、P为单质,E是一种红棕色气体。(2)反应①②均为制备理想的绿色水处理剂Na2FeO4的方法,其中反应①在生成Na2FeO4同时还生成NaNO2和H2O。各物质之闻的转化关系如下图所示f图中部分生成物没有列出)。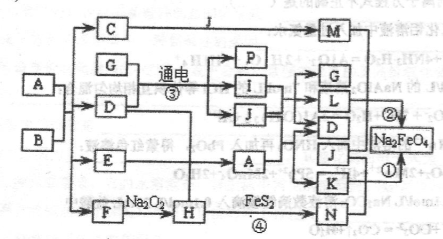
请填写以下空白:
(1)用电子式表示F的形成过程_________________________________________
(2)按要求完成下列反应:__________________________________________
反应③的离子方程式为________________________________________
反应①的化学方程式为________________________________________
(3)反应②中氧化剂与还原剂的物质的量比为__________________________________
反应④中的氧化产物的化学式为_______________________________________
(4)实验室中检验C溶液中金属阳离子的常用方法是________________________
(5)如果A与B反应时生成E与F的物质的量比为13:1,则化合物B的化学式为__________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下图表示有关物质(均由短周期元素形成)之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物。(反应条件图中已省略。)
(1)A、B、C、D代表的物质分别为 、 、 、 (填化学式);
(2)反应①中的C、D均过量,该反应的化学方程式是 ; (3)反应②中,若B与F物质的量之比为4∶3,G、H分别是 、 (填化学式);
(3)反应②中,若B与F物质的量之比为4∶3,G、H分别是 、 (填化学式); (4)反应③产物中K的化学式为 ;
(4)反应③产物中K的化学式为 ; (5)反应④的离子方程式为 。
(5)反应④的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知通常状况下甲、乙、丙、丁等为气体单质,A、B、C、D、E、F、G、H等为化合物,其中A、B、E、G均为气体,C为常见液体。反应①、②、③都是重要的化工反应,反应④是重要的实验室制取气体的反应。有关的转化关系如下图所示(反应条件均已略去)。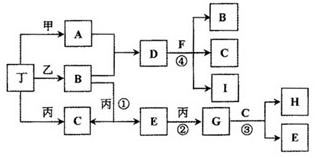
请回答下列问题:
(1)反应④的化学方程式为: ________________________。
(2)B和E在一定条件下可发生反应,这是一个具有实际意义的反应,可消除E对环境的污染,该反应氧化产物与还原产物的物质的量之比为________。
(3)0.1mol lL-1A溶液和0.1mol ?L-1B溶液等体积混合,溶液呈________性,原因是(用离子方程式说明) ________________。
(4)请设计实验检验D晶体中的阳离子(简述实验操作、现象和结论):________________。
(5)pH相同的A、D、H三种溶液,由水电离出的c(OH-)的大小关系是(用A、D、H表示) : ____________。
(6)向一定量的Fe、FeO、Fe3O4的混合物中,加入1mol? L-1 A的溶液100 mL,恰好使混合物全部溶解,且放出336mL(标准状况下)的气体,向所得溶液中加入KSCN溶液,溶液无红色出现;若取同质量的Fe、FeO、Fe3O4混合物,加入1 mol ? L-1 H的溶液,也恰好使混合物全部溶解,且向所得溶液中加入KSCN溶液,溶液也无红色出现,则所加入的H溶液的体积是________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下图所示的是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质和反应条件被略去。常温常压下,化合物A是家庭生活中常用的一种调味品,A、C的焰色反应都呈黄色,8是无色无味的液体,D是黄绿色气体,E、F都是无色气体,F的水溶液是盐酸,H的水溶液具有漂白、杀菌性,J在水溶液中生成时为红褐色沉淀。
(1)H的化学式为 。
(2)F的电子式为 。
(3)反应①的化学方程式为 。
(4)反应②的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列图示实验现象及其解释不正确的是( )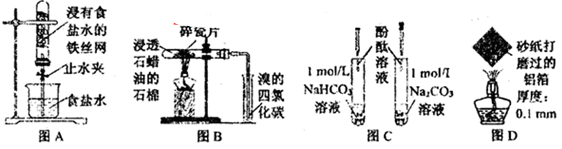
| A.图A,一段时间后打开止水夹,观察到导管中液面上升,因为铁发生了吸氧腐蚀 |
| B.图B,加热一段时间,观察到溴的四氯化碳溶液颜色褪去,因为有气态烯烃产生 |
| C.图C,溶液均变红,碳酸钠溶液颜色较深,因为相同条件下水解能力HCO3-强于CO32- |
| D.图D,加热一段时间,观察到熔化的铝未滴落,因为铝表面生成氧化铝的熔点很高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com