
【题目】【辽宁省大连市2017届高三3月双基测试】下列化学用语正确的有
①乙酸的最简式:CH2O ②二氧化硅的分子式:SiO2
③HClO的结构式:H—Cl—O ④乙烯是结构简式:CH2CH2
⑤Cl-的结构示意图: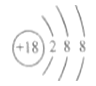
⑥过氧化钠的电子式:
⑦H2CO3的电离方程式:H2CO3![]() H++HCO3-
H++HCO3-
⑧吸氧腐蚀的正极反应:O2+4e-+4H+=2H2O
A. 1个 B. 2个 C. 3个 D. 4个
【答案】B
【解析】①乙酸分子式C2H4O2,乙酸的最简式:CH2O,故①正确; ②SiO2是原子构成,不是分子式是化学式,故②错误;③次氯酸分子中O原子分别与H、Cl原子之间之间形成1对共用电子对,故HClO的结构式为H-O-Cl,故③错误;④乙烯是结构简式:CH2=CH2 ,故④错误;⑤氯离子是由氯原子的得到一个电子后形成的,核内质子数为17,核外电子数18,离子的结构示意图是:![]() ,故⑤错误;⑥过氧化钠是由2个钠离子与1个过氧根离子通过离子键结合而成的离子化合物,电子式为:
,故⑤错误;⑥过氧化钠是由2个钠离子与1个过氧根离子通过离子键结合而成的离子化合物,电子式为:![]() ,是由Na+与O22-构成的,故⑥错误;⑦H2CO3的电离方程式为:H2CO3H++HCO3-,HCO3-=H++CO32-,故⑦正确;⑧吸氧腐蚀是中性电解质溶液中发生的原电池反应,正极电极反应O2+4e-+2H2O═4OH-,故⑧错误;故选B。
,是由Na+与O22-构成的,故⑥错误;⑦H2CO3的电离方程式为:H2CO3H++HCO3-,HCO3-=H++CO32-,故⑦正确;⑧吸氧腐蚀是中性电解质溶液中发生的原电池反应,正极电极反应O2+4e-+2H2O═4OH-,故⑧错误;故选B。


科目:高中化学 来源: 题型:
【题目】下列对沉淀溶解平衡的描述正确的是( )
A. 反应开始时,溶液中各离子浓度相等
B. 沉淀溶解达到平衡时,沉淀的速率和溶解的速率相等
C. 沉淀溶解达到平衡时,溶液中溶质的离子浓度相等,且保持不变
D. 沉淀溶解达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是从蛇床子果实中提取的一种中草药有效成分,是由碳、氢、氧元素组成的酯类化合物;B称作冰片,可用于医药和制香精,樟脑等;C的核磁共振氢谱显示其分子中含有4种氢原子;D中只含一个氧原子,与Na反应放出H2;F为烃。仔细阅读以下转化关系:
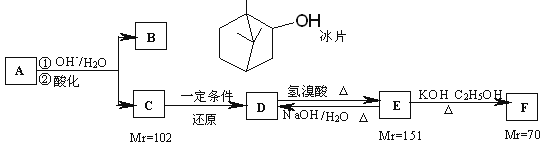

回答以下问题:
(1)B的分子式为__________。
(2)B不能发生的反应是___________(填序号)。
a.氧化反应 b.聚合反应 c.消去反应 d.取代反应 e.与Br2加成反应
(3)E→F的反应类型是____________。
(4)F的分子式为_________,化合物H是F的同系物,相对分子质量为56,H所有可能的结构有______种。
(5)用系统命名法给F命名的名称为______________。
(6)写出E→D的化学力程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,实验现象与结论均正确的是( )
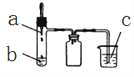
选项 | 实验试剂 | 实验现象 | 实验结论 | ||
a | b | c | |||
A | 浓氨水 | 碱石灰 | FeCl2溶液 | 产生白色沉淀,迅速变为灰绿色,最后变为红褐色 | 氨气具有氧化性 |
B | 稀硫酸 | FeS | AgCl悬浊液 | 悬浊液由白色变为黑色 | Ksp(AgCl)>Ksp(Ag2S) |
C | 浓硝酸 | 铜 | BaSO3悬浊液 | 悬浊液变澄清 | +4价硫具有还原性 |
D | 浓盐酸 | KMnO4 | 紫色石蕊试液 | 溶液先变红后褪色 | Cl2有酸性和漂白性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浅绿色的硫酸亚铁铵晶体[又名莫尔盐,(NH4)2SO4·FeSO4·6H2O]比绿矾(FeSO4﹒7H2O)更稳定,常用于定量分析。莫尔盐的一种实验室制法如下:
![]()
(1)向废铁屑中加入稀硫酸后,并不等铁屑完全溶解而是剩余少量时就进行过滤,其目的是________。
(2)0.10mol·L-1莫尔盐溶液中离子浓度由大到小的顺序为_________;
(3)常温下,若0.1 mol﹒L-1 (NH4)2SO4溶液的pH=5,求算NH3﹒H2O的电离平衡常数Kb=___________
(4)为了测定产品的纯度,称取ag产品溶于水,配制成500mL溶液,用浓度为c mol﹒L-1的酸性KMnO4溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
实验次数. | 第一次 | 第二次 | 第三次 |
消耗高锰酸钾溶液体积/mL | .25.52, | 25.02 | 24.98 |
滴定过程中发生反应的离子方程式为:_______________。滴定终点的现象是____________________。
通过实验数据计算的该产品纯度为_________(用字母ac表)。上表中第一次实验中记录数据明显大于后两次,其原因可能是____________(填符号)。
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烃1 mol能和2 mol HCl加成得到饱和产物,其饱和产物又能和6 mol Cl2完全取代,则该烃是
A. C2H6 B. C2H2 C. C3H4 D. C4H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸是一种常见的弱酸,回答下列问题:
(1)醋酸的电离方程式是 ;
在0.1mol·L﹣1醋酸中加入下列物质,醋酸的电离平衡及平衡时物质的浓度的变化:
(2)向醋酸中加入醋酸钠固体,电离平衡 移动(填向左、向右或不变,下同);c(H+) (填增大、减小或不变,下同),pH (填增大、减小或不变,下同)
(3)向醋酸中加入碳酸钙固体,电离平衡向 移动;c(CH3COOH) .
(4)向醋酸中加入大量的水,c(OH﹣) .导电能力 ,电离平衡常数 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容容器中.可逆反应2NO(g)+O2(g)![]() 2NO2(g)△H<0,不能说明已达到平衡状态的是
2NO2(g)△H<0,不能说明已达到平衡状态的是
A. O2的消耗速率和NO2的生成速率之比为l:2
B. 反应容器中压强不随时间变化而变化
C. 混合气体颜色深浅保持不变
D. 混合气体平均分子量保持不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com