
| X | ||||
| Y | Z | W |
 ��
��| �¶�/�� | 400 | 500 | 800 |
| ƽ�ⳣ��K | 9.94 | 9 | 1 |
���� I����Ԫ�������ڱ���λ�ã���֪X���ڵڶ����ڣ�Y��Z��W���ڵ������ڣ�Y������������������������ȣ���YΪAl������֪ZΪSi��XΪN��WΪCl��
��3����������������Ӧ��Si�ڸ���ʧȥ���ӣ���������������SiO32-��H2O��
��4����֪����C��s��+O2��g���TCO2��g����H=a kJ•mol-1��
��CO2��g��+C��s���T2CO��g����H=b kJ•mol-1��
��Si��s��+O2��g���TSiO2��s����H=c kJ•mol-1
���ݸ�˹���ɣ���+��-�ۿɵ�2C��s��+SiO2��s��=Si��s��+2CO��g������Ӧ��Ҳ������Ӧ�ļ��㣻
��5���ɱ������ݿ�֪�������¶ȣ�ƽ�ⳣ����С��˵��ƽ�����淴Ӧ�����ƶ���
��CO��H2O��ʼ���ʵ�����Ϊ1mol����ƽ��ʱ�μӷ�ӦCO�����ʵ���Ϊxmol����������ʽ��ʾ����������ʵ����仯����ƽ��ʱ��������ʵ�������Ӧǰ����������������仯�������ʵ�������Ũ�ȴ���ƽ�ⳣ������ʽ�з��̼�����
��� �⣺I����Ԫ�������ڱ���λ�ã���֪X���ڵڶ����ڣ�Y��Z��W���ڵ������ڣ�Y������������������������ȣ���YΪAl������֪ZΪSi��XΪN��WΪCl��
��1��Nԭ�ӽṹʾ��ͼΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��2��˵��Cl�ǽ�����ǿ��Si�ķ���ʽΪ��2HClO4+Na2SiO3=2NaClO4+H2SiO3����
�ʴ�Ϊ��2HClO4+Na2SiO3=2NaClO4+H2SiO3����
��3����������������Ӧ��Si�ڸ���ʧȥ���ӣ���������������SiO32-��H2O�������缫��ӦʽΪ��Si-4e-+6OH-=SiO32-+3H2O��
�ʴ�Ϊ��Si-4e-+6OH-=SiO32-+3H2O��
��4����֪����C��s��+O2��g���TCO2��g����H=a kJ•mol-1��
��CO2��g��+C��s���T2CO��g����H=b kJ•mol-1��
��Si��s��+O2��g���TSiO2��s����H=c kJ•mol-1
���ݸ�˹���ɣ���+��-�ۿɵã�2C��s��+SiO2��s��=Si��s��+2CO��g����H=��a+b-c��kJ•mol-1��
�ʴ�Ϊ��2C��s��+SiO2��s��=Si��s��+2CO��g����H=��a+b-c��kJ•mol-1��
��5���ɱ������ݿ�֪�������¶ȣ�ƽ�ⳣ����С��˵��ƽ�����淴Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ�����÷�Ӧ�ġ�H��0��
��CO��H2O��ʼ���ʵ�����Ϊ1mol����ƽ��ʱ�μӷ�ӦCO�����ʵ���Ϊxmol����
CO��g��+H2O��g��?H2��g��+CO2��g��
��ʼ��mol����1 1 0 0
ת����mol����x x x x
ƽ�⣨mol����1-x 1-x x x
��Ӧǰ����������������仯���������ʵ�������Ũ�ȼ���ƽ�ⳣ������$\frac{x��x}{��1-x������1-x��}$=9�����x=0.75����COƽ��ת����Ϊ$\frac{0.75mol}{1mol}$��100%=75%��
�ʴ�Ϊ������75%��
���� ��������ƴ������Ŀ���漰�ṹ����λ�ù�ϵ���缫��Ӧʽ���Ȼ�ѧ����ʽ��ƽ�ⳣ��Ӱ�����ؼ�Ӧ�õȣ��ѶȲ���


 ��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�
��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 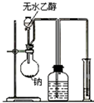 ���������Ҵ���Ӧ����H2����� | B�� | 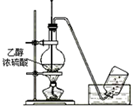 ��ȡ��ϩ | ||
| C�� | 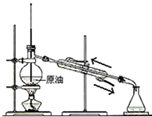 ����ʯ�� | D�� | 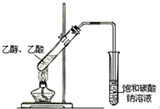 ��ȡ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ȵ�ͭ˿Ѹ�ٲ����Ҵ��У��ɹ۲쵽ͭ˿�����죬�����ŵ��̼�����ζ | |
| B�� | �Ҵ���CH3CH2OH��������ѣ�CH3-O-CH3����Ϊͬ���칹�� | |
| C�� | �ڵ�������Һ�м��뱥���������Һ����ʹ�����ʷ������� | |
| D�� | ú�ĸ����ǻ�ѧ�仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Fe3+����Һ�У�NH4+��Mg2+��Cl-��HSO3- | |
| B�� | ����Al��H2���ɵ���Һ�У�Na+��NH4+��Cl-��NO3- | |
| C�� | NaOH��Һ�У�K+��Na+��AlO2-��CO32- | |
| D�� | NaHCO3��Һ�У�K+��Al3+��Cl-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
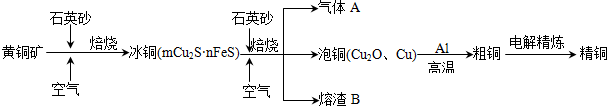
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʱ��ʯī������������������� | |
| B�� | ���ʱ��������Ӧ�ǣ�I--6e-+3H2O�TIO3-+6H+ | |
| C�� | ��Һ������ǿ���ԣ����������� | |
| D�� | ����������Χ��Һ��pH���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
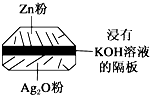 ��1��Ǧ�����ǵ��͵Ŀɳ��͵�أ�����ܷ�ӦʽΪ��Pb+PbO2+4H++2$S{O}_{4}^{2-}$$?_{���}^{�ŵ�}$2PbSO4+2H2O����ش��������⣨�������⡢����������ԭ����
��1��Ǧ�����ǵ��͵Ŀɳ��͵�أ�����ܷ�ӦʽΪ��Pb+PbO2+4H++2$S{O}_{4}^{2-}$$?_{���}^{�ŵ�}$2PbSO4+2H2O����ش��������⣨�������⡢����������ԭ�����鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com