
【题目】按照组成元素可将有机物分为烃和烃的衍生物。
I.丙烯(CH3CH=CH2)是一种重要的化工原料,它存在如下转化关系:

(1)等质量的甲烷、丙烷和丙烯,完全燃烧时耗氧量最多的物质是___。
(2)在120℃、1.01×105Pa条件下时,取一定体积的丙烯和足量的氧气混合点燃,相同条件下测得反应前后气体体积将___(填“变大”“变小”或“不变”)。
(3)丙烯能使溴水褪色,其反应的化学方程式为___,反应类型为___。
(4)CH3CHBrCH3的同分异构体的结构简式为___。
II.由丙烯可以制得多种重要的衍生物,如丙烯酸(CH2=CHCOOH)、乳酸[CH3CH(OH)COOH]等。
(1)丙烯酸中含有的无氧官能团的名称是___。
(2)丙烯酸与CH318OH发生酯化反应的化学方程式为___。
(3)0.2mol乳酸与足量碳酸氢钠溶液反应,能生成标准状况下的CO2___L。
【答案】甲烷(或CH4) 变大 CH3—CH=CH2+Br2![]() 加成反应 CH3CH2CH2Br 碳碳双键 CH2=CHCOOH+CH318OH
加成反应 CH3CH2CH2Br 碳碳双键 CH2=CHCOOH+CH318OH![]()
![]() +H2O(或CH2=CHCOOH+CH318OH
+H2O(或CH2=CHCOOH+CH318OH![]() CH2=CHCO18OCH3+H2O) 4.48
CH2=CHCO18OCH3+H2O) 4.48
【解析】
I.(1)由C~O2~CO2,4H~O2~2H2O进行比较可知,等质量的烃完全燃烧时,消耗氧气的量取决于CHx中x的值,x值越大,耗氧量越多;
(2)丙烯在氧气中完全燃烧生成二氧化碳和水,反应的化学方程式为2C3H6+9O2 ![]() 6CO2+6H2O,由方程式可知在120℃、1.01×105Pa下时,反应前的气体体积小于反应后气体体积;
6CO2+6H2O,由方程式可知在120℃、1.01×105Pa下时,反应前的气体体积小于反应后气体体积;
(3)丙烯含有碳碳双键,能与溴水发生加成反应,使溴水褪色;
(4)丙烷结构对称,分子中含有2类氢原子,一溴代物有2种;
II.(1)丙烯酸的结构简式为CH2=CHCOOH,官能团为羧基和碳碳双键;
(2)在浓硫酸作用下,丙烯酸与CH318OH共热发生酯化反应生成![]() 和H2O;
和H2O;
(3)CH3CH(OH)COOH含有1个羧基和1个羟基,羧基能与碳酸氢钠溶液反应,羟基与碳酸氢钠溶液不反应。
I.(1)由C~O2~CO2,4H~O2~2H2O进行比较可知,等质量的烃完全燃烧时,消耗氧气的量取决于CHx中x的值,x值越大,耗氧量越多,甲烷、丙烷和丙烯中x值分别为4、![]() 、2,则甲烷的耗氧量最高,故答案为:甲烷(或CH4);
、2,则甲烷的耗氧量最高,故答案为:甲烷(或CH4);
(2)丙烯在氧气中完全燃烧生成二氧化碳和水,反应的化学方程式为2C3H6+9O2 ![]() 6CO2+6H2O,由方程式可知在120℃、1.01×105Pa下时,反应前的气体体积小于反应后气体体积,则丙烯完全燃烧后,气体体积变大,故答案为:变大;
6CO2+6H2O,由方程式可知在120℃、1.01×105Pa下时,反应前的气体体积小于反应后气体体积,则丙烯完全燃烧后,气体体积变大,故答案为:变大;
(3)丙烯含有碳碳双键,能与溴水发生加成反应,使溴水褪色,反应的化学方程式为CH3—CH=CH2+Br2![]() ,故答案为:CH3—CH=CH2+Br2
,故答案为:CH3—CH=CH2+Br2![]() ;加成反应;
;加成反应;
(4)丙烷结构对称,分子中含有2类氢原子,一溴代物有2种,则CH3CHBrCH3的同分异构体为CH3CH2CH2Br,故答案为:CH3CH2CH2Br;
II.(1)丙烯酸的结构简式为CH2=CHCOOH,无氧官能团为碳碳双键,故答案为:碳碳双键;
(2)在浓硫酸作用下,丙烯酸与CH318OH共热发生酯化反应生成![]() 和H2O,反应的化学方程式为CH2=CHCOOH+CH318OH
和H2O,反应的化学方程式为CH2=CHCOOH+CH318OH![]()
![]() +H2O,故答案为:CH2=CHCOOH+CH318OH
+H2O,故答案为:CH2=CHCOOH+CH318OH![]() +H2O(或CH2=CHCOOH+CH318OH
+H2O(或CH2=CHCOOH+CH318OH![]() CH2=CHCO18OCH3+H2O);
CH2=CHCO18OCH3+H2O);
(3)CH3CH(OH)COOH含有1个羧基和1个羟基,羧基能与碳酸氢钠溶液反应,羟基与碳酸氢钠溶液不反应,则0.2mol乳酸与足量碳酸氢钠溶液反应生成0.2mol二氧化碳,标准状况下的体积为0.2mol×22.4L/mol=4.48L,故答案为:4.48。


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
【题目】(一)乙醇是一种重要的化工原料,也常用于生产乙醇汽油,解决燃油替代问题。最新以生物质为原料合成乙醇的方案设计中,化学家提出了用H2还原乙酸的方法来提高乙醇的产率和品质。
(1)用H2还原乙酸获得乙醇的反应为 CH3COOH(g)+2H2(g)![]() CH3CH2OH(g)+H2O(g) ΔH。该反应在一定条件下能自发进行,则ΔH__________(填“<”或“>”)0。
CH3CH2OH(g)+H2O(g) ΔH。该反应在一定条件下能自发进行,则ΔH__________(填“<”或“>”)0。
(2)已知该工艺中存在副反应:CH3COOH(g)+H2(g)![]() CO(g)+CH4(g)+H2O(g) ΔH>0。下列措施不能提高乙醇产率的是_____________。
CO(g)+CH4(g)+H2O(g) ΔH>0。下列措施不能提高乙醇产率的是_____________。
A.升高温度 B.增大压强
C.选择合适催化剂 D.增大![]()
(3)下列描述能说明反应CH3COOH(g)+2H2(g)![]() CH3CH2OH(g)+H2O(g)已达化学平衡的是________。
CH3CH2OH(g)+H2O(g)已达化学平衡的是________。
A.氢气、乙酸、乙醇的浓度相同 B.2v(H2)正=v(CH3CH2OH)逆
C.生成1 mol CH3COOH的同时生成1 mol H2O D.体系中乙醇的百分含量保持不变
(4)在![]() =2的条件下投料,某研究小组进行了在相同压强下在相同时间内乙醇的产率随温度变化的测定实验。在图中画出乙醇的产率随温度变化的示意图__________。
=2的条件下投料,某研究小组进行了在相同压强下在相同时间内乙醇的产率随温度变化的测定实验。在图中画出乙醇的产率随温度变化的示意图__________。

(二)NO2是大气污染的主要污染物之一;硝酸盐是水体污染的污染物之一。电化学降解NO3-的原理如图所示,阴极电极反应式为___________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可燃冰是另一种CH4的重要来源,利用可燃冰制备的甲烷可以设计成如下燃料电池,可以作为“移动的发电厂”,源源不断的对外供电,下列说法错误的是

A.a电极通入甲烷气体,作负极
B.每通入1mol CH4,有8mol e-通过质子交换膜
C.b电极的电极反应式为:O2+4e-+4H+=2H2O
D.催化剂电极采用疏松多孔结构可提高电极反应效率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的短周期元素,且X、Z原子序数之和是Y、W原子序数之和的1/2。甲、乙、丙、丁是由这些元素组成的二元化合物,M是某种元索对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下)。上述物质间的转化关系如图所示(部分反应物和生成物省略)。下列说法正确的是

A. 原于半径:r(Y)>r(Z)>r(W)
B. 化合物N、乙烯使溴水褪色的原理相同
C. 含W元素的盐溶液可能显酸性、中性或碱性
D. Z与X、Y、W形成的化合物中,各元素均满足8电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在BaSO4饱和溶液中加入少量的BaCl2溶液产生BaSO4沉淀,若以Ksp表示BaSO4的溶度积常数,则平衡后溶液中
A.c(Ba2+)·c(SO42-)=Ksp,c(Ba2+)>c(SO42-)
B.c(Ba2+)=c(SO42-)=(Ksp)1/2
C.c(Ba2+)·c(SO42-)>Ksp,c(Ba2+)=c(SO42-)
D.c(Ba2+)·c(SO42-)≠Ksp,c(Ba2+)<c(SO42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学兴趣小组设计“乙醇催化氧化实验”来探究催化剂的催化机理并对反应后的产物进行分析,装置(夹持装置等已省略)如图所示。试回答以下问题:
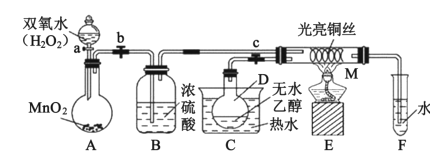
(1)C中热水的作用是___;在装入实验药品之前,应进行的操作是___。
(2)装入实验药品后,关闭活塞a、b、c,在铜丝的中间部分加热片刻,M处铜丝由红变黑,反应的化学方程式为___,然后打开活塞a、b、c,通过控制活塞a和b,间歇性地通入气体,即可在M处观察到受热部分的铜丝交替出现变红、变黑的现象。铜丝由黑变红时,发生反应的化学方程式为___。通过实验,可以得出结论:该实验过程中催化剂___(填“参加”或“不参加”)化学反应。
(3)反应进行一段时间后,试管F中能收集到的有机物主要有___、___。
(4)若试管F中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还有___。要除去该物质,可先在混合液中加入___(填字母),然后通过___即可(填操作名称)。
A.氯化钠溶液 B.苯 C.碳酸氢钠溶液 D.四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于![]() 晶体网状结构(如图)的叙述正确的是
晶体网状结构(如图)的叙述正确的是
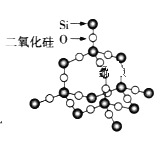
A. 存在四面体结构单元, ![]() 处于中心,
处于中心, ![]() 处于4个顶角
处于4个顶角
B. 最小环上有3个![]() 原子和3个
原子和3个![]() 原子
原子
C. 最小环上![]() 和
和![]() 原子数之比为1:2
原子数之比为1:2
D. 最小环上有6个![]() 原子和6个
原子和6个![]() 原子
原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D都是含有碳、氢、氧三种元素的有机物,其中A、C分别是白酒和食醋中含有的成分,A、B、C、D间有如下转化关系:
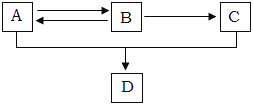
(1)A结构简式为___,C结构简式为___。
(2)写出A与C在浓H2SO4存在条件下加热反应生成D的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 饱和Na2CO3溶液与CaSO4固体反应:CO32+CaSO4![]() CaCO3+SO42
CaCO3+SO42
B. 酸化NaIO3和NaI的混合溶液:I +IO3+6H+![]() I2+3H2O
I2+3H2O
C. KClO碱性溶液与Fe(OH)3反应:3ClO+2Fe(OH)3![]() 2FeO42+3Cl+4H++H2O
2FeO42+3Cl+4H++H2O
D. 电解饱和食盐水:2Cl+2H+![]() Cl2↑+ H2↑
Cl2↑+ H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com