
【题目】下列指定反应的离子方程式正确的是
A. 饱和Na2CO3溶液与CaSO4固体反应:CO32+CaSO4![]() CaCO3+SO42
CaCO3+SO42
B. 酸化NaIO3和NaI的混合溶液:I +IO3+6H+![]() I2+3H2O
I2+3H2O
C. KClO碱性溶液与Fe(OH)3反应:3ClO+2Fe(OH)3![]() 2FeO42+3Cl+4H++H2O
2FeO42+3Cl+4H++H2O
D. 电解饱和食盐水:2Cl+2H+![]() Cl2↑+ H2↑
Cl2↑+ H2↑
【答案】A
【解析】分析:A项,饱和Na2CO3溶液与CaSO4发生复分解反应生成更难溶于水的CaCO3;B项,电荷不守恒,得失电子不守恒;C项,在碱性溶液中不可能生成H+;D项,电解饱和食盐水生成NaOH、H2和Cl2。
详解:A项,饱和Na2CO3溶液与CaSO4发生复分解反应生成更难溶于水的CaCO3,反应的离子方程式为CO32-+CaSO4![]() CaCO3+SO42-,A项正确;B项,电荷不守恒,得失电子不守恒,正确的离子方程式为5I-+IO3-+6H+=3I2+3H2O,B项错误;C项,在碱性溶液中不可能生成H+,正确的离子方程式为3ClO-+2Fe(OH)3+4OH-=3Cl-+2FeO42-+5H2O,C项错误;D项,电解饱和食盐水生成NaOH、H2和Cl2,电解饱和食盐水的离子方程式为2Cl-+2H2O
CaCO3+SO42-,A项正确;B项,电荷不守恒,得失电子不守恒,正确的离子方程式为5I-+IO3-+6H+=3I2+3H2O,B项错误;C项,在碱性溶液中不可能生成H+,正确的离子方程式为3ClO-+2Fe(OH)3+4OH-=3Cl-+2FeO42-+5H2O,C项错误;D项,电解饱和食盐水生成NaOH、H2和Cl2,电解饱和食盐水的离子方程式为2Cl-+2H2O![]() Cl2↑+H2↑+2OH-,D项错误;答案选A。
Cl2↑+H2↑+2OH-,D项错误;答案选A。


科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分是Al2O3、Fe2O3、SiO2)提纯Al2O3做冶炼铝的原料,提取的操作过程可用以下流程图表示:
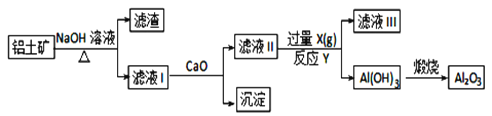
已知:Na2SiO3 + Ca(OH)2= CaSiO3↓+ 2NaOH
(1)氢氧化钠溶液浸取铝土矿时,发生反应的离子方程式有:______________________、______________________。
(2)滤液II中通入过量的气体X是________。反应的化学方程式:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,氧化剂与还原剂的物质的量之比为1:2的是
①2CH3COOH+Ca(C1O)2=2HC1O+Ca(CH3COO)2
② SiO2+2C![]() Si+2CO↑
Si+2CO↑
③4HC1(浓)+MnO2![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
④SiO2+3C![]() SiC+2CO↑
SiC+2CO↑
A. 仅有② B. 仅有②④ C. 仅有②③④ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿是工业炼铜的主要原料,主要成分为CuFeS2,含少量脉石。为测定该黄铜矿的纯度,某同学设计了如下实验:
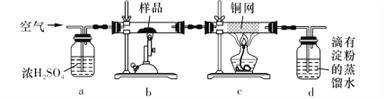
现用电子天平称取研细的黄铜矿样品1.150 g,在空气存在下进行煅烧,生成Cu、Fe3O4和SO2气体,实验后取d中溶液的1/10置于锥形瓶中,用0.05 mol L-1标准碘溶液进行滴定,消耗标准碘溶液20. 00 mL。请回答下列问题:
(1)将样品研细后再进行反应,其目的是_____________________;标准碘溶液应盛放在___________(填“碱式”或“酸式”)滴定管中。
(2) a装置的作用是__________________(填字母代号)。
A.除去空气中的二氧化碳
B.除去空气中的水蒸气
C有利于气体混合
D.有利于观察、控制空气流速
(3)若去掉c装置,会使测定结果_______________(填“偏低”“偏高”或“无影响”),写出影响测定结果的化学方程式:________________________。
(4)上述反应结束后,仍需通一段时间的空气,其目的是___________________________。
(5)通过计算可知,该黄铜矿的纯度为_________________________。
(6) 假设实验操作均正确,测得的黄铜矿纯度仍然偏低,可能的原因主要有_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组拟验证CO2与Na2O2反应的产物,现设计以下实验装置进行实验:

(1)写出装置A中反应的化学方程式________。
(2)写出装置B中反应的化学方程式________。
(3)拟用装置D收集气体产物,请将装置补充完整________。
(4)产物检验:检验气体产物的方法________。
(5)检验固体产物的方法:从B装置中取少量固体,溶于水配成溶液,________。
(6)有同学认为该实验装置存在明显缺陷,你认为该缺陷是什么________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式不正确的是
A. 氯气溶于水:Cl2+H2O![]() H++Cl-+HClO
H++Cl-+HClO
B. Fe和盐酸反应:Fe+2H+ ═Fe3++H2↑
C. NO2溶于水的反应:3NO2+H2O ═ 2H+ + 2NO3- + NO
D. 氧化铜与硫酸反应:CuO+2H+═ Cu2++H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的实验装置图正确且能达到相应实验目的的是
A. 装置除去Cl2中的HCl 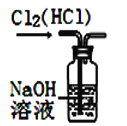
B. 装置实验室制NH3 
C. 装置分离MnO2和KCl 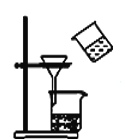
D. 装置蒸干NH4Cl饱和溶液制备NH4Cl晶体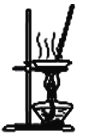
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,pH=1的某溶液A中含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、Cl-、I-、SO42-中的4种,且溶液中各离子的物质的量浓度均为0.1mol/L,现取该溶液进行有关实验,实验结果如下图所示: 下列有关说法正确的是
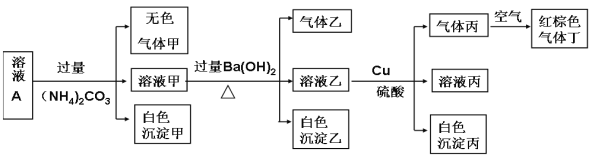
A.该溶液中一定有上述离子中的NO3-、Al3+、SO42-、Cl-四种离子
B.实验消耗Cu 14.4g,则生成气体丁的体积为3.36L
C.沉淀乙一定有BaCO3,可能有BaSO4
D.一定没有Fe3+,但是无法确定是否含有I-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳及其化合物在能源和材料方面具有广泛的用途,回答下列问题:
(1)已知CH4(g)+![]() O2(g)=CO(g)+2H2O(l)
O2(g)=CO(g)+2H2O(l) ![]() =-607.31kJ/mol
=-607.31kJ/mol
2CO(g)+ O2(g)=2CO2(g) ![]() =-566.0kJ/mol
=-566.0kJ/mol
写出表示甲烷燃烧热的热化学方程式________________。
(2)天然气的一个重要用途是制取H2,其原理为:CO2(g)+CH4(g) ![]() 2CO(g)+2H2(g) 。
2CO(g)+2H2(g) 。
在密闭容器中通入物质的量浓度均为0.1mol/L的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图所示。则:
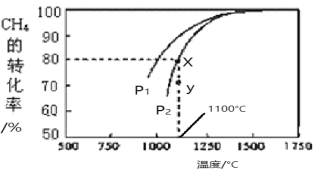
①压强P2_____P1(填 “>”或“<”);原因________________________________________________________________________________。
②压强为P1时,在Y点:v(逆)_______v(正)(填“>”、“<”或“=”)。
③求X点对应温度下的该反应的平衡常数K=____________。(计算结果保留两位小数)
(3)CO可以合成二甲醚,CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g) △H<0,二甲醚可以作为燃料电池的原料。利用此燃料电池以石墨为电极电解1L,0.5mol/L的CuSO4溶液,导线通过0.1mol电子时,假设溶液体积不变,则所得溶液pH=______________,标况下理论上产生O2_______________L(保留小数点后两位)。
CH3OCH3(g)+H2O(g) △H<0,二甲醚可以作为燃料电池的原料。利用此燃料电池以石墨为电极电解1L,0.5mol/L的CuSO4溶液,导线通过0.1mol电子时,假设溶液体积不变,则所得溶液pH=______________,标况下理论上产生O2_______________L(保留小数点后两位)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com