


科目:高中化学 来源: 题型:
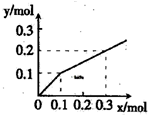 (2010?桂林一模)以Pt为电极,电解含有金属离子M+、N3+各0.10mol的溶液,阴极析出的金属单质或气体的总物质的量(y)与导线中通过电子的物质的量(x)的关系如图所示.对离子氧化能力的强弱判断正确的是(选项中H+为氢离子)( )
(2010?桂林一模)以Pt为电极,电解含有金属离子M+、N3+各0.10mol的溶液,阴极析出的金属单质或气体的总物质的量(y)与导线中通过电子的物质的量(x)的关系如图所示.对离子氧化能力的强弱判断正确的是(选项中H+为氢离子)( )查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 (2010?桂林二模)某课外实验小组设计了如图所示装置进行“一器多用”的实验探究(夹持装置已略去).
(2010?桂林二模)某课外实验小组设计了如图所示装置进行“一器多用”的实验探究(夹持装置已略去).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com