
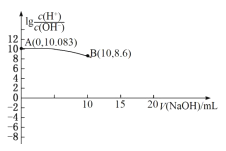
【题目】常温下,用0.010mol/L的NaOH溶液滴定10.00mL 0.010mol/L的酸H2A,滴定过程中加入NaOH溶液的体积(V)与溶液中lg![]() 的关系如图所示(10mL之后的曲线未画出)。下列叙述正确的是( )
的关系如图所示(10mL之后的曲线未画出)。下列叙述正确的是( )
A.H2A![]() H++HA-
H++HA-
B.Ka(HA-)的数量级为10-5
C.滴定过程中,水的电离程度最大的为B点溶液
D.V(NaOH)=15mL时的溶液中:c(Na+)>c(A2-)>c(HA-)
【答案】D
【解析】
用0.010mol/L的NaOH溶液滴定10.00mL 0.010mol/L的酸H2A,依次发生NaOH+H2A=NaHA+H2O、NaHA+NaOH=Na2A+H2O,则当加入10mL的NaOH溶液,溶液中溶质为NaHA。
A.根据A点可知,lg![]() =10.083,因为Kw=[H+][OH-]=10-14,则A点[H+]=10-1.9585mol/L=0.011mol/L,则H2A一级电离为完全电离,H2A=H++HA-,A错误;
=10.083,因为Kw=[H+][OH-]=10-14,则A点[H+]=10-1.9585mol/L=0.011mol/L,则H2A一级电离为完全电离,H2A=H++HA-,A错误;
B.根据A点,[H+]=10-1.9585mol/L=0.011mol/L,因为H2A一级电离为完全电离,则第二步电离出的[A2-]=(0.011-0.01)mol/L=0.001mol/L,则![]() ,Ka(HA-)的数量级为10-3,B错误;
,Ka(HA-)的数量级为10-3,B错误;
C.根据酸碱的数量关系10mL时,完全反应生成NaHA为强酸强碱,20mL时完全中和生成Na2A为强碱弱酸盐,能促进水的电离,故水电离程度最大的点为完全中和时,C错误;
D. V(NaOH)=15mL时的溶液中n(NaHA):n(Na2A)=1:1,又因为Ka(HA-)![]() 10-3mol/L,HA-的电离程度大于A2-的水解程度,故当n(NaHA):n(Na2A)=1:1时溶液显酸性,故c(Na+)>c(A2-)>c(HA-),D正确;
10-3mol/L,HA-的电离程度大于A2-的水解程度,故当n(NaHA):n(Na2A)=1:1时溶液显酸性,故c(Na+)>c(A2-)>c(HA-),D正确;
答案选D。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】灼热的焦炭与水蒸气反应所得产物为H2、CO和少量CO2,为了检验产物中的H2和CO(设气体均被充分吸收),设计如下实验装置。下列有关说法错误的是
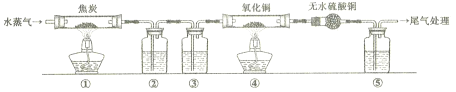
A. 为了实验安全,应先点燃①处酒精灯,后点燃④处酒精灯
B. ②、③、⑤中依次盛装氢氧化钠溶液、浓硫酸和澄清石灰水
C. ④中黑色固体变红色,即可证明产物中一定含有H2和CO中的一种或两种
D. 若用碱石灰替换无水硫酸铜,也可以达到检验H2和CO目的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA 表示阿伏加德罗常数,下列叙述正确的是( )
A.常温常压下,4gH2含有的分子数为2NA
B.17g氨气所含电子数目为8NA
C.将1体积c1mol/L的硫酸溶于4体积水中 ,稀溶液的浓度为0.2c1mol/L
D.将5.85gNaCl 晶体溶入100mL水中,制得0.1mol/L的NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】太和一中理化创新社的同学们为了探究在实验室制备![]() 的过程中有水蒸气和
的过程中有水蒸气和![]() 挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。

(1)若用含有![]() 的浓盐酸与足量的
的浓盐酸与足量的![]() 反应制
反应制![]() ,制得的
,制得的![]() 体积(标准状况下)总是小于
体积(标准状况下)总是小于![]() 的原因是_____________________。
的原因是_____________________。
(2)①装置B的作用是_______________________,现象是_____________________。
②装置C和D出现的不同现象说明的问题是__________________________。
③装置E的作用是_______________________________。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入![]() 溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入
溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入![]() 溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在_________与_________之间(填装置字母序号),装置中应放入___________________________。
溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在_________与_________之间(填装置字母序号),装置中应放入___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究团队在优化催化剂的基础上,通过调节电极的孔道和疏水性增加CO的扩散速率,实现了高选择性将CO电解还原制备乙烯,如图所示。下列叙述错误的是( )
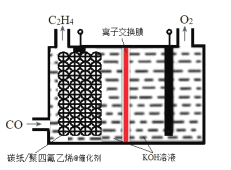
A.碳纸/聚四氟乙烯电极为阴极
B.聚四氟乙烯的作用是吸附并增加CO的浓度
C.为了维持电解的效率,离子交换膜应为阳离子交换膜
D.碳纸上生成C2H4的电极反应式为:2CO+6H2O+8e-=C2H4+8OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:A(g)+3B(g)![]() 2C(g),有关下列图像说法的不正确的是( )
2C(g),有关下列图像说法的不正确的是( )
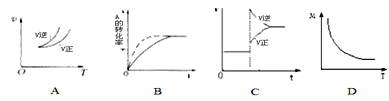
A. 依据图A可判断正反应为放热反应
B. 在图B中,虚线可表示使用了催化剂
C. 若正反应的△H<0,图C可表示升高温度使平衡向逆反应方向移动
D. 由图D中混合气体的平均相对分子质量随温度的变化情况,可推知正反应的△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述中正确的是( )
A. 分子总数为NA的二氧化硫和二氧化碳混合气体中含有的原子数为3NA
B. 任何条件下,20 L 氧气含有的分子数都不可能为NA
C. 在标准状况下,2 g氖气含有NA个氖原子
D. 物质的量相等的任何气体中都含有相同的原子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水合肼(N2H4H2O)是制备叠氮化钠(NaN3)的原料,而叠氮化钠又是汽车安全气囊最理想的气体发生剂的原料。如图是工业水合肼法制备叠氮化钠的工艺流程。

查阅资料:①水合肼有毒且不稳定,具有强还原性和强碱性;
②有关物质的物理性质如下表:
物质 | 甲醇 | 水合肼 | 亚硝酸甲酯 | 叠氮化钠 |
熔点(℃) | -97 | -40 | -17 | 275(410℃:易分解) |
沸点(℃) | 64.7 | 118.5 | -12 | — |
回答下列问题:
Ⅰ.合成水合肼。实验室水合肼合成水合肼装置如图所示,NaClO碱性溶液与尿素CO(NH2)2水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应可以制得水合肼。
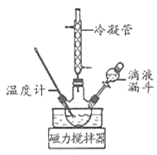
(1)实验中通过滴液漏斗向三颈瓶中缓慢滴加NaClO溶液的原因是_____;N2H4 的结构式为_____,制取N2H4H2O的离子方程式为_________。
II.制备叠氮化钠。实验室可利用如图所示的装置及药品制备叠氮化钠。
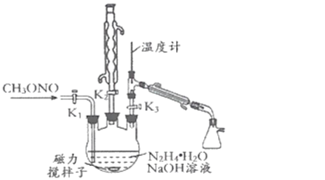
(2)①根据实验发现温度在20℃左右反应的转化率最高,但是该反应属于放热反应,因此 可釆取的措施是_____;流程中A溶液蒸馏前,图中装置中开关K1、K2、K3的合理 操作顺序是______。
②写出该方法制备叠氮化钠的化学方程式:_____。
(3)流程中由B溶液获得叠氮化钠产品的实验步骤为_____,减压过滤,晶体用乙醇洗涤23次后,再_____干燥。
(4)化工生产中,多余的叠氮化钠常使用次氯酸钠溶液处理,在酸性条件下,二者反应可生成无毒的气体。若处理6.5gNaN3,理论上需加入0.5mol L-1的NaClO溶液_____mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物,在标准状况下,其蒸气密度为2.054g/L,则其摩尔质量为_____________,又知4.6克该有机物完全燃烧生成二氧化碳2.24L(标准状况)和1.8克水,则该有机物的分子式为________,该有机物能与乙醇发生酯化反应,则该有机物的结构简式为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com