
【题目】某温度下,向一定体积1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=﹣lg c[OH﹣])与pH的变化关系如图所示,则( ) 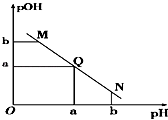
A.M点所示溶液导电能力强于Q点
B.N点所示溶液中c(CH3COO﹣)>c(Na+)
C.M点和N点所示溶液中水的电离程度不相同
D.Q点消耗NaOH溶液的体积小于醋酸溶液的体积
【答案】D
【解析】解:A.Q点的pOH=pH,溶液为中性,由于醋酸是弱酸,电离程度很小,离子浓度也较小,醋酸溶液中离子浓度小于Q点溶液中离子浓度,故M点溶液的导电能力较弱,故A错误;B.N点所示溶液为碱性,则c(H+)<c(OH﹣),由电荷守恒:c(H+)+c(Na+)=c(CH3COO﹣)+c(OH﹣),可得:c(Na+)>c(CH3COO﹣),故B错误;
C.M点的溶液中氢氧根离子源于水的电离,N点氢氧根离子源于水的电离,由于M点的H+浓度等于N点的OH﹣浓度,所以两点水电离程度相同,故C错误;
D.Q点的pOH=pH,溶液为中性,而两者等体积混合后生成醋酸钠,水解显碱性,则醋酸稍过量些,所加NaOH溶液体积略小于醋酸溶液的体积,故D正确.
故选D.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】关于酸、碱、盐的下列各种说法中,正确的是
A. 化合物电离时,生成的阳离子有氢离子的是酸
B. 化合物电离时,生成的阴离子有氢氧根离子的是碱
C. 化合物电离时,生成金属阳离子(或NH4+)和酸根离子的是盐
D. NH4Cl电离的电离方程式是:NH4Cl=NH4++Cl-,所以NH4Cl不是盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锡为第IVA族具有可变价的金属元素,其单质沸点为2260℃。四氯化锡(SnCl4)是无色液体,熔点-33℃,沸点114℃,极易水解,在潮湿的空气中发烟。实验室中可用氯气与过量金属锡通过下图装置制备SnCl4 (夹持装置已略去)。
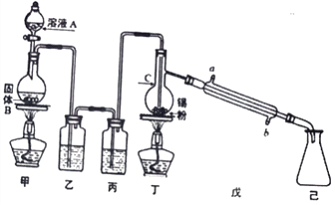
(1)仪器C的名称为___________,装置乙中的试剂是_____________。
(2)装置甲中发生反应的化学方程式为___________________________________。
(3)氯气与锡的反应类似与铁的反应,但该实验中对装置丁要持续加热,其原因是_____________。
(4)你认为该实验装置需要进行的改进是:__________________________________________。
(5)用下列方法和步骤测定所用金属锡样品的纯度(杂质不参加反应)
①将2.000g锡完全溶于过量稀盐酸中,并用所得溶液去还原过量的FeCl3稀溶液,最后得100.00mL 溶液。写出第二步反应的离子方程式:_____________________________。
②取①所得溶液amL用0.100 mol·L-1 的K2Cr2O7溶液滴定,发生如下反应:6FeCl2+ K2Cr2O7+ 14HCl=6FeCl3+2KCl+2CrCl3+7H2O。
K2Cr2O7溶液应注入到____式(填"酸或碱”) 滴定管中。到达滴定终点时用去bmL。则样品中锡的质量分数为_______%(用含a、b 的最简代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒是一种重要的合金元素,还用于催化剂和新型电池。从含钒固体废弃物(含有SiO2、Al2O3及其他残渣)中提取钒的一种新工艺主要流程如下:
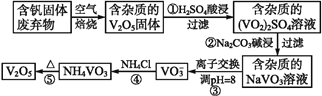
部分含钒化合物在水中的溶解性如下表:
物质 | V2O5 | NH4VO3 | VOSO4 | (VO2)2SO4 |
溶解性 | 难溶 | 难溶 | 可溶 | 易溶 |
请回答下列问题:
(1)反应①所得溶液中除H+之外的阳离子有______。
(2)反应②碱浸后滤出的固体主要成分是______(写化学式)。
(3)反应④的离子方程式为__________。
(4)25 ℃、101 kPa时,4Al(s)+3O2(g)![]() 2Al2O3(s) ΔH1= —a kJ·mol-1,4V(s)+5O2(g)
2Al2O3(s) ΔH1= —a kJ·mol-1,4V(s)+5O2(g)![]() 2V2O5(s) ΔH2=—b kJ·mol-1。用V2O5发生铝热反应冶炼金属钒的热化学方程式是___________。
2V2O5(s) ΔH2=—b kJ·mol-1。用V2O5发生铝热反应冶炼金属钒的热化学方程式是___________。
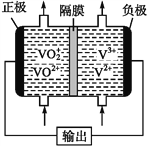
(5)钒液流电池(如下图所示)具有广阔的应用领域和市场前景,该电池中隔膜只允许H+通过。电池放电时负极的电极反应式为_______,电池充电时阳极的电极反应式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式中正确的是( )
A.KOH═K++OH﹣ B.NaHCO3═Na++H++CO32﹣
C.H2SO4═2H++SO42﹣ D.Fe2(SO4)3═Fe23++3SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种元素同周期,且从左到右按原子序数的递增(原子序数为五个连续的自然数)的顺序排列如下:
![]()
下列说法正确的是
A. 若HnCOm为强酸,则D元素肯定是活泼的非金属元素
B. 若A(OH)n为强碱,则B(OH)m也一定为强碱
C. 若C的最高正化合价为+5价,则五种元素均为非金属元素
D. 若D的最低负化合价为-2价,则E的最高正价为+6价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴化碘(IBr)的化学性质与卤素单质相似,能与大多数金属反应生成金属卤化物,和某些非金属单质反应生成相应的卤化物,跟水反应的方程式为IBr+H2O==HBr+HIO。下列有关IBr的叙述中,不正确的是
A. IBr的电子式:![]()
B. IBr和Zn的反应化学方程式2IBr+2Zn==ZnI2+ZnBr2
C. IBr和NaOH溶液反应生成NaBr和NaIO
D. IBr和水反应时,既是氧化剂又是还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com