
【题目】下列离子方程式改写成化学方程式正确的是( )
A.Zn2++2OH﹣═Zn(OH)2↓? ZnCO3+2NaOH═Zn(OH)2↓+Na2CO3
B.Ba2++SO ![]() ═BaSO4↓????? Ba(OH)2+H2SO4═BaSO4↓+2H2O
═BaSO4↓????? Ba(OH)2+H2SO4═BaSO4↓+2H2O
C.Ag++Cl﹣═AgCl↓????? AgNO3+KCl═AgCl↓+KNO3
D.Cu+2Ag+═Cu2++2Ag???? Cu+2AgCl═CuCl2+2Ag
【答案】C
【解析】解:A.Zn2++2OH﹣═Zn(OH)2↓ 表示可溶性锌盐和可溶性强碱反应且不生成除了氢氧化锌外的难溶性物质;碳酸锌是难溶性固体,应该写化学式,正确的如:ZnSO4+2NaOH═Zn(OH)2↓+Na2SO4 , 故A错误;B.Ba2++SO ![]() ═BaSO4表示可溶性钡盐和可溶性硫酸盐或硫酸反应生成硫酸钡沉淀,但不能生成其它弱电解质水或非电解质,该离子方程式中还生成水,正确的如:Ba(OH)2+Na2SO4═BaSO4↓+2NaOH,故B错误;
═BaSO4表示可溶性钡盐和可溶性硫酸盐或硫酸反应生成硫酸钡沉淀,但不能生成其它弱电解质水或非电解质,该离子方程式中还生成水,正确的如:Ba(OH)2+Na2SO4═BaSO4↓+2NaOH,故B错误;
C.Ag++Cl﹣═AgCl↓ 表示硝酸银和可溶性氯化物或盐酸反应离子方程式,正确的如AgNO3+KCl═AgCl↓+KNO3 , 故C正确;
D.Cu+2Ag+═Cu2++2Ag 表示铜和可溶性银盐的反应,氯化银是沉淀,应该写化学式,正确的如Cu+2AgNO3═Cu(NO3)2+2Ag,故D错误;
故选C.


科目:高中化学 来源: 题型:
【题目】在银锌原电池中,以硫酸铜为电解质溶液,锌为极,电极上发生的是反应(“氧化”或“还原”),电极反应式为 , 锌片上观察到的现象为;银电极上的电极反应式是 , 银片上观察到的现象是 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰锂电池的体积小、性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2 . 回答下列问题: 
(1)外电路的电流方向是由极流向极(填字母).
(2)电池正极反应式 .
(3)是否可用水代替电池中的混合有机溶剂?(填“是”或“否”),原因是 .
(4)MnO2可与KOH和KClO3在高温下反应,生成K2MnO4 , 反应的化学方程式为 . K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.
(1)蓄电池在放电时起原电池作用,在充电时起电解池的作用.铅蓄电池在放电时发生的电池反应式为: .
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu═2FeCl2+CuCl2 , 若将此反应设计成原电池,则负极所用电极材料为 , 当线路中转移0.2mol电子时,则被腐蚀铜的质量为g
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为 .
A.铝片、铜片
B.铜片、铝片
C.铝片、铝片
(4)燃料电池是一种高效、环境友好的供电装置,如图是甲烷燃料电池原理示意图, 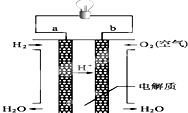
回答下列问题:
①氢氧燃料电池的总反应化学式是: .
②电池工作一段时间后电解质溶液的pH(填“增大”、“减小”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,6﹣已二酸(G)是合成尼龙的主要原料之一,可用含六个碳原子的有机化合物氧化制备.如图为A通过氧化反应制备G的反应过程(可能的反应中间物质为B、C、D、E和F): 
回答下列问题:
(1)化合物A中含碳87.8%,其余为氢,A的化学名称为 .
(2)B到C的反应类型为 .
(3)F的结构简式为 .
(4)在上述中间物质中,核磁共振氢谱出峰最多的是 , 最少的是 . (填化合物代号)
(5)由G合成尼龙的化学方程式为 .
(6)由A通过两步反应制备1,3﹣环已二烯的合成路线为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知C﹣C单键可以绕键轴旋转,其结构简式可表示为 ![]() 的烃,下列说法中正确的是( )
的烃,下列说法中正确的是( )
A.分子中只可能有4 个碳原子处于同一直线上
B.该烃的一氯代物最多有四种
C.分子中至少有10个碳原子处于同一平面上
D.该烃是苯的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素的部分性质数据如下:
元素 | T | X | Y | Z | W |
原子半径(nm) | 0.037 | 0.075 | 0.099 | 0.102 | 0.143 |
最高或最低化合价 | +1 | +5﹣3 | +7﹣1 | +6﹣2 | +3 |
(1)Z离子的结构示意图为 .
(2)关于Y、Z两种元素,下列叙述正确的是(填序号). a.简单离子的半径 Y>Z
b.气态氢化物的稳定性Y比 Z强
c.最高价氧化物对应水化物的酸性Z比Y强
(3)甲是由T、X两种元素形成的10e﹣分子,乙是由Y、W两种元素形成的化合物.某同学设计了如图所示装置(夹持仪器省略)进行实验,将甲的浓溶液逐滴加入到NaOH固体中,烧瓶中即有甲放出,原因是 . 一段时间后,观察到试管中的现象是 , 发生反应的离子方程式是 . 
(4)T,X两种元素形成XT5固体,它的所有原子的最外层都符合相应稀有气体原子的最外层结构,则其电子式为 .
(5)XO2是导致光化学烟雾的“罪魁祸首”之一.它被氢氧化钠溶液吸收的化学方程式是:2XO2+2NaOH═M+NaXO3+H2O(已配平),产物M中元素X的化合价为 .
(6)常温下,Z2Y2是一种橙黄色液体,广泛用于橡胶工业的硫化机,其分子结构与双氧水分子相似.试写出其结构式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.在20℃,1.01×105Pa时,22.4L甲烷(CH4)所含的原子数为5NA
B.常温常压下,28g氮气所含的原子数为2NA
C.标准状况下,22.4L水所含有的分子数目为NA
D.0.5mol H2O所含的电子数目为9 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在配制一定物质的量浓度的盐酸时,下列错误操作可使所配制溶液浓度偏高的是
A.用量筒量取浓盐酸时仰视读数
B.溶解搅拌时有液体飞溅
C.定容时仰视容量瓶瓶颈刻度线
D.摇匀后见液面下降,再加水至刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com