
【题目】某活动小组利用下图装置验证NO的还原性及探究工业生产硝酸的原理. 
(1)如何检查该装置气密性 .
(2)向广口瓶①中通入NO并测定NO的体积
通入NO前,向广口瓶①中加入水,让水充满广口瓶①,且调节滴定管中液面与①相平并记录滴定管的刻度.
从导管a通入一定量的NO并准确测定通入NO的体积的主要操作:;计算出通入的NO的体积为VmL(V<50mL).
(3)验证NO的还原性;探究工业生产硝酸的原理
A、停止通入NO后关闭K1、K3 , 打开K2 , 从导管b缓缓通入O2 , 写出通入O2过程中发生的化学反应方程式;
B、继续通入O2 , 打开K3并及时调整滴定管③液面与广口瓶①中液面相平.
Ⅰ.当通入氧气的体积为 ![]() 时,则广口瓶①的气体体积为;
时,则广口瓶①的气体体积为;
Ⅱ.当广口瓶①的气体体积为 ![]() ,则通入氧气的体积可能为 .
,则通入氧气的体积可能为 .
【答案】
(1)关闭K1、K2 , 打开K3 , 从滴定管上口加水,没过广口瓶①中长导管口,继续加水,使广口瓶①中长导管内外出现一段液柱,停止加水,静置一段时间后,若这段液柱不变,说明装置气密性好,反之,说明装置气密性不好
(2)关闭K2 , 打开K3 , K1 , 通入一定量的NO并调整滴定管液面与①中液面相平,再次读取滴定管刻度
(3)2NO+O2=2NO2;3NO2+H2O=2HNO3+NO;![]() ;
;![]()
【解析】解:(1)关闭K1、K2 , 打开K3 , 从滴定管上口加水,没过广口瓶①中长导管口,继续加水,使广口瓶①中长导管内外出现一段液柱,停止加水,静置一段时间后,若这段液柱不变,说明装置气密性好,反之,说明装置气密性不好,所以答案是:关闭K1、K2 , 打开K3 , 从滴定管上口加水,没过广口瓶①中长导管口,继续加水,使广口瓶①中长导管内外出现一段液柱,停止加水,静置一段时间后,若这段液柱不变,说明装置气密性好,反之,说明装置气密性不好;(2)广口瓶①中压强均与外界相同,通过调节两端液面,到两端高度相同时再读取体积.具体操作为:关闭K2 , 打开K3 , K1 , 通入NO并调整滴定管液面与①中液面相平,再次记录滴定管刻度,所以答案是:关闭K2 , 打开K3 , K1 , 通入一定量的NO并调整滴定管液面与①中液面相平,再次读取滴定管刻度;(3)A、NO易与氧气反应2NO+O2═2NO2 生成红棕色的NO2 , NO2又与水反应3NO2+H2O═2HNO3+NO,颜色变浅,所以答案是:2NO+O2=2NO2;3NO2+H2O=2HNO3+NO;B、Ⅰ.设 ![]() 的氧气参加反应时,需要一氧化氮的体积为x,
的氧气参加反应时,需要一氧化氮的体积为x,
4NO+3O2+2H2O═4HNO3
4 3
x ![]()
所以x= ![]() <V,所以一氧化氮剩余,剩余的一氧化氮为V﹣
<V,所以一氧化氮剩余,剩余的一氧化氮为V﹣ ![]() ,
,
所以答案是: ![]() ;
;
Ⅱ.剩余的气体可能是氧气或一氧化氮,
①当剩余的气体为氧气时,一氧化氮不足量,以一氧化氮为标准进行金属,
设参加反应的氧气为Y,
4NO+3O2+2H2O═4HNO3
4 3
V Y
Y= ![]() ,
,
所以通入的氧气体积为 ![]() ,
,
②当剩余的气体为一氧化氮时,氧气的量不足,以氧气的量为标准进行计算,
参加反应的一氧化氮为V﹣ ![]() ,
,
设参加反应的氧气为Z,
4NO+3O2+2H2O═4HNO3
4 3![]() Z
Z
Z= ![]()
所以答案是: ![]() .
.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】某氧化物难溶于水,可溶于烧碱溶液,生成易溶于水的化合物,取所得溶液,逐滴滴入过量稀盐酸,立即生成白色沉淀且逐渐增多,则原氧化物为
A.MgOB.Al2O3 C.SiO2D.SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】古语道:“人要实,火要虚”。此话的意思是做人必须脚踏实地,事业才能有成;燃烧固体燃料需要架空,燃烧才能更旺。从燃烧的条件看,“火要虚”的实质是( )
A. 增大可燃物的热值 B. 提高空气中氧气的含量
C. 提高可燃物的着火点 D. 增大可燃物与空气的接触面积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为常见金属,X,Y为常见非金属,X,E,F,G常温下为气体,C为液体,B是一种盐,受热极易分解,在工农业生产中用途较广(如被用作某些电池的电解质).现用A与石墨作电极,B的浓溶液作电解质,构成原电池.有关物质之间的转化关系如下图:(注意:其中有些反应的条件及部分生成物被略去) 
请填写下列空白:
(1)反应④为A在某种气体中燃烧,生成单质Y和A的氧化物,其反应方程式为 .
(2)A与石墨作电极,B的浓溶液作电解质,构成原电池,
负极反应:;正极反应: .
(3)从D溶液制备D的无水晶体的“操作A”为 .
(4)反应②的化学方程式为 .
(5)反应⑤的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“张﹣烯炔环异构化反应”,可高效构筑五元环状化合物: 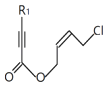
![]()
 (R1代表氢原子或烃基) 某五元环状化合物的合成路线如图:
(R1代表氢原子或烃基) 某五元环状化合物的合成路线如图: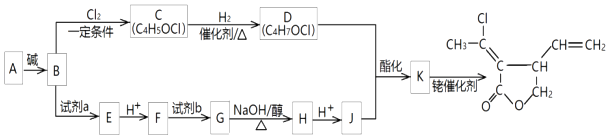
已知: ![]() +
+ ![]()
![]()
![]() +H2O
+H2O
(1)A中所含官能团名称是;B→C的反应类型是 .
(2)A→B的化学方程式是 ![]() .
.
(3)D的结构简式是 .
(4)下列叙述中正确的是 . ①B能使酸性KMnO4和Br2的四氯化碳溶液均褪色
②试剂a一定是银氨溶液
③J、A的核磁共振氢谱峰面积之比均为3:1
(5)与F具有相同官能团的同分异构体(不含顺反异构)的结构简式有 .
(6)试剂b为Cl2 , G→H反应的化学方程式是 .
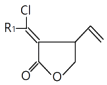
(7)D与J反应形成K的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸、硝酸和盐酸既是重要的化工原料也是化学实验室里必备的试剂.
(1)常温下,可用铝槽车装运浓硫酸,这是因为浓硫酸具有性;硝酸应保存在棕色试剂瓶中,这是因为硝酸具有性;敞口放置的浓盐酸浓度会减小,这是因为盐酸具有性.
(2)①在100mL 18molL﹣1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积为13.44L,则参加反应的铜片的质量为(选填序号);
a.115.2g b.76.8g c.57.6g d.38.4g
②若使上述①中反应剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式: .
(3)工业制盐酸是以电解饱和氯化钠溶液为基础进行的,该电解过程中阳极的电极反应式为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砒霜的主要成分是As2O3,有剧毒,致死量为0.1 g。As2O3是两性偏酸性氧化物,微溶于水,生成H3AsO3;该酸及其对应的盐也均有毒性,其中碱金属对应的盐溶于水,其他金属对应的盐均几乎不溶于水。下列关于处理一瓶含有砒霜废液的方案正确的是( )
A.直接倒入下水道
B.经过滤后倒入下水道
C.加入足量生石灰后,倒入指定地点
D.加入足量氢氧化钠后,倒入指定地点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列溶液中各组离子一定大量共存的是( )
A.使甲基橙呈红色的溶液中:Na+、AlO2﹣、NO3﹣、CO32﹣
B.c(ClO﹣)=1.0 mol?L﹣1溶液:Na+、SO32﹣、S2﹣、Cl﹣
C.含有0.1 mol?L﹣1 HCO3﹣的溶液:Na+、Fe3+、NO ![]() 、C6H5O﹣
、C6H5O﹣
D.![]() =0.1 mol?L﹣1的溶液:Na+、K+、CO32﹣、NO3﹣
=0.1 mol?L﹣1的溶液:Na+、K+、CO32﹣、NO3﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com